Книга: Общая химия
КРЕМНИЙ (SILICIUM) 178. Кремний в природе. Получение и свойства кремния.
| <<< Назад 177. Природные и синтетические высокомолекулярные соединения (полимеры). |
Вперед >>> 179. Соединения кремния с водородом и галогенами. |
КРЕМНИЙ (SILICIUM)
178. Кремний в природе. Получение и свойства кремния.
Кремний — один из самых распространенных в земной коре элементов. Он составляет 27% (масс.) доступной нашему исследованию части земной коры, занимая по распространенности второе место после кислорода. В природе кремний встречается только в соединениях: в виде диоксида (двуокиси) кремния SiO2, называемого также кремниевым ангидридом или кремнеземом, и в виде солей кремниевых кислот (силикатов), Наиболее широко распространены в природе алюмосиликаты, т. е. силикаты, в состав которых входиф, алюминий, К ним относятся полевые шпаты, слюды, каолин и др.
- 492 -
Как углерод, входя в состав всех органических веществ, является важнейшим элементом растительного и животного царства, Так кремний — главный элемент в царстве минералов и горных пород.
В большинстве организмов содержание кремния очень невелико. Однако некоторые морские организмы накапливают большие количества кремния. К богатым им морским растениям относятся диатомовые водоросли, из животных много кремния содержат радиолярии, кремниевые губки.
Свободный кремний можно получить прокаливанием с магнием мелкого белого песка, который представляет собой диоксид кремния:
SiO2 + 2Mg = 2MgO +Si
При этом образуется бурый порошок аморфного кремния.
Кремний растворим в расплавленных металлах. При медленном охлаждении раствора кремния в цинке или в алюминии кремний выделяется в виде хорошо образованных кристаллов октаэдрической формы. Кристаллический кремний обладает стальным блеском.
Кристаллы кремния высокой чистоты, имеющие минимальное число дефектов структуры, характеризуются очень низкой электрической проводимостью. Примеси и нарушения правильности строения резко увеличивают их проводимость.
Кремний применяется главным образом в металлургии и в полупроводниковой технике. В металлургии он используется для удаления кислорода из расплавленных металлов и служит составной частью многих сплавов. Важнейшие из них — это сплавы на основе железа, меди и алюминия. В полупроводниковой технике кремний используют для изготовления фотоэлементов, усилителей, выпрямителей. Полупроводниковые приборы на основе кремния выдерживают нагрев до 250°C, что расширяет область их применения.
В промышленности кремний получают восстановлением диоксида кремния коксом в электрических печах:
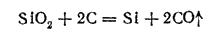
Полученный по этому способу кремний содержит 2-5% примесей. Необходимый для изготовления полупроводниковых приборов кремний высокой чистоты получают более сложным путем. Природный кремнезем переводят в такое соединение кремния, которое поддается глубокой очистке. Затем кремний выделяют из полученного чистого вещества термическим разложением или действием восстановителя. Один из таких методов состоит в превращении кремнезема в хлорид кремния SiCl4, очистке этого продукта и восстановлении из него кремния высокочистым цинком, Весьма чистый кремний можно получить также термическим разложением иодида кремния SiI4 или силана SiH4.
- 493 -
Получающийся кремний содержит весьма мало примесей и пригоден для изготовления некоторых полупроводниковых приборов. Для получения еще более чистого продукта его подвергают дополнительной очистке, например зонной плавке (см. § 193).
В химическом отношении кремний, особенно кристаллический, малоактивен; при комнатной температуре он непосредственно соединяется только с фтором. При нагревании аморфный кремний легко соединяется с кислородом, галогенами и серой.
Кислоты, кроме смеси фтороводорода и азотной кислоты, не действуют на кремний, но щелочи энергично реагируют с ним, выделяя водород и образуя соли кремниевой кислоты H2SiO3:
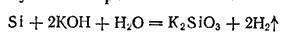
В присутствии следов щелочи, играющей роль катализатора, кремний вытесняет водород также из воды.
Если накаливать в электрической печи смесь песка и кокса, взятых в определенном соотношении, то получается соединение кремния с углеродом — карбид кремния SiC , называемый карборундом:
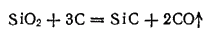
Чистый карборунд — бесцветные очень твердые кристаллы (плотность 3,2 г/см3). Технический продукт обычно окрашен примесями в темно-серый цвет.
По внутреннему строению карборунд представляет собой как бы алмаз, в котором половина атомов углерода равномерно заменена атомами кремния. Каждый атом углерода находится в центре тетраэдра, в вершинах которого расположены атомы кремния; в свою очередь каждый атом кремния окружен подобным же образом четырьмя атомами углерода. Ковалентные связи, соединяющие все атомы в этой структуре, как и в алмазе, очень прочны. Этим объясняется большая твердость карборунда.
Карборунд получают в больших количествах; применение его разнообразно и связано с его высокой твердостью и огнеупорностью. Из порошка карборунда изготовляют шлифовальные круги, бруски, шлифовальную бумагу. На его основе производят плиты для сооружения полов, платформ и переходов в метро и на вокзалах. Из него готовят муфели и футеровку для различных печей. Смесь порошков карборунда и кремния служит материалом для изготовления силитовых стержней для электрических печей.
При высокой температуре кремний вступает в соединение со многими металлами, образуя силициды. Например, при нагревании диоксида кремния с избытком металлического магния восстанавливающийся кремний соединяется с магнием, образуя силицид магния Mg2Si:
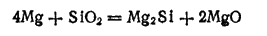
- 494 -
| <<< Назад 177. Природные и синтетические высокомолекулярные соединения (полимеры). |
Вперед >>> 179. Соединения кремния с водородом и галогенами. |
- 152. Углерод в природе.
- 153. Аллотропия углерода.
- 154. Химические свойства углерода. Карбиды.
- 155. Диоксид углерода. Угольная кислота.
- 156. Оксид углерода (II).
- 157. Соединения углерода с серой и азотом.
- 158. Топливо и его виды.
- 159. Газообразное топливо.
- 160. Общая характеристика органических соединений.
- 161. Отличительные особенности органических соединений.
- 162. Теория химического строения органических соединений.
- 163. Классификация органических соединений.
- 164. Предельные (насыщенные) углеводороды.
- 165. Непредельные (ненасыщенные) углеводороды.
- 166. Предельные циклические углеводороды.
- 167. Ароматические углеводороды.
- 168. Галогенпроизводные углеводородов.
- 169. Спирты и фенолы.
- 170. Простые эфиры.
- 171. Альдегиды и кетоны.
- 172. Карбоновые кислоты.
- 173. Сложные эфиры карбоновых кислот. Жиры.
- 174. Углеводы.
- 175. Амины.
- 176. Аминокислоты и белки.
- 177. Природные и синтетические высокомолекулярные соединения (полимеры).
- КРЕМНИЙ (SILICIUM) 178. Кремний в природе. Получение и свойства кремния.
- 179. Соединения кремния с водородом и галогенами.
- 180. Диоксид кремния.
- 181. Кремниевые кислоты и их соли.
- 182. Стекло.
- 183. Керамика.
- 184. Цемент.
- 185. Кремнийорганические соединения.
- 186. Германий (Germanium).
- 187. Олово (Stannuin).
- 188. Свинец (Plumbum).
- 189. Свинцовый аккумулятор.
- 179. Соединения кремния с водородом и галогенами.
- Получение и использование синтетических полимеров
- Глава 7 Получение нуклеотидов из продуктов атмосферной фотохимии
- Получение нуклеотидов
- Глава 21 По ту сторону физики Получение знания, имеющего смысл, но неизмеримого экспериментально…
- Получение кристаллов с определенными свойствами
- Получение кристаллов с заданным химическим составом
- Получение кристаллов заданной формы
- Получение крупногабаритных кристаллов
- КРЕМНИЙ
- 8.35. ПОЛУЧЕНИЕ ФЕНОЛА — НЕЛЕГКАЯ ЗАДАЧА
- Кремний и жизнь
