Книга: Общая химия
Глава XIX. ВТОРАЯ ГРУППА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ
| <<< Назад 208. Влияние координации на свойства лигандов и центрального атома. |
Вперед >>> 209. Бериллий (Beryllium). |
Глава XIX. ВТОРАЯ ГРУППА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ
В главную подгруппу II группы входят элементы бериллий, магний, кальций, стронций, барий и радий. Все эти элементы, кроме бериллия, обладают ярко выраженными металлическими свойствами. В свободном состоянии они представляют собой серебристо-белые вещества, более твердые, чем щелочные металлы, с довольно высокими температурами плавления. По плотности все они, кроме радия, относятся к легким металлам. Их важнейшие свойства приведены в табл. 32.
Первые два члена рассматриваемой подгруппы занимают в ней несколько особое положение, отличаясь во многих отношениях от остальных четырех элементов. Бериллий по некоторым своим свойствам приближается к алюминию («диагональное сходство» — см. стр. 590).
Все изотопы последнего элемента подгруппы — радия — радиоактивны. Долгоживущий изотоп 226Ra раньше использовался в радиотерапии; в настоящее время его заменили более дешевыми изотопами других элементов, образующимися в ядерных реакторах.
В наружном электронном слое атомы элементов этой подгруппы имеют два электрона, во втором снаружи слое у бериллия находится два электрона, а у остальных элементов — восемь. Два электрона внешнего слоя сравнительно легко отщепляются от атомов, которые превращаются при этом в положительные двухзарядные ионы. Поэтому в отношении химической активности эти элементы лишь немного уступают щелочным металлам. Подобно последним, они довольно быстро окисляются на воздухе и могут вытеснять водород из воды при комнатной температуре. Однако бериллий и магний взаимодействуют с водой очень медленно, так как образующиеся при этом гидроксиды малорастворимы в воде: покрывая поверхность металла, они затрудняют дальнейшее течение реакции. Остальные четыре металла ввиду лучшей растворимости их гидроксидов реагируют с водой значительно энергичнее.
- 588 -
Таблица 32, Некоторые свойства бериллия, магния, радия и щелочноземельных металлов
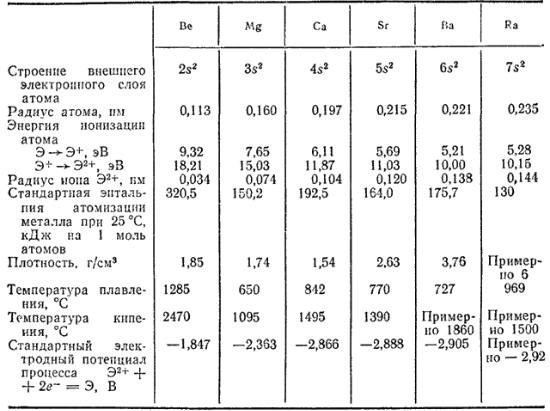
Входящие в состав главной подгруппы кальций, стронций и барий издавна получили название щелочноземельных металлов. Происхождение этого названия связано с тем, что гидроксиды кальция, стронция и бария, так же, как и гидроксиды натрия и калия, обладают щелочными свойствами, оксиды же этих металлов по их тугоплавкости сходны с оксидами алюминия и тяжелых металлов, носившими прежде общее название земель.
При сжигании щелочноземельных металлов всегда получаются оксиды. Пероксиды, поскольку они вообще образуются, гораздо менее стойки, чем пероксиды щелочных металлов.
Оксиды кальция, стронция и бария непосредственно соединяются с водой, образуя гидроксиды. Растворимость последних сильно увеличивается при переходе от кальция к следующим щелочноземельным металлам. В такой же последовательности увеличиваются и основные свойства гидроксидов.
Щелочноземельные металлы могут соединяться с водородом, образуя гидриды, аналогичные гидридам щелочных металлов (например, CaH2).
Замечательна склонность щелочноземельных металлов соединяться с азотом, возрастающая по мере увеличения их атомной массы.
- 589 -
Уже при комнатной температуре щелочноземельные металлы медленно соединяются с азотом, образуя нитриды.
В отличие от солей щелочных металлов, многие из солей щелочноземельных металлов малорастворимы в воде. К таким солям относятся карбонаты, сульфаты, фосфаты и некоторые другие.
Во всех своих соединениях щелочноземельные металлы имеют степень окисленности +2.
| <<< Назад 208. Влияние координации на свойства лигандов и центрального атома. |
Вперед >>> 209. Бериллий (Beryllium). |
- XIX. Болезнь Альцгеймера
- Идеология и наука XIX века – основы современного знания
- В XIX веке
- Открытия и исследования в Антарктике в XIX — XX вв.
- Соловей (рис. XIX)
- XIX.2 Разрушение шаг за шагом при болезни Альцгеймера
- XIX.3 «Use it or lose it»: реактивация нейронов при болезни Альцгеймера
- Часть I. Теории и дискуссии о законах наследственности: от античности до XIX века
- XIX.4 Боль при деменции
- XIX.1 Старение мозга, болезнь Альцгеймера и прочие формы деменции
- XIX. 5 Болезнь Альцгеймера и выбор момента добровольного ухода из жизни
- 1.4. Кометы, планеты, спутники: открытия XVIII–XIX вв.
