Книга: Общая химия
186. Германий (Germanium).
| <<< Назад 185. Кремнийорганические соединения. |
Вперед >>> 187. Олово (Stannuin). |
186. Германий (Germanium).
Этот элемент, существование которого было в 1871 г. предсказано Д. И. Менделеевым на основе периодического закона, открыт в 1886 г. немецким химиком Винклером (см. § 19). Общее содержание германия в земной коре составляет около 0,0007% (масс.). Минералы, содержащие германий в сколько-нибудь значительных количествах, крайне редки. Источником получения германия обычно служат побочные продукты, получающиеся при переработке руд цветных металлов, а также зола от сжигания некоторых углей.
В компактном состоянии германий имеет серебристый цвет и по внешнему виду похож на металл. При комнатной температуре он устойчив к действию воздуха, кислорода, воды, соляной и разбавленной серной кислот. Азотная и концентрированная серная кислоты окисляют его до диоксида GeO2, особенно при нагревании
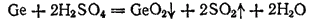
Германий взаимодействует также со щелочами в присутствии пероксида водорода. При этом образуются соли германиевой кислоты — германаты, например:
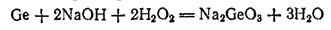
Соединения германия(II) малоустойчивы. Гораздо более характерны для германия соединения, в которых степень его окисленности равна +4.
Диоксид германия GeO2 — белые кристаллы плотностью 4,703 г/см3, заметно растворимые в воде, причем раствор проводит электрический ток. Получают GeO2 различными способами; в частности, он может быть получен нагреванием германия в кислороде или окислением его концентрированной азотной кислотой.
Диоксид германия — амфотерное соединение с сильно преобладающими кислотными свойствами, вследствие чего он легко растворяется в щелочах, образуя германаты.
Германоводороды. Действуя на хлорид германия GeCl4 амальгамой иатрия в токе водорода или же разлагая кислотами сплав германия с магнием, можно получить тетрагидрид германия GeH4. Это бесцветный газ, который аналогично гидриду мышьяка при нагревании разлагается, образуя на стенках реакционного сосуда металлическое зеркало.
При получении простейшего германоводорода - образуются в небольшом количестве его гомологи Ge2H6 и Ge3H8.
Германий обладает полупроводниковыми свойствами и с этим связано его основное применение. Германий, идущий для изготовления полупроводниковых приборов, подвергается очень тщательной очистке.
- 505 -
Она осуществляется различными способами. Один из важнейших методов получения высокочистого германия — это зонная плавка (см. § 193). Для придания очищенному германию необходимых электрических свойств в него вводят очень небольшие количества определенных примесей. Такими примесями служат элементы пятой и третьей групп периодической системы, например, мышьяк, сурьма, алюминий, галлий. Полупроводниковые приборы из германия (выпрямители, усилители) широко применяются в радио- и телевизионной технике, в радиолокации, в счетно-решающих устройствах. Из германия изготовляют также термометры сопротивления.
Из соединений германия применяют, например, GeO2, который входит в состав стекол, обладающих высоким коэффициентом преломления и прозрачностью в инфракрасной части спектра.
| <<< Назад 185. Кремнийорганические соединения. |
Вперед >>> 187. Олово (Stannuin). |
- 152. Углерод в природе.
- 153. Аллотропия углерода.
- 154. Химические свойства углерода. Карбиды.
- 155. Диоксид углерода. Угольная кислота.
- 156. Оксид углерода (II).
- 157. Соединения углерода с серой и азотом.
- 158. Топливо и его виды.
- 159. Газообразное топливо.
- 160. Общая характеристика органических соединений.
- 161. Отличительные особенности органических соединений.
- 162. Теория химического строения органических соединений.
- 163. Классификация органических соединений.
- 164. Предельные (насыщенные) углеводороды.
- 165. Непредельные (ненасыщенные) углеводороды.
- 166. Предельные циклические углеводороды.
- 167. Ароматические углеводороды.
- 168. Галогенпроизводные углеводородов.
- 169. Спирты и фенолы.
- 170. Простые эфиры.
- 171. Альдегиды и кетоны.
- 172. Карбоновые кислоты.
- 173. Сложные эфиры карбоновых кислот. Жиры.
- 174. Углеводы.
- 175. Амины.
- 176. Аминокислоты и белки.
- 177. Природные и синтетические высокомолекулярные соединения (полимеры).
- КРЕМНИЙ (SILICIUM) 178. Кремний в природе. Получение и свойства кремния.
- 179. Соединения кремния с водородом и галогенами.
- 180. Диоксид кремния.
- 181. Кремниевые кислоты и их соли.
- 182. Стекло.
- 183. Керамика.
- 184. Цемент.
- 185. Кремнийорганические соединения.
- 186. Германий (Germanium).
- 187. Олово (Stannuin).
- 188. Свинец (Plumbum).
- 189. Свинцовый аккумулятор.
