Книга: Общая химия
167. Ароматические углеводороды.
| <<< Назад 166. Предельные циклические углеводороды. |
Вперед >>> 168. Галогенпроизводные углеводородов. |
167. Ароматические углеводороды.
Очень важную группу образуют циклические углеводороды ароматического ряда; простейшими из них являются бензол C6H6 и его гомологи, например толуол (метилбензол) C6H5-CH3 и этилбензол C6H5-CH2CH3, состав которых отвечает общей формуле CnH2n-6, а строение обычно выражают структурными формулами:
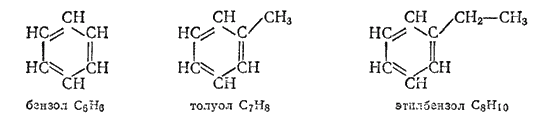
Во всех этих соединениях содержится особая циклическая группировка из шести атомов углерода — бензольное ароматическое ядро. Структурная формула бензольного ядра с чередующимися тремя двойными и тремя простыми связями была предложена еще в 1865 г. немецким химиком А. Кекуле. Для простоты написания бензольное ядро изображают упрощенно в виде шестиугольника, в котором символы С и Н, относящиеся к кольцу, не пишут:
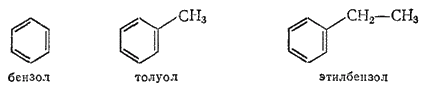
Одновалентный радикал бензола C6H5- или
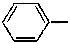
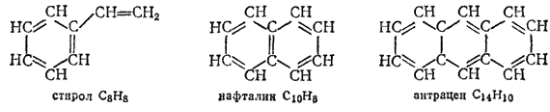
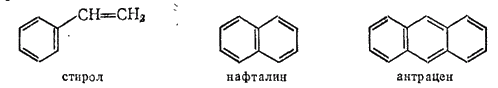
Известны ароматические углеводороды с кратными связями в боковых цепях, например стирол, а также многоядерные, содержащие несколько бензольных ядер, например нафталин и антрацен:
- 460 -
или упрощенно:
Ароматические углеводороды содержатся в каменноугольной смоле, получаемой при коксовании каменного угля. Другим важным источником их получения служит нефть некоторых месторождений, например Майкопского. Чтобы удовлетворить огромную потребность в ароматических углеводородах, их получают также путем каталитической ароматизации ациклических углеводородов нефти.
Эта проблема была успешно разрешена Н. Д. Зелинским и его учениками Б. А. Казанским и А. Ф. Платэ, осуществившими превращение многих предельных углеводородов в ароматические. Так, Из гептана C7H16 при нагревании в присутствии катализатора получается толуол:
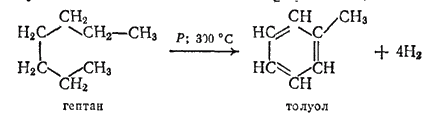
Ароматические углеводороды и их производные широко применяют для получения пластических масс, синтетических красителей, лекарственных и взрывчатых веществ, синтетических каучуков, моющих средств.
Бензол и все соединения, содержащие ядро бензола, названы ароматическими (в начале XIX века), поскольку первыми изученными представителями этого ряда были душистые вещества или соединения, выделенные из природных ароматных веществ. Теперь к этому ряду относят и многочисленные соединения, не имеющие приятного запаха, но обладающие комплексом химических свойств, называемых ароматическими свойствами.
Бензол — бесцветная жидкость с характерным запахом; температура кипения 80,1°C, температура плавления 5,5°C. Ароматические свойства бензола, определяемые особенностями его структуры, выражаются в относительной устойчивости бензольного ядра, несмотря на непредельность бензола по составу. Так, в отличие от непредельных соединений с этиленовыми двойными связями, бензол устойчив к действию окислителей; например, подобно предельным углеводородам, он не обесцвечивает раствор перманганата калия. Реакции присоединения для бензола не характерны, наоборот, для него, как и для других ароматических соединений, характерны реакции замещения атомов водорода в бензольном, ядре. Ниже приведены важнейшие из таких реакций.
- 461 -
Реакция галогенирования. При действии брома или хлора (в присутствии катализаторов) образуются галоген производные:
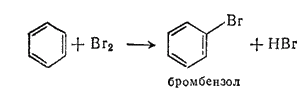
Реакция сульфирования. При действии концентрированной серной кислоты (при нагревании) образуются сульфокислоты:
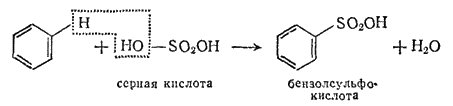
Реакция нитрования. При действии концентрированной азотной кислоты (в присутствии концентрированной H2SO4) образуются нитросоединения:
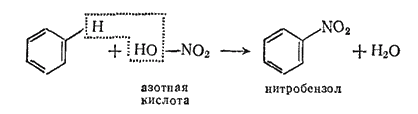
Нитрованием толуола получают взрывчатое вещество — тринитротолуол (тротил, или гол):
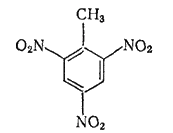
Многие другие ароматические полинитросоединения (содержащие три и более нитрогрупп — NO2) также используются как взрывчатые вещества. Нитросоединения могут быть восстановлены в амины (§ 175).
Из сказанного следует, что формула бензола в виде цикла с чередующимися двойными и простыми связями (формула Кекуле) неточно выражает природу связей между атомами углерода в бензольном ядре. В соответствии с этой формулой в бензоле должно быть три локализованных ?-связи, т. е. три пары ?-электронов, каждая из которых фиксирована между двумя атомами углерода — схема (1); если обозначить эти ?-электроны точками, то строение бензола следует представить схемой (2);
- 462 -
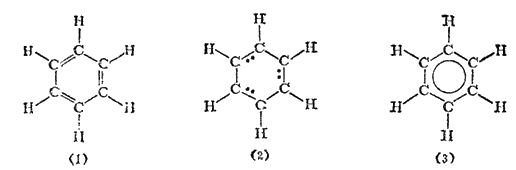
Однако опыт показывает, что в кольце бензола нет обычных двойных связей, чередующихся с простыми, и что все связи между С-атомами в бензоле равноценны. Длина каждой из них (0,140 нм) имеет промежуточное значение по сравнению с длиной простой связи C-C (0.154 нм) и этиленовой двойной связи C=C (0.134 нм) в других (неароматических) органических соединениях.
Каждый из атомов углерода в кольце бензола находится в состоянии sp2-гибридизации и затрачивает по три валентных электрона на образование ?-связей с двумя соседними атомами углерода и с одним атомом водорода. При этом все шесть атомов углерода и все ?-связи C-C и C-H лежат в одной плоскости (рис. 131). Облако четвертого валентного электрона каждого из атомов углерода (т. е. облако р-электрона, не участвующего в гибридизации) имеет форму объемной восьмерки («гантели») и ориентировано перпендикулярно плоскости бензольного кольца. Каждое из таких p-облаков перекрывается над и под плоскостью кольца с р-электронньши облаками двух соседних атомов углерода. Это показано на рис. 132, а и, в проекции, на рис. 132,б. Плотность облаков ?-электронов в бензоле равномерно распределена между всеми связями C-C. Иначе говоря, шесть ?-электронов обобщены всеми углеродными атомами кольца и образуют единое кольцевое облако (ароматический электронный секстет). Так объясняется равноценность (выравненность) ароматических связей, обусловливающих характерные (ароматические) свойства бензольного ядра. Равномерное распределение облака ?-электронов и выравненность связей в бензоле иногда изображают формулой (3) (стр. 462).
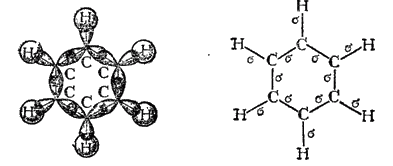
Рис. 131. Схема образования ?-связей в молекуле бензола.
- 463 -
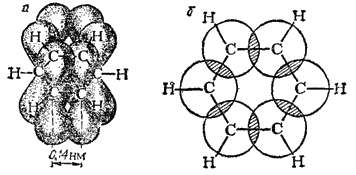
Рис. 132. Схема перекрывания ?-электронных облаков в молекуле бензола.
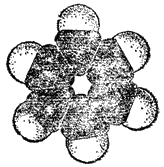
Рис. 133. Сегментовая модель молекулы бензола.
Соответственно, вместо общепринятого символа бензольного ядра в виде шестиугольника с чередующимися двойными и простыми связями, отвечающего формуле Кекуле (1а), бензол изображают шестиугольником с кружочком внутри (3а):

На рис. 133 представлена сегментовая модель молекулы бензола.
С точки зрения метода наложения валентных схем структуру молекулы бензола, представленную формулой (3), следует рассматривать как промежуточную между двумя возможными структурами бензола, выражаемыми формулами Кекуле:
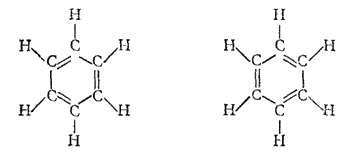
Поскольку в молекуле бензола три электронные пары являются общими для всех шести атомов углерода бензольного кольца, образуемые ими связи — шестицентровые (см, § 44).
| <<< Назад 166. Предельные циклические углеводороды. |
Вперед >>> 168. Галогенпроизводные углеводородов. |
- 152. Углерод в природе.
- 153. Аллотропия углерода.
- 154. Химические свойства углерода. Карбиды.
- 155. Диоксид углерода. Угольная кислота.
- 156. Оксид углерода (II).
- 157. Соединения углерода с серой и азотом.
- 158. Топливо и его виды.
- 159. Газообразное топливо.
- 160. Общая характеристика органических соединений.
- 161. Отличительные особенности органических соединений.
- 162. Теория химического строения органических соединений.
- 163. Классификация органических соединений.
- 164. Предельные (насыщенные) углеводороды.
- 165. Непредельные (ненасыщенные) углеводороды.
- 166. Предельные циклические углеводороды.
- 167. Ароматические углеводороды.
- 168. Галогенпроизводные углеводородов.
- 169. Спирты и фенолы.
- 170. Простые эфиры.
- 171. Альдегиды и кетоны.
- 172. Карбоновые кислоты.
- 173. Сложные эфиры карбоновых кислот. Жиры.
- 174. Углеводы.
- 175. Амины.
- 176. Аминокислоты и белки.
- 177. Природные и синтетические высокомолекулярные соединения (полимеры).
- КРЕМНИЙ (SILICIUM) 178. Кремний в природе. Получение и свойства кремния.
- 179. Соединения кремния с водородом и галогенами.
- 180. Диоксид кремния.
- 181. Кремниевые кислоты и их соли.
- 182. Стекло.
- 183. Керамика.
- 184. Цемент.
- 185. Кремнийорганические соединения.
- 186. Германий (Germanium).
- 187. Олово (Stannuin).
- 188. Свинец (Plumbum).
- 189. Свинцовый аккумулятор.
