Книга: Общая химия
187. Олово (Stannuin).
| <<< Назад 186. Германий (Germanium). |
Вперед >>> 188. Свинец (Plumbum). |
Разделы на этой странице:
187. Олово (Stannuin).
Олово не принадлежит к числу широко распространенных металлов (содержание его в земной коре составляет 0,04 %), но оно легко выплавляется из руд и поэтому стало известно человеку в виде его сплавов с медью (бронзы) со времен глубокой древности. Олово обычно встречается в виде кислородного соединения SnO2 оловянного камня, из которого и получается посредством восстановления углем.
В свободном состоянии олово — серебристо-белый мягкий металл. При сгибании палочки олова слышится характерный треск, обусловленный трением отдельных кристаллов друг о друга. Олово обладает мягкостью и тягучестью и легко может быть прокатано в тонкие листы, называемые оловянной фольгой или станиолем.
Кроме обычного белого олова, кристаллизующегося в тетрагональной системе, существует другое видоизменение олова — серое олово, кристаллизующееся в кубической системе и имеющее меньшую плотность. Белое олово устойчиво при температурах выше 14°C, а серое — при температурах ниже 14°C. Поэтому при охлаждении белое олово превращается в серое. В связи со значительным изменением плотности металл при этом рассыпается в серый порошок. Это явление получило название оловянной чумы. Быстрее всего превращение белого олова в серое протекает при температурах около -30°C; оно ускоряется в присутствии зародышей кристаллов серого олова.
Сплавы олова с сурьмой и медью применяются для изготовления подшипников. Эти сплавы (оловянные баббиты) обладают высокими антифрикционными свойствами. Сплавы олова со свинцом — припои — широко применяются для пайки. В качестве легирующего компонента олово входит в некоторые сплавы меди.
На воздухе олово при комнатной температуре не окисляется, но нагретое выше температуры плавления постепенно превращается в диоксид олова SnO2.
Вода не действует на олово.
- 506 -
Разбавленные соляная и серная кислоты действуют на него очень медленно, что объясняется большим перенапряжением выделения водорода на этом металле. Концентрированные растворы этих кислот, особенно при нагревании, растворяют олово. При этом в соляной кислоте получается хлорид олова (II), а в серной — сульфат олова (IV);
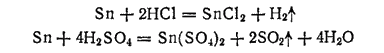
С азотной кислотой олово взаимодействует тем интенсивнее, чем выше концентрация кислоты и температура. В разбавленной кислоте образуется растворимый нитрат олова (II)
4Sn + 10HNO3 = 4Sn(NO3)2 + NH4NO3 + 3H2O
а в концентрированной — соединения олова (IV), главным образом нерастворимая ?-оловянная кислота, состав которой приблизительно соответствует формуле H2SnO3:
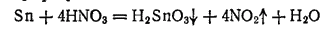
Концентрированные щелочи также растворяют олово. В этом случае получаются станниты — соли оловянистой кислоты H2SnO2:
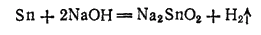
В растворах станниты существуют в гидратированных формах, образуя гидроксостанниты, например:
Na2SnO2 + 2H2O = Na2[Sn(OH)4]
На воздухе олово покрывается тонкой оксидной пленкой, обладающей защитным действием. Поэтому в условиях несильного коррозионного воздействия оно является химически стойким металлом. Около 40% всего выплавляемого олова расходуется для покрытия им изделий из железа, соприкасающихся с продуктами питания, Прежде всего — консервных банок. Это объясняется указанной химической стойкостью олова, а также тем, что оно легко наносится на железо и что продукты его коррозии безвредны.
Олово образует устойчивые соединения, в которых имеет степень окисленности +2 и +4.
Соединения олова (II).
Оксид олова(II) , или окись олова, SnO — темно-бурый порошок, образующийся при разложении гидроксида олова (II) Sn(OH)2 в атмосфере диоксида углерода.
Гидроксид олова (II) Sn(OH)2 получается в виде белого осадка при действии щелочей на соли олова (II):
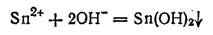
Гидроксид олова (II) — амфотерное соединение. Он легко растворяется как в кислотах, так и в щелочах, в последнем случай с образованием гидроксостаннитов:
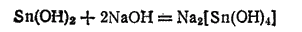
- 507 -
Хлорид олова(II) SnCl2·2H2O образует бесцветные кристаллы. При нагревании или сильном разбавлении хлорида(II) водой происходит его частичный гидролиз с образованней осадка основной соли:
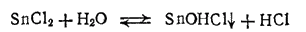
Хлорид олова (II) — восстановитель. Так, хлорид железа (III) FeCl3 восстанавливается им в хлорид железа (II) FeCl2:
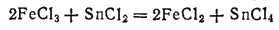
При действии хлорида олова (II) на раствор хлорида ртути (II) (сулемы) HgCl2 образуется белый осадок хлорида ртути (I) (каломели) Hg2Cl2:
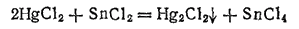
При избытке хлорида олова восстановление идет еще дальше и получается металлическая ртуть:
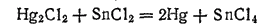
Соединения олова (IV).
Диоксид (или двуокись) олова SnO2 встречается в природе и может быть получен искусственно сжиганием металла на воздухе или окислением его азотной кислотой с последующим прокаливанием полученного продукта. Применяется диоксид олова для приготовления белых глазурей и эмалей.
Гидроксиды олова (IV) называются оловянными кислотами и известны в двух модификациях: в виде ?-оловянной кислоты и в виде ?-оловянной кислоты.
?-Оловянная кислота H2SnO2 может быть получена действием водного раствора аммиака на раствор хлорида олова(IV):
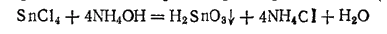
Выпадающий белый осадок при высушивании постепенно теряет воду, превращаясь в диоксид олова. Таким образом кислоты определенного состава получить не удается. Поэтому приведенная выше формула ?-оловянной кислоты является лишь простейшей из возможных. Правильнее было бы изобразить состав этой кислоты формулой mSnO2·nH2O.
?-Оловянная кислота легко растворяется в щелочах, образуя соли, содержащие комплексный анкон [Sn(OH)6]2- и называемые гидроксостаннатами:
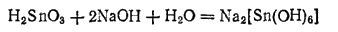
Гидроксостаннат натрия выделяется из растворов в виде кристаллов, состав которых можно выразить формулой Na2SnO3·3H2O. Эта соль применяется в качестве протравы в красильном деле и для утяжеления шелка. Шелковые ткани, обработанные перед Крашением растворами соединений олова, иногда содержат, до 50%(масс.) олова.
- 508 -
Кислоты также растворяют ?-оловянную кислоту с образованием солей олова (IV). Например:
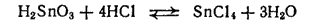
При избытке соляной кислоты хлорид олова(IV) присоединяет две молекулы хлороводорода, образуя комплексную гексахлоро-оловянную (или оловянохлористоводородную) кислоту H2[SnCl6]. Аммонийная соль этой кислоты (NH4)2[SnCl6] имеет то же применение, что и гидроксостаннат натрия.
?-Оловянная кислота получается в виде белого порошка при действии концентрированной азотной кислоты на олово (см. выше). Состав ее столь же неопределенен, как и состав ?-оловянной кислоты. В отличие от ?-оловянной кислоты, она не растворяется ни в кислотах, ни в растворах щелочей. Но путем сплавления со щелочами можно перевести ее в раствор в виде станната. ?-Оловянная кислота при хранении ее в соприкосновении с раствором, из которого она выделилась, постепенно тоже превращается в ?-оловянную кислоту.
Хлорид олова(IV) представляет собой жидкость, кипящую при 112°C и сильно дымящую на воздухе. Хлорид олова (IV) образуется при действии хлора на металлическое олово или на хлорид олова (II). В технике его получают главным образом путем обработки отбросов белой жести (старых консервных банок) хлором.
Хлорид олова (IV) растворяется в воде и может быть выделен из раствора в виде различных кристаллогидратов, например SnCl4·5H2O.
В водных растворах, особенно в разбавленных, хлорид олова (IV) подвергается гидролизу; конечным продуктом гидролиза является ?-оловянная кислота:
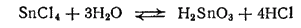
Гидрид олова SnH4 -бесцветный, очень ядовитый газ. Он сжижается при -52°C, а при комнатной температуре постепенно разлагается на олово и водород.
Сульфиды олова. При действии сероводорода на раствор хлорида олова(II) получается бурый осадок сульфида олова(II). Из раствора хлорида олова (IV) при тех же условиях выпадает желтый осадок дисульфида олова SnS2. Последнее соединение может быть получено также нагреванием оловянных опилок с серой и хлоридом аммония. Приготовленный по этому способу дисульфид имеет вид золотисто-желтых чешуек и под названием «сусального золота» употребляется для позолоты дерева.
Дисульфид олова растворяется в растворах сульфидов щелочных металлов и аммония, причем получаются легкорастворимые соли тиооловянной кислоты H2SnS3:
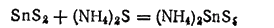
- 509 -
Свободная тиооловянная кислота не известна. При действии кислот на ее соли (тиостаннаты) выделяется сероводород и снова получается дисульфид олова:
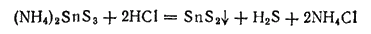
Сульфид олова (II) не растворяется в сульфидах щелочных металлов и аммония, но полисульфиды аммония и щелочных металлов растворяют его с образованием тиостаннатов:
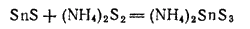
| <<< Назад 186. Германий (Germanium). |
Вперед >>> 188. Свинец (Plumbum). |
- 152. Углерод в природе.
- 153. Аллотропия углерода.
- 154. Химические свойства углерода. Карбиды.
- 155. Диоксид углерода. Угольная кислота.
- 156. Оксид углерода (II).
- 157. Соединения углерода с серой и азотом.
- 158. Топливо и его виды.
- 159. Газообразное топливо.
- 160. Общая характеристика органических соединений.
- 161. Отличительные особенности органических соединений.
- 162. Теория химического строения органических соединений.
- 163. Классификация органических соединений.
- 164. Предельные (насыщенные) углеводороды.
- 165. Непредельные (ненасыщенные) углеводороды.
- 166. Предельные циклические углеводороды.
- 167. Ароматические углеводороды.
- 168. Галогенпроизводные углеводородов.
- 169. Спирты и фенолы.
- 170. Простые эфиры.
- 171. Альдегиды и кетоны.
- 172. Карбоновые кислоты.
- 173. Сложные эфиры карбоновых кислот. Жиры.
- 174. Углеводы.
- 175. Амины.
- 176. Аминокислоты и белки.
- 177. Природные и синтетические высокомолекулярные соединения (полимеры).
- КРЕМНИЙ (SILICIUM) 178. Кремний в природе. Получение и свойства кремния.
- 179. Соединения кремния с водородом и галогенами.
- 180. Диоксид кремния.
- 181. Кремниевые кислоты и их соли.
- 182. Стекло.
- 183. Керамика.
- 184. Цемент.
- 185. Кремнийорганические соединения.
- 186. Германий (Germanium).
- 187. Олово (Stannuin).
- 188. Свинец (Plumbum).
- 189. Свинцовый аккумулятор.
- ГЕРМАНИЙ
- 189. Свинцовый аккумулятор.
- 186. Германий (Germanium).
- 168. Галогенпроизводные углеводородов.
- 176. Аминокислоты и белки.
- 188. Свинец (Plumbum).
- 160. Общая характеристика органических соединений.
- 180. Диоксид кремния.
- 166. Предельные циклические углеводороды.
- 170. Простые эфиры.
- Германий как он есть
- 185. Кремнийорганические соединения.
