Книга: Общая химия
165. Непредельные (ненасыщенные) углеводороды.
| <<< Назад 164. Предельные (насыщенные) углеводороды. |
Вперед >>> 166. Предельные циклические углеводороды. |
165. Непредельные (ненасыщенные) углеводороды.
Простейший непредельный углеводород с двойной связью — этилен C2H4 или CH2=CH2 , как уже указывалось, является родоначальником гомологического ряда непредельных этиленовых углеводородов:
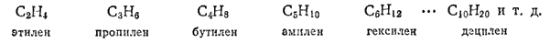
Состав любого углеводорода этого ряда выражает общая формула CnH2n (где n — число атомов углерода).
- 456 -
Состав членов гомологического ряда непредельных ацетиленовых углеводородов (с тройной связью), родоначальником которых является ацетилен C2H2, или CH?CH, выражается общей формулой CnH2n-2.
Общая формула CnH2n-2 выражает также состав углеводородов с двумя двойными связями* из них отметим бутадиен (или дивинил) C4H6 и изопрен C5H8 , имеющие следующее строение:

Известны углеводороды с большим числом двойных (полиены) или тройных (полиины) связей.
Непредельные углеводороды могут быть получены из предельных путем каталитического отщепления водорода (реакция дегидрирования, или дегидрогенизации). Например, из содержащегося в попутном нефтяном газе этана получают этилен, а из бутана — бутадиен:
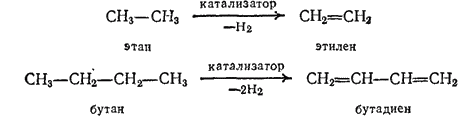
Изопрен может быть получен дегидрированием изопентана:

Важным источником получения этилена и его гомологов служат газообразные и жидкие продукты крекинга углеводородов нефти. Крекингом называют процесс расщепления углеводородов с длинными цепями на молекулы меньшей длины, происходящий в присутствии катализаторов (каталитический крекинг) или при нагревании предельных углеводородов до 500-700°C под давлением (термический крекинг). Например:
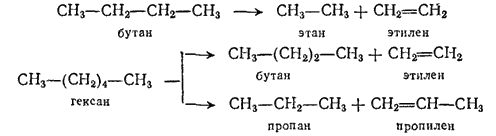
* См. примечание на стр. 455.
- 457 -
Крекинг нефтяных продуктов позволяет получать смеси низкокипящих углеводородов (например, бензин) из углеводородов с высокой температурой кипения. При крекинге наряду с предельными углеводородами всегда получаются и непредельные. Непредельные углеводороды, образующиеся при крекинге, а также полученные дегидрированием предельных углеводородов, содержащихся в попутных газах нефтедобычи, все шире используются в промышленности органического синтеза в качестве сырья для производства пластических масс, химических волокон, спиртов, каучукоподобных материалов, моющих средств, растворителей и других ценных продуктов.
Физические свойства этиленовых и ацетиленовых углеводородов в гомологических рядах изменяются с той же закономерностью, как и у предельных: низшие представители — газы, более сложные жидкости, а затем — вещества с постепенно возрастающими температурами плавления и кипения, находящиеся при обычных условиях в твердом состоянии.
По химическим свойствам непредельные углеводороды резко отличаются от предельных; они исключительно реакционноспособны и вступают в разнообразные реакции присоединения. Такие реакции происходят путем присоединения атомов или групп атомов к атомам углерода, связанным двойной или тройной связью. При этом кратные связи довольно легко разрываются и превращаются в простые.
Так, этилен и ацетилен легко присоединяют бром, переходя в соответствующие ди- и тетрагалогенпроизводные:
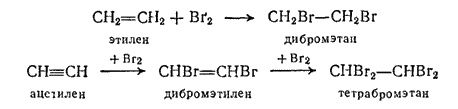
ацетилен дибромэтилен тетрабромэтан
Реакция может служить для обнаружения непредельных углеводородов — бурая окраска брома быстро исчезает.
Другой качественной реакцией на наличие кратных связей служит окисление перманганатом калия: непредельные соединения окисляются очень легко с разрывом кратных связей, а фиолетовая окраска KMnO4 при этом исчезает.
Важным свойством непредельных углеводородов является способность их молекул соединяться друг с другом или с молекулами других непредельных углеводородов (реакция полимеризации, § 177).
Этилен C2H4 бесцветный газ со слабым приятным запахом, довольно хорошо растворимый в воде. Его температура кипения -103,8°C, температура затвердевания -169,5°C. На воздухе он горит слегка светящимся пламенем.
- 458 -
Этилен — весьма важное сырье для получения ряда синтетических продуктов, особенно этилового спирта, этиленоксида (окиси этилена), этиленгликоля (антифриз), полиэтилена (см. § 177) и др.
Ацетилен C2H2 бесцветный газ с характерным слабым запахом; температура кипения -83,8°C, температура затвердевания — -80,8°C. Технический ацетилен, получаемый из карбида кальция, пахнет неприятно из-за имеющихся в нем примесей. На воздухе ацетилен горит сильно коптящим пламенем. При его сгорании выделяется большое количество теплоты. Поэтому ацетилен в смеси с кислородом широко используют для сварки и резки металлов (автогенная сварка; температура пламени до 3350°C). Взрывоопасен; смеси с воздухом, содержащие от 2,3 до 80,7% ацетилена, взрывают от искры. Трудно растворим в воде; под небольшим давлением (1,2-1,5 МПа) хорошо растворяется в ацетоне (до 300 объемов) и в таком виде безопасен.
Действие воды на карбид кальция CaC2 до сих пор остается одним из распространенных способов получения ацетилена:
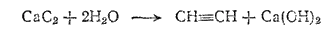
Новый, современный метод получения ацетилена заключается в пиролизе (превращение при высоких температурах) углеводородов, главным образом метана:
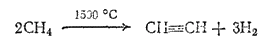
Ацетилен, подобно этилену, — ценное химическое сырье. Из него получают уксусный альдегид, этиловый спирт, уксусную кислоту, синтетические каучуки, пластические массы и другие продукты.
В области непредельных, а особенно ацетиленовых углеводородов большое значение имеют исследования, проведенные А. Е. Фаворским (1860—1945) и его учениками. Фаворский открыл большое число различных перегруппировок молекул при химических реакциях и показал, как можно управлять этими процессами.
| <<< Назад 164. Предельные (насыщенные) углеводороды. |
Вперед >>> 166. Предельные циклические углеводороды. |
- 152. Углерод в природе.
- 153. Аллотропия углерода.
- 154. Химические свойства углерода. Карбиды.
- 155. Диоксид углерода. Угольная кислота.
- 156. Оксид углерода (II).
- 157. Соединения углерода с серой и азотом.
- 158. Топливо и его виды.
- 159. Газообразное топливо.
- 160. Общая характеристика органических соединений.
- 161. Отличительные особенности органических соединений.
- 162. Теория химического строения органических соединений.
- 163. Классификация органических соединений.
- 164. Предельные (насыщенные) углеводороды.
- 165. Непредельные (ненасыщенные) углеводороды.
- 166. Предельные циклические углеводороды.
- 167. Ароматические углеводороды.
- 168. Галогенпроизводные углеводородов.
- 169. Спирты и фенолы.
- 170. Простые эфиры.
- 171. Альдегиды и кетоны.
- 172. Карбоновые кислоты.
- 173. Сложные эфиры карбоновых кислот. Жиры.
- 174. Углеводы.
- 175. Амины.
- 176. Аминокислоты и белки.
- 177. Природные и синтетические высокомолекулярные соединения (полимеры).
- КРЕМНИЙ (SILICIUM) 178. Кремний в природе. Получение и свойства кремния.
- 179. Соединения кремния с водородом и галогенами.
- 180. Диоксид кремния.
- 181. Кремниевые кислоты и их соли.
- 182. Стекло.
- 183. Керамика.
- 184. Цемент.
- 185. Кремнийорганические соединения.
- 186. Германий (Germanium).
- 187. Олово (Stannuin).
- 188. Свинец (Plumbum).
- 189. Свинцовый аккумулятор.
