Книга: Общая химия
131. Получение и применение серной кислоты.
| <<< Назад 130. Триоксид серы. Серная кислота. |
Вперед >>> 132. Пероксодвусерная кислота. |
131. Получение и применение серной кислоты.
В промышленности серная кислота получается окислением диоксида серы SO2 до триоксида с последующим взаимодействием SO3 с водой.
Необходимый для производства кислоты диоксид серы получают в технике различными способами. Наиболее распространенным из них является обжиг железного колчедана при доступе воздуха (см. § 129).
В СССР вместо пирита обжигу преимущественно подвергают флотационный колчедан — продукт флотации (см. § 192) медных руд с низким содержанием меди — и углистый колчедан, получаемый при обогащении каменных углей с высоким содержанием серы.
- 378 -
Образующийся при обжиге колчедана оксид железа(III) («колчеданный огарок») удаляется из печей и может быть, использован для получения железа, а смесь диоксида серы с кислородом и азотом воздуха пропускается через очистительные аппараты, в которых она освобождается от пыли и других примесей.
Диоксид серы получают также сжиганием серы. В этом случае образуется газ, свободный от вредных примесей; поэтому отпадает необходимость в очистительных аппаратах, что значительно упрощает производство серной кислоты.
Важным источником получения диоксида серы служат отходящие газы заводов цветной металлургии. Значение этого источника видно хотя бы из того, что при выплавке 1 т меди образуется 7,5 т SO2, из которого можно получить более 10 т серной кислоты.
Большое количество SO2 извлекают из топочных газов, особенно получаемых при сжигании каменного угля, содержащего много серы.
Сырьем для получения SO2 служит также гипс CaSO4·2H2O и ангидрит CaSO4. Эти минералы при 1350-1400°C разлагаются с образованием SO2:
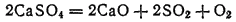
Если прокаливать гипс, смешанный в необходимой пропорции с оксидом железа(III) Fe2O3 , оксидом алюминия Al2O3 и кремнеземом SiO2, то одновременно с диоксидом серы получается цемент.
При получении серной кислоты SO2 окисляют двумя методами: контактным и нитрозным.
Контактный метод основан на присоединении кислорода к диоксиду серы при соприкосновении (контакте) этих газов с катализатором. Обязательным условием успешного протекания процесса является полное удаление примесей из реакционных газов, так как даже ничтожные следы некоторых веществ (соединений мышьяка, фосфора и др.) «отравляют» катализатор, вызывая быструю потерю им своей активности.
В качестве катализатора для окисления SO2 применяют ванадиевый ангидрид V2O5.
При получении серной кислоты контактным методом смесь диоксида серы и воздуха после освобождения от примесей проходит через подогреватель, обогреваемый выходящими из контактного аппарата газами, и поступает в контактный аппарат. На катализаторе происходит окисление SO2 в SO3 , сопровождающееся выделением значительного количества теплоты:
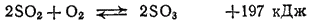
Увеличение содержания кислорода в смеси повышает выход SO3, смещая равновесие вправо. При 450°C и избытке кислорода степень превращения SO2 в SO3 достигает 95-97%.
Образовавшийся в контактном аппарате триоксид серы пропускают в 96—98 %-ную серную кислоту, которая, насыщаясь SO3, превращается в олеум.
В России производство серной кислоты по контактному методу впервые было осуществлено на Тентелевском заводе (ныне завод «Красный химик») в Петербурге.
- 379 -
Разработанная химиками этого завода «тентелевская система» была одной из самых совершенных систем своего времени и получила мировую известность. По этой системе были построены контактные установки в ряде стран, в том числе в Японии и США.
Нитрозный метод. Контактный метод получения серной кислоты стал применяться сравнительно недавно. До этого серную кислоту получали исключительно нитрозным методом, сущность которого заключается в окислении диоксида серы диоксидом азота NO2 в присутствии воды.
Газообразный диоксид азота реагирует с диоксидом серы согласно уравнению:

Отдавая диоксиду серы часть кислорода, NO2 превращается в другой газ — оксид NO. Последний взаимодействует с кислородом воздуха, в результате чего вновь образуется диоксид азота
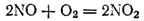
который идет на окисление новых порций SO2.
Таким образом, при производстве серной кислоты NO служит по существу катализатором, ускоряющим процесс окисления диоксида серы.
Промышленность выпускает несколько сортов серной кислоты. Они различаются между собою концентрацией, а также содержанием примесей. Большая часть производимой кислоты имеет плотность 1,825-1,84 г/см3, что соответствует массовой доле H2SO4 от 91 до 94%.
Серная кислота — один из важнейших продуктов основной химической промышленности; к последней относится производство кислот, щелочей, солей, минеральных удобрений и хлора. Основным потребителем серной кислоты является производство минеральных удобрений. Она служит также для получения многих других кислот, применяется в большом количестве в органическом синтезе, при производстве взрывчатых веществ, для очистки керосина, нефтяных масел и продуктов коксохимической промышленности (бензола, толуола), при изготовлении красок, травлении черных металлов (снятие окалины).
До Октябрьской революции производство серной кислоты в России было ничтожным по сравнению с производством ее в других странах. Продукция всех заводов составляла в 1913 г всего около 145 тыс. т.
После революции положение резко изменилось. Старые заводы были расширены и заново переоборудованы. Была создана отечественная сырьевая база для сернокислотной промышленности и построен ряд новых заводов. Это позволило значительно увеличить производство серной кислоты;

- 380 -
| <<< Назад 130. Триоксид серы. Серная кислота. |
Вперед >>> 132. Пероксодвусерная кислота. |
- КИСЛОРОД (OXYGENIUM) 123. Кислород в природе. Воздух.
- 124. Получение и свойства кислорода.
- 125. Озон.
- 126. Сера в природе. Получение серы.
- 127. Свойства и применение серы.
- 128. Сероводород. Сульфиды.
- 129. Диоксид серы. Сернистая кислота.
- 130. Триоксид серы. Серная кислота.
- 131. Получение и применение серной кислоты.
- 132. Пероксодвусерная кислота.
- 133. Тиосерная кислота.
- 134. Соединения серы с галогенами.
- 135. Селен (Selenium). Теллур (Tellurium).
- Применение солей.
- Бактерии, вырабатывающие аминокислоты
- Применение бамбука
- Глава 6. Самое главное применение
- 9. Органические вещества. Нуклеиновые кислоты
- 2.3.4.Нуклеиновые кислоты
- § 53 Соли и их применение
- § 52 Строение и свойства неорганических веществ. Кислоты и основания
- Сложные неорганические вещества: кислоты и основания.
- Получение и использование синтетических полимеров
- 2.6. Органические вещества. Нуклеиновые кислоты
- Органические кислоты
