Книга: Книга по химии для домашнего чтения
3.5. СИСТЕМА СИМВОЛОВ БЕРЦЕЛИУСА
| <<< Назад 3.4. ХИМИЧЕСКИЕ ЗАПИСИ ПЕТРА I |
Вперед >>> 3.6. СОЛИ ТАХЕНИЯ |
Разделы на этой странице:
3.5. СИСТЕМА СИМВОЛОВ БЕРЦЕЛИУСА
Торнберн-Улаф Бергман (1735–1784) — шведский химик и минералог, член Шведской королевской академии наук — советовал в последние годы своей жизни французскому химику Гитону де Морво, инициатору создания первой номенклатуры химических веществ: «Не щадите ни одного неправильного наименования, знающие поймут всегда, незнающие поймут тем скорее».
Шведский химик Берцелиус (см. 2.19) использовал этот совет для разработки своей системы химических символов, которая сохранилась и в современной химии. Он предложил в качестве символов химических элементов принимать первую букву их латинских названий, а в случае совпадения первых букв — использовать и вторую букву. Так, для обозначения кислорода он взял символ «О» — первую букву от Oxygenium (оксигениум), для водорода — «Н» — от Hydrogenium (гидрогениум), для углерода — «С» — от Carboneum (карбонеум). Символ химического элемента кальция «Ca» уже содержит две первые буквы слова Calcium (кальциум) — во избежание совпадения с символом углерода. Две буквы нужны и для символа химического элемента меди: «Cu» от Cuprum (купрум) — по той же причине.
Если же кислород входит в состав сложного вещества, то Берцелиус рекомендовал пользоваться точками над символом элемента.
Например, ?a — оксид кальция CaO;
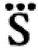
— серная кислота H2SO4;

— азотная кислота с формулой HNO3. Если в составе вещества два атома одинакового вида, Берцелиус предлагал ставить поперечную черту на расстоянии 1/3 от нижней части символа:
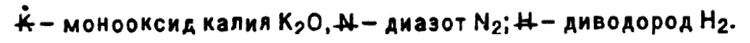
Реакция получения аммиака NH3 взаимодействием хлорида аммония NH4Cl и оксида кальция CaO по Берцелиусу записывалась так:
NH4Cl + ?a = CaCl + ? + NH3
Современная запись этой реакции:
2NH4Cl + CaO = CaCl2 + H2O + 2NH3.
Уже после Берцелиуса число атомов в соединениях стали указывать цифрами справа вверху символа химического элемента. Например, K2SO4 — сульфат калия, NH3 — аммиак, Al2O3 — оксид алюминия. Надстрочные индексы в формулах соединений сохранились до конца XIX в. и использовались Менделеевым во всех восьми изданиях его знаменитого учебника «Основы химии». Принятое в настоящее время указание числа атомов в молекулах соединений подстрочной цифрой (K2SO4, NH3) было предложено еще в 1834 г. Либихом (см. 2.17).
| <<< Назад 3.4. ХИМИЧЕСКИЕ ЗАПИСИ ПЕТРА I |
Вперед >>> 3.6. СОЛИ ТАХЕНИЯ |
- 3.1. МИСТИЧЕСКОЕ ЧИСЛО СЕМЬ. АЛХИМИЧЕСКИЕ СИМВОЛЫ: «КРАСНЫЙ ЛЕВ» И «ПРЕКРАСНАЯ ЛИЛИЯ»
- 3.2. ПЕРВЫЕ УСЛОВНЫЕ ОБОЗНАЧЕНИЯ ВЕЩЕСТВ
- 3.3. «СПИРИТУС НИТРИ» РАСТВОРЯЕТ «ВЕНЕРУ», «МАРС» И «ЛУНУ». ЧТО ЭТО ЗНАЧИТ?
- 3.4. ХИМИЧЕСКИЕ ЗАПИСИ ПЕТРА I
- 3.5. СИСТЕМА СИМВОЛОВ БЕРЦЕЛИУСА
- 3.6. СОЛИ ТАХЕНИЯ
- 3.7. ХИМИЯ БЕЗ ФОРМУЛ
- 3.8. ИМЕНА КИСЛОТ
- 3.9. ГЕОМЕТРИЧЕСКИЕ ФИГУРЫ И ХИМИЧЕСКИЕ СИМВОЛЫ
- 3.10. СТРАННЫЕ СПИРТЫ
- 3.11. «МАГИЧЕСКИЕ», «ЖЕСТКИЕ», «МЯГКИЕ», «СВЕРХКИСЛОТЫ», «КИСЛОТЫ ЛЬЮИСА», «КИСЛОТЫ БРЁНСТЕДА» — ЧТО ЭТО ТАКОЕ?
- 3.12. «СОЛЕНЫЙ СПИРТ»
- 3.13. «КОРОЛЕВСКАЯ ВОДКА»
- 3.14. СТРАННАЯ ФОРМУЛА
- 3.15. ГАС ГЕЛЬМОНТА
- 3.16. ВОДОРОД ХЛОРОВИЧ…
- 3.17. «СЕРНОКИСЕНЬ»
- 3.18. «МЕДНЫЙ ИДРАТ»
- 3.19. «КУПОРОС ЗЕЛЕНЫЙ»
- 3.20. И СНОВА «ЯМЧУГ»…
- 3.21. ШАРАДЫ В РУКОПИСИ ЛОМОНОСОВА
- 3.22. ЕЩЕ РАЗ О НАЗВАНИЯХ ВЕЩЕСТВ
- 3.23. РАЗНЫЕ ИЗВЕСТИ
- 3.24. НЕОЖИДАННЫЙ ВЗРЫВ
- 3.25. «СУСАЛЬНОЕ ЗОЛОТО»
- 3.26. «ГРЕМУЧЕЕ СЕРЕБРО»
- 3.27. БЫВАЮТ ЛИ КИСЛОТЫ ЖИРНЫМИ?
- 3.28. КАК ПОЯВИЛОСЬ НАЗВАНИЕ «ЛИМОННАЯ КИСЛОТА»
- 3.29. КИСЛОТЫ ИЗ ЯНТАРЯ И МОЛОКА
- 3.30. ЕСТЬ ЛИ В ЯБЛОКАХ ЯБЛОЧНАЯ КИСЛОТА, А В ВИНЕ — ВИННАЯ?
- 3.31. ОТЧЕГО УКУСЫ МУРАВЬЕВ ТАК БОЛЕЗНЕННЫ? ЕДИМ ЛИ МЫ ЩАВЕЛЕВУЮ КИСЛОТУ!
- 3.32. «ДРЕВЕСНАЯ КИСЛОТА». «КРИМИНАЛЬНОЕ» ПРОИСХОЖДЕНИЕ БЕНЗОЛЬНОГО КОЛЬЦА
- 3.33. ЧТО ОЗНАЧАЕТ НАЗВАНИЕ «РОДАНИДЫ»?
- 3.34. ЧТО ТАКОЕ «ТЕНАРОВА СИНЬ»?
- 3.35. ГЛАУБЕРОВА СОЛЬ
- 3.36. «СЕНЬЕТОВА СОЛЬ»
- 3.37. «КРОВЯНЫЕ СОЛИ»
- 3.38. «ПРЕЦИПИТАТЫ»
- 3.39. «АЛКАЛЬ»
- 3.40. КАКАЯ РАЗНИЦА МЕЖДУ АНГИДРИДОМ, АНГИДРИТОМ И АНГИДРОНОМ?
- 3.41. ЧЕМ СХОДНЫ И ЧЕМ РАЗЛИЧАЮТСЯ СИЛАН И СЕЛАН?
- 3.42. МОЖЕТ ЛИ ЗОЛОТО БЫТЬ ЧЕРВОННЫМ?
- 3.43. КАКОЕ ОТНОШЕНИЕ К ТЕРМИТАМ ИМЕЕТ ТЕРМИТНАЯ СМЕСЬ?
- 3.44. БЕЛАЯ И ЧЕРНАЯ…
- 3.45. ЕСТЬ ЛИ ЦЕМЕНТ В ЦЕМЕНТИТЕ?
- 3.46. УЧАСТВУЕТ ЛИ ЦЕМЕНТ В ЦЕМЕНТАЦИИ?
- 3.47. ВСЯКОЕ ЛИ МАСЛО ПРИГОДНО ДЛЯ СМАЗКИ?
- 3.48. МОЖНО ЛИ ПОЛУЧИТЬ «БАРИТОВУЮ ВОДУ», РАСТВОРЯЯ БАРИТ В ВОДЕ?
- 3.49. ПРАВДА ЛИ, ЧТО KETEH — СЫН КЕТОНА?
- 3.50. «ЗОЛОТАЯ» СОЛЬ
- 3.51. МАНГАНИН И МАНГАНAT
- 3.52. БОРАЗОН — ИЛИ БОРАЗИН — ИЛИ БОРАЗОЛ?
- 3.53. В ЧЕМ РАЗЛИЧИЕ МЕЖДУ ГИДРОКСИЛОМ И ГИДРОКСИДОМ?
- 3.54. НЕ ОШИБАЙТЕСЬ: СОЛИ РАЗНЫЕ!
- 3.55. «МУМИЯ» И «МУМИЁ»
- 3.56. «РЫБНЫЙ ГАЗ»
