Книга: Общая химия
76. Растворимость.
| <<< Назад 75. Гидраты и кристаллогидраты. |
Вперед >>> 77. Пересыщенные растворы. |
76. Растворимость.
Растворимостью называется способность вещества растворяться в том или ином растворителе. Мерой растворимости вещества при данных условиях служит содержание его в насыщенном растворе. Поэтому численно растворимость может быть выражена теми же способами, что и состав, например, процентным отношением массы растворенного вещества к массе насыщенного раствора или количеством растворенного вещества, содержащимся в 1 л насыщенного раствора. Часто растворимость выражают также числом единиц массы безводного вещества, насыщающего при данных условиях 100 единиц массы растворителя; иногда выраженную этим способом растворимость называют коэффициентом растворимости.
Растворимость различных веществ в воде изменяется в широких пределах. Если в 100 г. воды растворяется более 10 г. вещества, то такое вещество принято называть хорошо растворимым; если растворяется менее 1 г. вещества — малорастворимым и, наконец, практически нерастворимым, если в раствор переходит менее 0,01 г. вещества.
Принципы, позволяющие предсказать растворимость вещества, пока не известны. Однако обычно вещества, состоящие из полярных молекул, и вещества с ионным типом связи лучше растворяются в полярных растворителях (вода, спирты, жидкий аммиак), а неполярные вещества — в неполярных растворителях (бензол, сероуглерод).
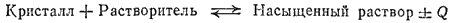
Рис. 75. Зависимость растворимости некоторых солей в воде от температуры.
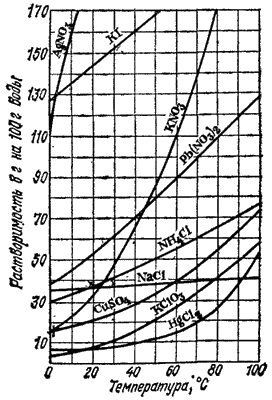
Рис. 76. Зависимость растворимости сульфата натрия в воде от температуры.
Растворение большинства твердых тел сопровождается поглощением теплоты. Это объясняется затратой значительного количества энергии на разрушение кристаллической решетки твердого тела, что обычно не полностью компенсируется энергией, выделяющейся при образовании гидратов (сольватов). Прилагая принцип Ле Шателье к равновесию между веществом в кристаллическом состоянии и его насыщенным раствором
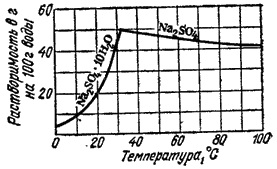
приходим к выводу, что в тех случаях, когда вещество растворяется с поглощением энергии, повышение температуры должно приводить к увеличению его растворимости. Если же, однако, энергия гидратации (сольватации) достаточно велика, чтобы образование раствора сопровождалось выделением энергии, растворимость с ростом температуры понижается. Это происходит, например, при растворении в воде щелочей, многих солей лития, магния, алюминия.
Зависимость между растворимостью и температурой очень удобно изображать графически — в виде кривых растворимости. Для построения кривой растворимости откладывают на горизонтальной оси температуру, а на вертикальной — растворимость вещества при соответствующей температуре.
На рис. 75 приведено несколько характерных кривых растворимости. Резко поднимающиеся вверх кривые растворимости нитратов калия, свинца, серебра показывают, что с повышением температуры растворимость этих веществ сильно возрастает. Растворимость хлорида натрия лишь незначительно изменяется по мере повышения температуры, что показывает почти горизонтальная кривая растворимости этой соли. Более сложный вид имеет кривая растворимости сульфата натрия (рис. 76).
- 212 -
До 32? эта кривая круто поднимается, что указывает на быстрое увеличение растворимости. При 32 ? происходит резкий излом кривой, после чего она идет несколько вниз. Следовательно, сульфат натрия обладает наибольшей растворимостью при 32?. Наличие максимума на кривой растворимости сульфата натрия объясняется тем, что ниже 32? в равновесии с насыщенным раствором находится кристаллогидрат Na2SO4·10H2O, растворение которого сопровождается поглощением теплоты; но при более высоких температурах твердая фаза, находящаяся в равновесии с насыщенным раствором, представляет собой безводную соль Na2SO4, растворяющуюся с выделением теплоты.
При растворении твердых тел в воде объем системы обычно изменяется незначительно. Поэтому растворимость веществ, находящихся в твердом состоянии, практически не зависит от давления.
Жидкости также могут растворяться в жидкостях. Некоторые из них неограниченно растворимы одна в другой, т. е. смешиваются друг с другом в любых пропорциях, как, например, спирт и вода, другие — взаимно растворяются лишь до известного предела. Так, если взболтать диэтиловый эфир с водой, то образуются два слоя: верхний представляет собой насыщенный раствор воды в эфире, а нижний — насыщенный раствор эфира в воде. В большинстве подобных случаев с повышением температуры взаимная растворимость жидкостей увеличивается до тех пор, пока не будет достигнута температура, при которой обе жидкости смешиваются в любых пропорциях.
Температура, при которой ограниченная взаимная растворимость жидкостей переходит в неограниченную, называется критической температурой растворения. Так, при температуре ниже 66.4? фенол ограниченно растворим в воде, а вода ограниченно растворима в феноле. Температура 66.4? — критическая температура растворения для системы вода — фенол: начиная с этой температуры, обе жидкости неограниченно растворимы друг в друге.
Как и в случае растворения твердых тел, взаимное растворение жидкостей обычно не сопровождается значительным изменением объема. Поэтому взаимная растворимость жидкостей мало зависит от давления и заметно возрастает лишь при очень высоких давлениях (порядка тысяч атмосфер).
Если в систему, состоящую из двух не смешивающихся жидкостей, ввести третье вещество, способное растворяться в каждой из этих жидкостей, то растворенное вещество будет распределяться между обеими жидкостями пропорционально своей растворимости в каждой из них. Отсюда вытекает закон распределения, согласно которому вещество, способное растворяться в двух несмешивающихся растворителях, распределяется между ними так, что отношение его концентраций в этих растворителях при постоянной температуре остается постоянным, независимо от общего количества растворенного вещества:
C1/C2=K
Здесь C1 и C2 — концентрации растворенного вещества в первом и втором растворителях; К — так называемый коэффициент распределения.
Так, коэффициент распределения иода между водой и хлороформом равен 130. Если к воде, содержащей растворенный иод, добавить не смешивающийся с нею хлороформ, взболтать эту систему и дать ей отстояться, то после установления равновесия концентрация иода в хлороформе окажется в 130 раз более высокой, чем в воде, независимо от общего количества растворенного иода. Таким образом с помощью хлороформа можно извлечь (экстрагировать) из воды преобладающую часть растворенного в ней иода. Такой, основанный на законе распределения способ извлечения растворенного вещества из раствора с помощью второго растворителя, не смешивающегося с первым, называется экстракцией и широко применяется в лабораторной практике и в химической промышленности.
Растворение газов в воде представляет собой экзотермический процесс. Поэтому растворимость газов с повышением температуры уменьшается. Если оставить в теплом помещении стакан с холодной водой, то внутренние стенки его покрываются пузырьками газа — это воздух, который был растворен в воде, выделяется из нее вследствие нагревания. Кипячением можно удалить из воды весь растворенный в ней воздух.
Однако растворение газов в органических жидкостях нередко сопровождается поглощением теплоты; в подобных случаях с ростом температуры растворимость газа увеличивается.
При растворении газа в жидкости устанавливается равновесие:
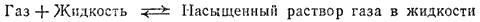
При этом объем системы существенно уменьшается. Следовательно, повышение давления должно приводить к смещению равновесия вправо, т. е. к увеличению растворимости газа.
К этому же выводу можно прийти, исходя из динамического характера равновесия между газом и его раствором в жидкости. Молекулы газа, находящиеся над жидкостью в закрытом сосуде, бомбардируют поверхность жидкости и растворяются в жидкости со скоростью, пропорциональной концентрации газа. Перешедшие в раствор молекулы в свою очередь время от времени ударяются о поверхность жидкости изнутри и вылетают наружу. По мере того как в результате растворения концентрация растворенных молекул будет увеличиваться, скорость их выделения, т. е. число молекул, уходящих из раствора в единицу времени, тоже будет расти, пока, наконец, не сравняется со скоростью растворения.
В результате установится состояние равновесия, т. е. жидкость станет насыщенной газом.
Если теперь увеличить давление газа, например, в 2 раза, то во столько же раз увеличится и концентрация его молекул над жидкостью, а следовательно, и скорость растворения газа. Равновесие нарушится. Чтобы при новом давлении снова установилось равновесие, концентрация растворенных молекул, очевидно, тоже должна увеличиться вдвое.
Таким образом, приходим к выводу, который известен под названием закона Генри:
Масса газа, растворяющегося при постоянной температуре в данном объеме жидкости, прямо пропорциональна парциальному давлению газа.
Закон Генри может быть выражен уравнением
C = kp
где С — массовая концентрация газа в насыщенном растворе; p — парциальное давление; k — коэффициент пропорциональности, называемый константой Генри (или коэффициентом Генри).
Отметим важное следствие закона Генри. Пусть при данном давлении в некотором объеме жидкости растворяется один объем газа, содержащий m г этого газа. Не меняя температуры, увеличим давление в n раз. При этом, согласно закону Бойля — Мариотта, объем, занимаемый газом, уменьшится в n раз; следовательно, масса газа, содержащегося в единице объема, возрастет в n раз и составит nm г. С другой стороны, в соответствии с законом Генри масса газа, растворяющегося в определенном объеме жидкости, также возрастет в n раз, т. е. также станет равна nm г. Иначе говоря, в данном объеме жидкости по-прежнему будет растворяться один объем газа.
Следовательно, объем газа, растворяющегося при постоянной температуре в данном объеме жидкости, не зависит от его парциального давления. Именно поэтому растворимость газов обычно выражают не в граммах, а в миллилитрах, указывая объем газа, растворяющийся в 100 мл растворителя.
Растворимость некоторых газов в воде при 0 и при 20? приведена в табл. 10.
Если над жидкостью находится смесь нескольких газов, то растворимость каждого из них определяется его парциальным давлением. Это необходимо учитывать при расчете растворимости газов, находящихся в смеси с другими газами.
Газы подчиняются закону Генри при не очень высоких давлениях и притом лишь в случае, когда они не вступают в химическое взаимодействие с растворителем.
Таблица 10. Растворимость газов в воде

При высоких давлениях, когда поведение всех газов заметно отличается от идеального, отклонение от закона Генри наблюдается и в случае газов, химически не взаимодействующих с растворителем.
| <<< Назад 75. Гидраты и кристаллогидраты. |
Вперед >>> 77. Пересыщенные растворы. |
- 69. Вода в природе.
- 70. Физические свойства воды.
- 71. Диаграмма состояния воды.
- 72. Химические свойства воды.
- 73. Характеристика растворов. Процесс растворения.
- 74. Способы выражения состава растворов.
- 75. Гидраты и кристаллогидраты.
- 76. Растворимость.
- 77. Пересыщенные растворы.
- 78. Осмос.
- 79. Давление пара растворов.
- 80. Замерзание и кипение растворов.
- Среда жизни
- Как смешиваются вкусы
- Тайна «озер-убийц»
- Белые «перья» Багам
- Глава VII. ВОДА, РАСТВОРЫ
- Источники газов при формировании планет
- 194. Сплавы.
- 89. Произведение растворимости.
- Между аргоном и гелием
- 74. Способы выражения состава растворов.
- 75. Гидраты и кристаллогидраты.
- 79. Давление пара растворов.
