Книга: Общая химия
72. Химические свойства воды.
| <<< Назад 71. Диаграмма состояния воды. |
Вперед >>> 73. Характеристика растворов. Процесс растворения. |
72. Химические свойства воды.
Молекулы воды отличаются большой устойчивостью к нагреванию. Однако при температурах выше 1000°C водяной пар начинает разлагаться на водород и кислород:
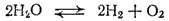
Процесс разложения вещества в результате его нагревания называется термической диссоциацией. Термическая диссоциация воды протекает с поглощением теплоты. Поэтому, согласно принципу Ле Шателье, чем выше температура, тем в большей степени разлагается вода. Однако даже при 2000°C степень термической диссоциации воды не превышает 2%, т. е. равновесие между газообразной водой и продуктами ее диссоциации — водородом и кислородом — все еще остается сдвинутым в сторону воды. При охлаждении же ниже 1000°C равновесие практически полностью сдвигается в этом направлении.
Для определения степени термической диссоциации вещества применяют различные методы. Один из них основан на так называемом «замораживании равновесия». Если образовавшиеся при высокой температуре продукты диссоциации быстро охладить, то равновесие не успевает сразу сместиться, а затем уже не смещается ввиду крайне малой скорости реакции при низкой температуре. Таким образом сохраняется соотношение между веществами, существовавшее при высокой температуре.
- 204 -
Это соотношение может быть определено путем анализа.
Вода — весьма реакционноспособное вещество. Оксиды многих металлов и неметаллов соединяются с водой, образуя основания и кислоты; некоторые соли образуют с водой кристаллогидраты (см. § 75); наиболее активные металлы взаимодействуют с водой с выделением водорода.
Вода обладает также каталитической способностью. В отсутствие следов влаги практически не протекают некоторые обычные реакции; например, хлор не взаимодействует с металлами, фторо-водород не разъедает стекло, натрий не окисляется в атмосфере воздуха.
Вода способна соединяться с рядом веществ, находящихся при обычных условиях в газообразном состоянии, образуя при этом так называемые гидраты газов. Примерами могут служить соединения Xe·6H2O, Cl2·8H2O, C2H6·6H2O, C2H8·17H2O, которые выпадают в виде кристаллов при температурах от 0 до 24°C (обычно при повышенном давлении соответствующего газа). Подобные соединения возникают в результате заполнения молекулами газа («гостя») межмолекулярных полостей, имеющихся в структуре воды (хозяина); они называются соединениями включения или клатратами.
В клатратных соединениях между молекулами «гостя» и «хозяина» образуются лишь слабые межмолекулярные связи: включенная молекула не может покинуть своего места в полости кристалла преимущественно из-за пространственных затруднений. Поэтому клатраты — неустойчивые соединения, которые могут существовать лишь при сравнительно низких температурах.
Клатраты используют для разделения углеводородов и благородных газов. В последнее время образование и разрушение клатратов газов (пропана и некоторых других) успешно применяется для обессоливания воды. Нагнетая в соленую воду при повышенном давлении соответствующий газ, получают льдоподобные кристаллы клатратов, а соли остаются в растворе. Похожую на снег массу кристаллов отделяют от маточного раствора и промывают. Затем при некотором повышении температуры или уменьшении давления клатраты разлагаются, образуя пресную воду и исходный газ, который вновь используется для получения клатрата. Высокая экономичность и сравнительно мягкие условия осуществления этого процесса делают его перспективным в качестве промышленного метода опреснения морской воды.
Тяжелая вода. При электролизе обычной воды, содержащей наряду с молекулами H2O также незначительное количество молекул D2O, образованных тяжелым изотопом водорода, разложению подвергаются преимущественно молекулы H2O. Поэтому при длительном электролизе воды остаток постепенно обогащается молекулами D2O. Из такого остатка после многократного повторения электролиза в 1933 г. впервые удалось выделить небольшое количество воды, состоящей почти на 100% из молекул D2O и получившей название тяжелой воды.
- 205 -
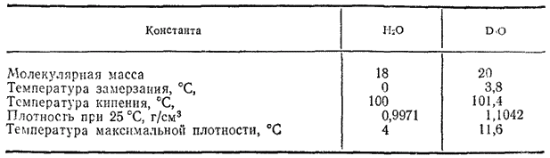
По своим свойствам тяжелая вода заметно отличается от обычной воды (табл. 9). Реакшт с тяжелой водой протекают медленнее, чем с обычной. Тяжелую воду применяют в качестве замедлителя нейтронов в ядерных реакторах.
Таблица 9. Некоторые константы обычной и тяжелой воды
Растворы имеют важное значение в жизни и практической деятельности человека. Так, процессы усвоения пищи человеком я животными связаны с переводом питательных веществ в раствор. Растворами являются все важнейшие физиологические жидкости (кровь, лимфа и т. д.). Производства, в основе которых лежат химические процессы, обычно связаны с использованием растворов.
| <<< Назад 71. Диаграмма состояния воды. |
Вперед >>> 73. Характеристика растворов. Процесс растворения. |
- 69. Вода в природе.
- 70. Физические свойства воды.
- 71. Диаграмма состояния воды.
- 72. Химические свойства воды.
- 73. Характеристика растворов. Процесс растворения.
- 74. Способы выражения состава растворов.
- 75. Гидраты и кристаллогидраты.
- 76. Растворимость.
- 77. Пересыщенные растворы.
- 78. Осмос.
- 79. Давление пара растворов.
- 80. Замерзание и кипение растворов.
- 1. Морфология и культуральные свойства
- Химические элементы и вещества
- § 50 Химические реакции
- 427. Какие химические элементы содержатся в морской воде в наибольших количествах?
- Глава 8 Биогенная миграция химических элементов и биогеохимические принципы
- 682. Как химические питательные вещества преобразуются в пищу?
- 8.2. Биогеохимические принципы
- 909. Каковы основные химические загрязнители?
- 429. Как различные химические элементы попали в морскую воду?
- § 14. Химические явления. Горение
- 182. Каковы важнейшие физико-химические свойства воды?
- Глава 7 Биогеохимические процессы и продукционные циклы
