Книга: Общая химия
39. Ковалентная связь. Метод валентных связей.
| <<< Назад 38. Теория химического строения. |
Вперед >>> 40. Неполярная и полярная ковалентная связь. |
39. Ковалентная связь. Метод валентных связей.
Мы уже знаем, что устойчивая молекула может образоваться только при условии уменьшения потенциальной энергии системы взаимодействующих атомов. Для описания состояния электронов в молекуле следовало бы составить уравнение Шредингера для соответствующей системы электронов и атомных ядер и найти его решение, отвечающее минимальной энергии системы. Но, как указывалось в § 31, для многоэлектронных систем точное решение уравнения Шредингера получить не удалось. Поэтому квантово-механическое описание строения молекул получают, как и в случае многоэлектронных атомов, лишь на основе приближенных решений уравнения Шредингера.
Впервые подобный приближенный расчет был произведен в 1927 г. В. Гейтлером и Ф. Лондоном для молекулы водорода. Эти авторы сначала рассмотрели систему из двух атомов водорода, находящихся на большом расстоянии друг от друга.
- 114 -
При этом условии можно учитывать только взаимодействие каждого электрона со «своим» ядром, а всеми остальными взаимодействиями (взаимное отталкивание ядер, притяжение каждого электрона к «чужому» ядру, взаимодействие между электронами) можно пренебречь. Тогда оказывается возможным выразить зависимость волновой функции рассматриваемой системы от координат и тем самым определить плотность общего электронного облака в любой точке пространства. (Напомним, что плотность электронного облака пропорциональна квадрату волновой функции — см. § 26).
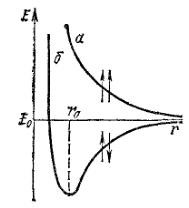
Рис. 26. Энергия системы, состоящей из двух атомов водорода:
а — при одинаково направленных спинах электронов; б — при противоположно направленных спинах; Е0 — энергия системы из двух невзаимодействующих атомов водорода; rc — межъядерное расстояние в молекуле водорода.
Далее Гейтлер и Лондон предположили, что найденная или зависимость волновой функции от координат сохраняется и при сближении атомов водорода. При этом, однако, необходимо уже учитывать и те взаимодействия (между ядрами, между электронами и т.д.) которыми при значительном удалении атомов друг от друга можно было пренебрегать. Эти дополнительные взаимодействия рассматриваются как некоторые поправки («возмущения») к исходному состоянию электронов в свободных атомах водорода.
В результате Гейтлер и Лондон получили уравнения, позволяющие найти зависимость потенциальной энергии Е системы, состоящей из двух атомов водорода, от расстояния r между ядрами этих атомов. При этом оказалось, что результаты расчета зависят от того, одинаковы или противоположны по знаку спины взаимодействующих электронов. При совпадающем направлении спинов (рис. 26, кривая а) сближение атомов приводит к непрерывному возрастанию энергии системы. В этом случае для сближения атомов требуется затрата энергии, так что такой процесс оказывается энергетически невыгодным и химическая связь между атомами не возникает. При противоположно направленных спинах (рис. 26, кривая б) сближение атомов до некоторого расстояния r0 сопровождается уменьшением энергии системы. При r = r0 система обладает наименьшей потенциальной энергией, т.е. находится в наиболее устойчивом состоянии; дальнейшее сближение атомов вновь приводит к возрастанию энергии. Но это и означает, что в случае противоположно направленных спинов атомных электронов образуется молекула H2 — устойчивая система из двух атомов водорода, находящихся на определенном расстоянии друг от друга.
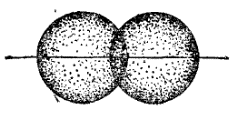
Рис. 27. Схема перекрывания атомных электронных облаков в молекуле водорода.
- 115 -
Образование химической связи между атомами водорода является результатом взаимопроникновения («перекрывания») электронных облаков, происходящего при сближении взаимодействующих атомов (рис. 27). Вследствие такого взаимопроникновения плотность отрицательного электрического заряда в межъядерном пространстве возрастает. Положительно заряженные ядра атомов притягиваются к области перекрывания электронных облаков, это притяжение преобладает над взаимным отталкиванием одноименно заряженных электронов, так что в результате образуется устойчивая молекула.
Полученные Гейтлером и Лондоном (и впоследствии уточненные другими исследователями) расчетные значения межъядерного расстояния и энергии связи в молекуле водорода оказались близки к экспериментально найденным значениям. Это означало, что приближения, использованные Гейтлером и Лондоном при решении уравнения Шредингера, не вносят существенных ошибок и могут считаться оправданными. Таким Образом, исследование Гейтлера и Лондона позволяло сделать вывод, что химическая связь в молекуле водорода осуществляется путем образования пары электронов с противоположно направленными спинами, принадлежащей обоим атомам. Процесс «спаривания» электронов при образовании молекулы водорода может быть изображен следующей схемой:
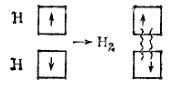
Волнистые линии на схеме показывают, что в молекуле водорода каждый электрон занимает место в квантовых ячейках обоих атомов, т.е. движется в силовом поле, образованном двумя силовыми центрами — ядрами атомов водорода.
Такая двухэлектронная двухцентровая связь называется ковалентной связью.
Представления о механизме образования химической связи, развитые Гейтлером и Лондоном на примере молекулы водорода, были распространены и на более сложные молекулы. Разработанная на этой основе теория химической связи получила название метода валентных связей (метод ВС). Метод ВС дал теоретическое объяснение важнейших свойств ковалентной связи, позволил понять строение большого числа молекул. Хотя, как мы увидим ниже, этот метод не оказался универсальным и в ряде случаев не в состоянии правильно описать структуру и свойства молекул (см. § 45), все же он сыграл большую роль в разработке квантово-механической теории химической связи и не потерял своего значения до настоящего времени.
- 116 -
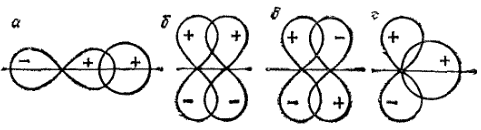
Рис. 28. Схема различных случаев перекрывания электронных облаков:
а и б — положительное перекрывание; в — отрицательное перекрывание; г — суммарное перекрывание, равное нулю.
В основе метода ВС лежат следующие положения:
1. Ковалентная химическая связь образуется двумя электронами с противоположно направленными спинами, причем эта электронная пара принадлежит двум атомам.
Комбинации таких двухэлектронных двухцентровых связей, отражающие электронную структуру молекулы, получили название валентных схем.
2. Ковалентная связь тем прочнее, чем в большей степени перекрываются взаимодействующие электронные облака.
При оценке степени перекрывания электронных облаков следует учитывать знаки волновых функций электронов. Поскольку электронам присущи волновые свойства, то при взаимодействии двух электронов образуется общая «электронная волна». Там, где амплитуды исходных волн имеют одинаковые знаки, при их сложении возникает суммарная волна с амплитудой, имеющей большее абсолютное значение, чем исходные амплитуды. Напротив, там, где амплитуды исходных волн имеют различные знаки, при их сложении возникает суммарная волна с амплитудой имеющей меньшее абсолютное значение, - волны будут «гасить» друг друга. Но, как уже указывалось, роль амплитуды электронной волны играет волновая функция ? (см. § 26). Поэтому в тех областях пространства, где волновые функции взаимодействующих электронов имеют одинаковые знаки, абсолютное значение волновой функции образующегося общего электронного облака будет больше, чем значения функции ? у изолированных атомов. При этом будет возрастать и величина ?2, т.е. плотность электронного облака. Здесь происходит положительное перекрывание электронных облаков, которое приводит к взаимному притяжению ядер. В тех же областях пространства, где знаки волновых функций взаимодействующих электронов противоположны, абсолютное значение суммарной волновой функции будет меньше, чем у изолированных атомов. Здесь величина ?2, а значит и плотность электронного облака, будет уменьшаться. В этом случае имеет место отрицательное перекрывание, приводящее к взаимному отталкиванию ядер.
Некоторые возможные варианты перекрывания электронных облаков с указанием знаков соответствующих волновых функций изображены на рис. 28.
Для наглядного изображения валентных схем обычно пользуются следующим способом. Электроны, находящиеся во внешнем электронном слое, обозначают точками, располагаемыми вокруг химического символа атома. Общие для двух атомов электроны показывают точками, помещаемыми между их химическими символами; двойная или тройная связь обозначается соответственно двумя или тремя парами общих точек.
- 117 -
Применяя эти обозначения, образование молекулы водорода можно представить следующим образом:
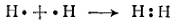
Эта схема показывает, что при соединении двух атомов водорода в молекулу каждый из атомов приобретает устойчивую двухэлектронную оболочку, подобную электронной оболочке атома гелия.
Аналогичными схемами можно представить образование молекулы азота:
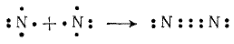
При соединении двух атомов азота в молекулу общими становятся три пары электронов (тройная связь); благодаря этому наружная оболочка каждого атома дополняется до устойчивой восьмиэлектронной конфигурации атома неона.
Строение молекул некоторых сложных веществ — аммиака, воды, диоксида углерода и метана можно изобразить схемами:
|
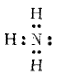
|

|
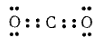
|

|
|
аммиак |
вода |
диоксид углерода |
метан |
В молекуле аммиака каждый из трех атомов водорода связан с атомом азота парой общих электронов (один электрон от атома водорода, другой — от атома азота). Таким образом, азот имеет восьмиэлектронную внешнюю оболочку, а ядро каждого атома водорода окружено двумя электронами, образующими устойчивую «гелиевую» оболочку. Такие же оболочки имеют атомы водорода в молекулах воды и метана. В молекуле диоксида углерода, где атом углерода связан с каждым из атомов кислорода двумя парами электронов (двойная связь), все три атома имеют вольмиэлектронные внешние оболочки.
Из приведенных схем видно, что каждая пара электронов, связывающих два атома, соответствует одной черточке, изображающей ковалентную связь в структурных формулах.
|
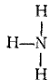
|
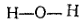
|
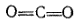
|

|
|
аммиак |
вода |
диоксид углерода |
метан |
Число таких общих электронных пар, связывающих атом данного элемента с другими атомами, или иначе говоря, число образуемых атомом ковалентных связей, называется ковалентностью элемента в соответствующем соединении.
- 118 -
Так, ковалентность азота в молекулах N2 и NH3 равна трем, ковалентность кислорода в молекулах H2O и CO2 — двум, ковалентность углерода в молекулах CH4 и CO2 — четырем.
| <<< Назад 38. Теория химического строения. |
Вперед >>> 40. Неполярная и полярная ковалентная связь. |
- 38. Теория химического строения.
- 39. Ковалентная связь. Метод валентных связей.
- 40. Неполярная и полярная ковалентная связь.
- 41. Способы образования ковалентной связи.
- 42. Направленность ковалентной связи.
- 43. Гибридизация атомных электронных орбиталей.
- 44. Многоцентровые связи.
- 45. Метод молекулярных орбиталей.
- 46. Ионная связь.
- 47. Водородная связь.
