Книга: Общая химия
36. Радиоактивные элементы и их распад.
| <<< Назад 35. Строение атомных ядер. Изотопы. |
Вперед >>> 37. Искусственная радиоактивность. Ядерные реакции. |
36. Радиоактивные элементы и их распад.
Явление радиоактивности уже было кратко рассмотрено в § 20. Используя понятие об изотопах, можно дать более строгое определение этому явлению: радиоактивностью называется самопроизвольное превращение неустойчивого изотопа одного химического элемента в изотоп другого элемента, сопровождающееся испусканием элементарных частиц или ядер (например, ?-частиц). Радиоактивность, проявляемая природными изотопами элементов, называется естественной радиоактивностью.
Процессы радиоактивных превращений протекают у разных изотопов с различной скоростью. Эта скорость характеризуется постоянной радиоактивного распада, показывающей, какая часть общего числа атомов радиоактивного изотопа распадается в 1 с.
- 102 -
Чем больше радиоактивная постоянная, тем быстрее распадается изотоп.
Изучение процессов радиоактивного распада показало, что количество атомов радиоактивного изотопа, распадающихся в единицу времени, пропорционально имеющемуся в данный момент общему количеству атомов этого изотопа. Другими словами, всегда распадается одна и та же часть имеющегося числа атомов. Таким образом, если в течение некоторого времени разложилась половина имевшегося радиоактивного изотопа, то в следующий такой же промежуток времени разложится половина остатка, т.е. вдвое меньше, чем в предыдущий, и т.д.
Наблюдая, например, за изменением количества радона, установили, что через 3,85 суток остается половина первоначального количества, через 3,85 суток — только 1/4, затем 1/8 и т.д.
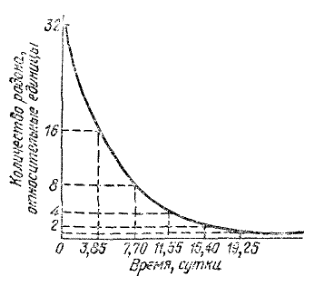
Рис. 25. Зависимость количества не распавшегося радона от времени.
Промежуток времени, в течение которого разлагается половина первоначального количества радиоактивного элемента, называется периодом полураспада. Эта величина характеризует продолжительность жизни элемента.
Для различных радиоактивных элементов она колеблется от долей секунды до миллиардов лет. Так, период полураспада радона составляет 3,85 суток, радия 1620 лет, урана 4,5 миллиарда лет.
К основным видам радиоактивного распада относятся ?-распад, ?-распад, электронный захват и спонтанное деление. Часто эти виды радиоактивного распада сопровождаются испусканием ?-лучей, т.е. жесткого (с малой длиной волны) электромагнитного излучения.
При ?-распаде ядро атома испускает два протона и два нейтрона, связанные в ядро атома гелия 24He; это приводит к уменьшению заряда исходного радиоактивного ядра на 2, а его массового числа на 4. Таким образом, в результате ?-распада образуется атом элемента, смещенного на два места от исходного радиоактивного элемента к началу периодической системы.
Возможность ?-распада связана с тем, что, по современным представлениям, протон и нейтрон представляют собой два состояния одной и той же элементарной частицы — нуклона (от латинского nucleus — ядро).
- 103 -
При известных условиях (например, когда избыток нейтронов в ядре приводит к его неустойчивости) нейтрон может превращаться в протон, одновременно «рождая» электрон. Этот процесс можно изобразить схемой:
Нейтрон?Протон + Электрон* или n ? p + e-,
Таким образом, при ?-распаде один из нейтронов, входящих в состав ядра, превращается в протон; возникающий при этом электрон вылетает из ядра, положительный заряд которого на единицу возрастает.
Возможно также превращение протона в нейтрон в соответствии со схемой:
Протон? Нейтрон + Позитрон* или p ? n + e+
Позитрон, обозначенный e+, - элементарная частица с массой, равной массе электрона, но несущая положительный электрический заряд; по абсолютной величине заряды электрона и позитрона одинаковы.
Процесс превращения протона в нейтрон с образованием позитрона может происходить в тех случаях, когда неустойчивость ядра вызвана избыточным содержанием в нем протонов. При этом один из протонов, входящих в состав ядра, превращается в нейтрон, возникающий позитрон вылетает за пределы ядра, а заряд ядра на единицу уменьшается. Такой вид радиоактивного распада называется позитронным ?-распадом (или ?+-распадом) в отличие от ранее рассмотренного электронного ?-распада ( ?—распада). Этот вид радиоактивного превращения наблюдается у некоторых искусственно полученных радиоактивных изотопов.
Изменение заряда-ядра при ?-распаде приводит к тому, что в результате ?-распада образуется атом элемента, смещенного на одно место от исходного радиоактивного элемента к концу периодической системы (в случае ?- -распада) или к ее началу (в случае ?+-распада).
К уменьшению заряда ядра на единицу при сохранении массового числа атома приводит не только ?+ -распад, но и электронный захват, при котором один из электронов атомной электронной оболочки захватывается ядром; взаимодействие этого электрона с одним из содержащихся в ядре протонов приводит к образованию нейтрона:
e- + p ?n
Электрон чаще всего захватывается из ближайшего к ядру K — слоя (K -захват), резе из L- или M-слоев.
*При взаимопревращениях протона и нейтрона образуются также другие элементарные частицы (нейтрино и антинейтрино). Поскольку масса покоя и электрический заряд этих частиц равны нулю, их участие в радиоактивных превращениях не отражено в проводимых здесь схемах.
- 104 -
Спонтанным делением называется самопроизвольный распад ядер тяжелых элементов на два (иногда на три или на четыре) ядра элементов середины периодической системы. Варианты такого деления очень разнообразны, так что общих правил смещения по периодической системе не существует; чаще всего происходит распад исходного ядра на тяжелый и легкий осколки, несущие соответственно около 60 и 40% заряда и массы исходного ядра. Относительно содержание нейтронов в ядрах изотопов тяжелых элементов выше, чем в ядрах устойчивых изотопов середины периодической системы. Поэтому при спонтанном делении распадающееся ядро испускает 2-4 нейтрона; образующиеся ядра все еще содержат избыток нейтронов, оказываются неустойчивыми и поэтому претерпевают последовательный ряд ?-распадов.
Элементы, расположенные в конце периодической системы (после висмута), не имеют стабильных изотопов. Подвергаясь радиоактивному распаду, они превращаются в другие элементы. Если вновь образовавшийся элемент радиоактивен, он тоже распадается, превращаясь в третий элемент, и так далее до тех пор, пока не получаются атомы устойчивого изотопа. Ряд элементов, образующихся подобным образом один из другого, называется радиоактивным рядом. Примером может служить приводимый ниже ряд урана — последовательность продуктов превращения изотопа 238U, составляющего преобладающую часть природного урана; для каждого превращения указан тип радиоактивного распада (над стрелкой) и период полураспада (под стрелкой):
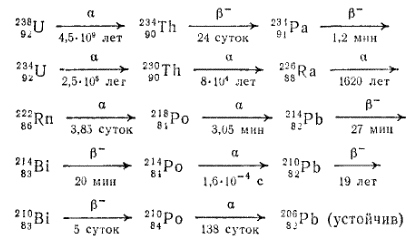
Таким образом, конечным продуктом распада является устойчивый изотоп свинца.
При ?-распаде массовое число изотопа не меняется, а при ?-распаде уменьшается на 4. Поэтому возможно существование четырех радиоактивных рядов: один из них включает изотопы, массовые числа которых выражаются общей формулой 4n (n — целое число), второму отвечает общая формула массового числа 4n + 1, третьему - 4n + 2 (это и есть радиоактивный ряд урана) и четвертому - 4n + 3.
- 105 -
Действительно, помимо ряда урана, известны еще два естественных радиоактивных ряда: ряд тория, начинающийся с изотопа 232Th и соответствующий общей формуле массового числа 4n, и ряд актиния, начинающийся с изотопа 235U («актиноуран») и отвечающий общей формуле массового числа 4n + 3. Устойчивые продукты превращений в этих рядах тоже представляют собой изотопы свинца (208Pb и 207Pb). Родоначальником четвертого радиоактивного ряда (ряда нептуния) с общей формулой массового числа 4n + 1 служит изотоп искусственно полученного элемента нептуния 23793Np; здесь конечным продуктом распада является устойчивый изотоп висмута 209Bi.
Накопление свинца в результате распада содержащихся в минералах радиоактивных элементов позволяет определить возраст соответствующих горных пород. Зная скорость распада 238U, 232Th и 235U и определив их содержание, а также содержание и изотопный состав свинца в минерале, можно вычислить возраст минерала, т.е. время, прошедшее с момента его образования (так называемый свинцовый метод определения возраста). Для минералов с плотной кристаллической упаковкой, хорошо сохраняющей содержащиеся в кристаллах газы, возраст радиоактивного минерала можно установить по количеству гелия накопившегося в нем в результате радиоактивных превращений (гелиевый метод). Для определения возраста сравнительно молодых образований (до 70 тыс. лет) применяется радиоуглеродный метод, основанный на радиоактивном распаде изотопа углерода 14C (период полураспада около 5600) лет). Этот изотоп образуется в атмосфере под действием космического излучения и усваивается организмами, после гибели которых его содержание убывает по закону радиоактивного распада. Возраст органических остатков (ископаемые организмы, торф, осадочные карбонатные породы) может быть определен путем сравнения радиоактивности содержащегося в них углерода с радиоактивностью углерода атмосферы.
| <<< Назад 35. Строение атомных ядер. Изотопы. |
Вперед >>> 37. Искусственная радиоактивность. Ядерные реакции. |
- 20. Радиоактивность.
- 21. Ядерная модель атома.
- 23. Квантовая теория света.
- 24. Строение электронной оболочки атома по Бору.
- 25. Исходные представления квантовой механики.
- 26. Волновая функция.
- 27. Энергетическое состояние электрона в атоме.
- 28. Главное квантовое число.
- 29. Орбитальное квантовое число. Формы электронных облаков.
- 30. Магнитное и спиновое квантовые числа.
- 31. Много электронные атомы.
- 32. Принцип Паули. Электронная структура атомов и периодическая система элементов.
- 33. Размеры атомов и ионов.
- 34. Энергия ионизации и сродство к электрону.
- 35. Строение атомных ядер. Изотопы.
- 36. Радиоактивные элементы и их распад.
- 37. Искусственная радиоактивность. Ядерные реакции.
- 4. КАК ОТКРЫВАЛИСЬ ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ И СОЗДАВАЛАСЬ ПЕРИОДИЧЕСКАЯ СИСТЕМА
- Биогенные элементы в движении
- Вирусы и мобильные генетические элементы
- Животные держат мобильные генетические элементы под контролем
- Эгоистичные гены, мусорная ДНК и мобильные элементы
- Химические элементы и вещества
- 2. Элементы развития у одноклеточных
- 427. Какие химические элементы содержатся в морской воде в наибольших количествах?
- 433. Какие элементы содержатся в океане в больших количествах, чем на суше?
- 677. Какие элементы накапливаются морскими организмами?
- 676. Какие редкие элементы необходимы для роста морских растений?
- 945. Безопасно ли сбрасывать радиоактивные отходы в глубоководных районах океана?
