Книга: Общая химия
30. Магнитное и спиновое квантовые числа.
| <<< Назад 29. Орбитальное квантовое число. Формы электронных облаков. |
Вперед >>> 31. Много электронные атомы. |
30. Магнитное и спиновое квантовые числа.
В предыдущих параграфах мы выяснили, что размеры и формы электронных облаков в атоме могут быть не любыми, а только такими, которые соответствуют возможным значениям квантовых чисел n и l. Из уравнения Шредингера следует, что и ориентация электронного облака в пространстве не может быть произвольной: она определяется значением третьего, так называемого магнитного квантового числа m.
Магнитное квантовое число может принимать любые целочисленные значения — как положительные, так и отрицательные — в пределах от + l до — l. Таким образом, для разных значений l число возможных значений m различно. Так, для s-электронов (l=0) возможны три различных значения m (-1, 0, +1); при l=2 (d-электроны) m может принимать пять различных значений (-2, -1, 0, +1, +2). Вообще, некоторому значению l соответствует (2l+1) возможных значений магнитного квантового числа, т.е. (2l+1) возможных расположений электронного облака в пространстве.
Мы уже знаем, что орбитальный момент количества движения электрона представляет собой вектор

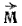
- 80 -
Рис. 19. К возможному набору значений магнитного квантового числа.
Стрелками показаны допустимые направления орбитального момента количества движения.
Набор возможных значений m можно пояснить следующим образом. Выберем некоторое направление в пространстве, например, ось z (рис. 19). Каждому направлению вектора заданной длины (в рассматриваемом случае — орбитального квантового числа l*) соответствует определенное значение его проекции на ось z. Из уравнения Шредингера следует, что эти направления могут быть только такими, при которых проекция вектора l на ось z равна целому числу (положительному или отрицательному) или нулю; значение этой проекции и есть магнитное квантовое число m. На рис. 19 представлен случай, когда l=2. Здесь m=2, если направления оси z и вектора l совпадают; m=-2, когда эти направления противоположны; m=0, когда вектор l перпендикулярен оси z; возможны и такие направления вектора l, когда m принимает значения ±1. Таким образом, магнитное квантовое число может принимать 2l+1 значений.
Квантовое число m получило название магнитного, поскольку от его значения зависит взаимодействие магнитного поля, создаваемого электроном, с внешним магнитным полем. В отсутствие внешнего магнитного поля энергия электрона в атоме не зависит от значения m. В этом случае электроны с одинаковыми значениями n и l, но с разными значениями m обладают одинаковой энергией.
Однако при действии на электрон внешнего магнитного поля энергия электрона в атоме изменяется, так что состояния электрона, различающиеся значением m, различаются и по энергии. Это происходит потому, что энергия взаимодействия магнитного поля электрона с внешним магнитным полем зависит от величины магнитного квантового числа. Именно поэтому в магнитном поле происходит расщепление некоторых атомных спектральных линий; вместо одной линии в спектре атома появляются несколько (так называемый эффект Зеемана).
Состояние электрона в атоме, характеризующееся определенными значениями квантовых чисел n, l и m, т.е. определенными размерами, формой и ориентацией в пространстве электронного облака, получило название атомной электронной орбитали.
На рис. 20 приведены формы и расположение в пространстве электронных облаков, соответствующих 1s-, 2p- и 3d-орбиталям. Поскольку s-состоянию (l=0) соответствует единственной значение магнитного квантового числа (m=0), то любые возможные расположения s-электронного облака в пространстве идентичны. Электронные облака, отвечающие p-орбиталям (l=0), могут характеризоваться тремя различными значениями m; в соответствии с этим они могут располагаться в пространстве тремя способами (рис. 20).
* Более строго следует рассматривать проекцию на ось z не орбитального квантового числа l, а определяемого им орбитального момента количества движения М.
- 81 -
При этом три p-электронных облака ориентированы во взаимно перпендикулярных направлениях, которые обычно принимают за направления координатных осей (x, y или z); соответствующие состояния электронов принято обозначать px, py и pz. Для d-орбиталей (l=2) возможно уже пять значений магнитного квантового числа и соответственно пять различных ориентаций d-электронных облаков в пространстве.
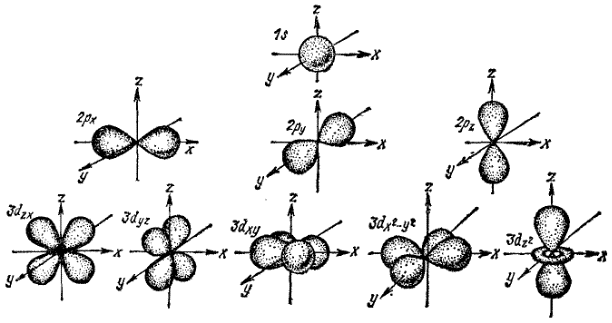
Рис. 20. Формы и пространственная ориентация электронных облаков 1s-, 2p- 3d-электронов.
Исследования атомных спектров привели к выводу, что, помимо квантовых чисел n, l и m, электрон характеризуется еще одной квантовой величиной, не связанной с движением электрона вокруг ядра, а определяющей его собственное состояние. Эта величина получила название спинового квантового числа или просто спина (от английского spin — кручение, вращение); спин обычно обозначают буквой s. Спин электрона может иметь только два значения: +1/2 или -1/2; таким образом, как и в случае остальных квантовых чисел, возможные значения спинового квантового числа различаются на единицу.
Кроме орбитального момента количества движения, определяемого значением l, электрон обладает и собственным моментом количества движения, что можно упрощенно рассматривать как результат вращения электрона вокруг своей оси. Проекция собственного момента количества движения электрона на избранное направление (например, на ось z) и называется спином.
Четыре квантовых числа — n, l, m и s — полностью определяют состояние электрона в атоме.
| <<< Назад 29. Орбитальное квантовое число. Формы электронных облаков. |
Вперед >>> 31. Много электронные атомы. |
- 20. Радиоактивность.
- 21. Ядерная модель атома.
- 23. Квантовая теория света.
- 24. Строение электронной оболочки атома по Бору.
- 25. Исходные представления квантовой механики.
- 26. Волновая функция.
- 27. Энергетическое состояние электрона в атоме.
- 28. Главное квантовое число.
- 29. Орбитальное квантовое число. Формы электронных облаков.
- 30. Магнитное и спиновое квантовые числа.
- 31. Много электронные атомы.
- 32. Принцип Паули. Электронная структура атомов и периодическая система элементов.
- 33. Размеры атомов и ионов.
- 34. Энергия ионизации и сродство к электрону.
- 35. Строение атомных ядер. Изотопы.
- 36. Радиоактивные элементы и их распад.
- 37. Искусственная радиоактивность. Ядерные реакции.
- Как пахнет электромагнитное поле?
- Магнитное поле.
- § 29 Электромагнитное поле
- Глава 2. КВАНТОВЫЕ СТРАННОСТИ
- Таинственная геология Луны: магнитное поле, извержения вулканов, сейсмическая активность
- Магнитное поле Меркурия
- Внутреннее строение и магнитное поле
- Межпланетное магнитное поле
- Магнитное поле Земли
- Солирует электромагнитное поле
- 7. Квантовые гены
- Глава 4. Вселенная в числах
