Книга: Общая химия
29. Орбитальное квантовое число. Формы электронных облаков.
| <<< Назад 28. Главное квантовое число. |
Вперед >>> 30. Магнитное и спиновое квантовые числа. |
29. Орбитальное квантовое число. Формы электронных облаков.
Не только энергия электрона в атоме (и связанный с ней размер электронного облака) может принимать лишь определенные значения. Произвольной не может быть и форма электронного облака. Она определяется орбитальным квантовым числом l (его называют также побочным, или азимутальным), которое может принимать целочисленные значения от 0 до ( n — 1), где n — главное квантовое число. Различным значениям n отвечает разное число возможных значений l. Так, при n=1 возможно только одно значение орбитального квантового числа — нуль (l=0), при n=2 может быть равным 0 или 1, при n=3 возможны значения l, равные 0, 1 и 2, вообще, данному значению главного квантового числа n соответствуют n различных возможных значений орбитального квантового числа.
Вывод о том, что формы атомных электронных облаков не могут быть произвольными, вытекает из физического смысла квантового числа l. Именно, оно определяет значение орбитального момента количества движения электрона; эта величина, как и энергия, является квантованной физической характеристикой состояния электрона в атоме.
Напомним, что орбитальным моментом количества движения
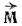
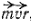
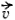
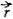
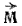
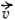
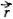
Определенной форме электронного облака соответствует вполне определенное значение орбитального момента количества движения электрона
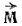
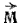
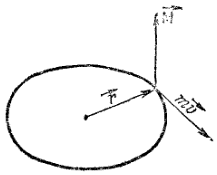
Рис 7. К понятию об орбитальном моменте количества движения.

Рис. 8. К понятию о размерах и форме электронного облака
Мы уже знаем, что энергия электрона в атоме зависит от главного квантового числа n. В атоме водорода энергия электрона полностью определяется значением n.
- 75 -
Однако в многоэлектронных атомах энергия электрона зависит и от значения орбитального квантового числа l; причины этой зависимости будут рассмотрены в § 31. Поэтому состояния электрона, характеризующиеся различными значениями l, принято называть энергетическими подуровнями электрона в атоме. Этим подуровням присвоены следующие буквенные обозначения:

В соответствии с этими обозначениями говорят об s-подуровне, p-подуровне и т.д. Электроны, характеризующиеся значениями побочного квантового числа 0, 1, 2 и 3, называют соответственно s-электронами, p-электронами, d-электронами и f-электронами. При данном значении главного квантового числа n наименьшей энергией обладают s-электроны, затем p-, d- и f- электроны.
Состояние электрона в атоме, отвечающее определенным значениям n и l, записывается следующим образом: сначала цифрой указывается значение главного квантового числа, затем буквой — орбитального квантового числа. Так, обозначение 2p относится к электрону, у которого n=2 и l=1, обозначение 3d к электрону, у которого n=3 и l=2.
Электронное облако не имеет резко очерченных в пространстве границ. Поэтому понятие о его размерах и форме требует уточнения. Рассмотрим в качестве примера электронное облако 1s-электрона в атоме водорода (рис. 8). В точке а, находящейся на некотором расстоянии от ядра, плотность электронного облака определяется квадратом волновой функции ?a2. Проведем через точку а поверхность равной электронной плотности, соединяющую точки в которых плотность электронного облака характеризуется тем же значением ?a2. В случае 1s-электрона такая поверхность окажется сферой, внутри которой заключена некоторая часть электронного облака (на рис. 8 сечение этой сферы плоскостью рисунка изображено окружностью, проходящей через точку а). Выберем теперь точку b, находящуюся на б'ольшем расстоянии от ядра, и также проведем через нее поверхность равной электронной плотности. Эта поверхность тоже будет обладать сферической формой, но внутри ее будет заключена б'ольшая часть электронного облака, чем внутри сферы а. Пусть, наконец, внутри поверхности равной электронной плотности, проведенной через некоторую точку с, заключена преобладающая часть электронного облака; обычно эту поверхность проводят так, чтобы она заключала 90% заряда и массы электрона. Такая поверхность называется граничной поверхностью, и именно ее форму и размеры принято считать формой и размерами электронного облака. Граничная поверхность 1s-электрона представляет собой сферу, однако граничные поверхности p- и d-электронов имеют более сложную форму (см. ниже).
- 76 -

Рис. 9. Графики функции ? и ?2 для 1s-электрона.
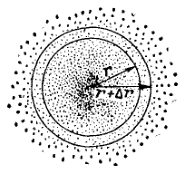
Рис. 10. Электронное облако 1s-электрона.
На рис. 9 изображены значения волновой функции ? (рис. 9, а) и ее квадрата (рис. 9, б) для 1s-электрона в зависимости от расстояния от ядра r. Изображенные кривые не зависят от направления, в котором откладывается измеряемое расстояние r; это означает, что электронное облако 1s-электрона обладает сферической симметрией, т.е. имеет форму шара. Кривая на рис. 9, а расположена по одну сторону от оси расстояний (ось абсцисс). Отсюда следует, что волновая функция 1s-электрона обладает постоянным знаком; будем считать его положительным.
Рис. 9, б показывает также, что при увеличении расстояния от ядра величина ?2 монотонно убывает. Это означает, что по мере удаления от ядра плотность электронного облака 1s-электрона уменьшается; иллюстрацией этого вывода может служить рис. 5.
Это не означает, однако, что с ростом r вероятность обнаружить 1s-электрон тоже монотонно убывает. На рис. 10 выделен тонкий слой, заключенный между сферами с радиусами r и (r + ?r), где ?r — некоторая малая величина. С ростом r плотность электронного облака в рассматриваемом сферическом слое уменьшается; но одновременно возрастает объем этого слоя, равный 4? r2 ?r. Как указывалось в § 26, вероятность обнаружить электрон в малом объеме ?V выражается произведением ?2 ?V. В данном случае ?V = 4? r2 ?r; следовательно, вероятность обнаружения электрона в сферическом слое, заключенном между r и (r + ?r), пропорциональна величине 4? r2?2, В этом произведении с увеличением r множитель 4? r2 возрастает, а множитель ?2 убывает. При малых значениях r величина 4? r2 возрастает быстрее, чем убывает ?2, при больших наоборот. Поэтому произведение 4? r2?2, характеризующее вероятность обнаружения электрона на расстоянии r от ядра, с увеличением r проходит через максимум.
Зависимость величины 4? r2?2 от r изображена для 1s-электрона на рис. 11 (подобные графики называются графиками радиального распределения вероятности нахождения электрона). Как показывает рис. 11, вероятность обнаружить 1s-электрон на малых расстояниях от ядра близка к нулю, так как r мало. Ничтожно мала и вероятность обнаружения электрона на очень большом расстоянии от ядра: здесь близок к нулю множитель (см. рис. 9, б).
Рис. 11 График радиального распределения вероятности для 1s-электрона.
- 77 -
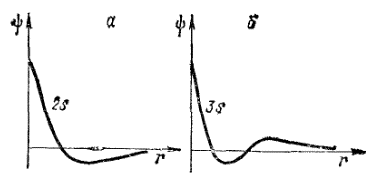
Рис. 12. Графики волновой функции для 2s-(а) и 3s-электронов (б).
На некотором расстоянии от ядра r0 вероятность обнаружения электрона имеет максимальное значение. Для атома водорода это расстояние равно 0,053 нм, что совпадает с вычисленным Бором значением радиуса ближайшей к ядру орбиты электрона. Однако трактовка этой величины в теории Бора и с точки зрения квантовой механики различна: согласно Бору, электрон в атоме водорода находится на расстоянии 0,053 нм от ядра, а с позиций квантовой механики этому расстоянию соответствует лишь максимальная вероятность обнаружения электрона.
Электронные облака s-электронов второго, третьего и последующих слоев обладают, как и в случае 1s-электронов, сферической симметрией, т.е. характеризуются шарообразной формой. Однако здесь волновая функция при увеличении расстояния от ядра меняется более сложным образом. Как показывает рис. 12, зависимость ? от r для 2s- и 3s-электронов не является монотонной, на разных расстояниях от ядра волновая функция имеет различный знак, а на соответствующих кривых есть узловые точки (или узлы), в которых значение волновой функции равно нулю. В случае 2s-электрона имеется один узел, в случае 3s-электрона — 2 узла и т.д. В соответствии с этим, структура электронного облака здесь также сложнее, чем у 1s-электрона. На рис. 13 в качестве примера схематически изображено электронное облако 2s-электрона.

Рис. 13. Схематическое изображение электронного облака 2s-электрона.
- 78 -
Более сложный вид имеют и графики радиального распределения вероятности для 2s- и 3s-электронов (рис. 14).
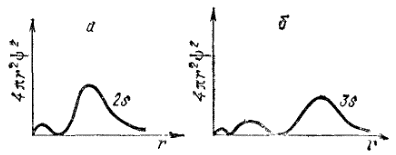
Рис 14. Графики радиального распределения вероятности для 2s- (а) и 3s-электронов (б).
Здесь появляется уже не один максимум, как в случае 1s-электрона, а соответственно два или три максимума. При этом главный максимум располагается тем дальше от ядра, чем больше значение главного квантового числа n.
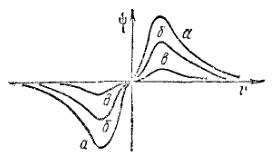
Рис. 15. График волновой функции 2p-электрона.
Рассмотрим теперь структуру электронного облака 2p-электрона. При удалении от ядра по некоторому направлению волновая функция 2p-электрона изменяется в соответствии с кривой, изображенной на рис. 15, а. По одну сторону от ядра (на рисунке - справа) волновая функция положительна, и здесь на кривой имеется максимум, по другую сторону от ядра (на рисунке — слева) волновая функция отрицательна, на кривой имеется минимум; в начале координат значение ? обращается в нуль. В отличие от s-электронов, волновая функция 2p-электрона не обладает сферической симметрией. Это выражается в том, что высота максимума (и соответственно глубина минимума) на рис. 15 зависит от выбранного направления радиуса-вектора r. В некотором направлении (для определенности будем считать его направлением оси координат x) высота максимума наибольшая (рис. 15, а). В направлениях , составляющих угол с осью x, высота максимума тем меньше, чем больше этот угол (рис. 15, б, в); если он равен 90?, то значение ? в соответствующем направлении равно нулю при любом расстоянии от ядра.
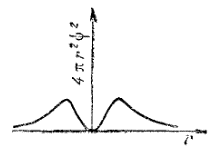
Рис. 16. График радиального распределения вероятности для 2p-электрона.
График радиального распределения вероятности для 2p-электрона (рис. 16) имеет вид, сходный с рис. 15, с той разницей, что вероятность обнаружения электрона на некотором расстоянии от ядра всегда положительна. Положение максимума на кривой распределения вероятности не зависит от выбора направления. Однако высота этого максимума зависит от направления: она наибольшая, когда радиус-вектор совпадает с направлением оси x, и убывает по мере отклонения радиуса-вектора от этого направления.
Такому распределению вероятности обнаружения 2p-электрона соответствует форма электронного облака напоминающая двойную грушу или гантель (рис. 17). Как видно, электронное облако сосредоточено вблизи оси x, а в плоскости yz, перпендикулярной этой оси, электронного облака нет: вероятность обнаружить здесь 2p-электрон равна нулю.
- 79 -
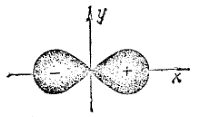
Рис. 17. Схематическое изображение электронного облака 2p-электрона.
Знаки «+» и «-» на рис. 17 относятся не к вероятности обнаружения электрона (она всегда положительна!), а к волновой функции ?, которая в разных частях электронного облака имеет различный знак.
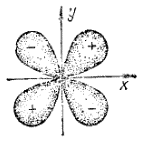
Рис. 18. Схематическое изображение электронного облака 3p-электрона.
Рис. 17 приближенно передает форму электронного облака не только 2p-электронов, но также и p-электронов третьего и последующих слоев. Но графики радиального распределения вероятности имеют здесь более сложный характер: вместо одного максимума, изображенного в правой части рис. 16, на соответствующих кривых появляются два максимума (3p-электрон), три максимума (4p-электрон) и т.д. При этом наибольший максимум располагается все дальше от ядра.
Еще более сложную форму имеют электронные облака d-электронов (l=2). Каждое из них представляет собой «четырехлепестковую» фигуру причем знаки волновой функции в «лепестках» чередуются (рис. 18).
| <<< Назад 28. Главное квантовое число. |
Вперед >>> 30. Магнитное и спиновое квантовые числа. |
- 20. Радиоактивность.
- 21. Ядерная модель атома.
- 23. Квантовая теория света.
- 24. Строение электронной оболочки атома по Бору.
- 25. Исходные представления квантовой механики.
- 26. Волновая функция.
- 27. Энергетическое состояние электрона в атоме.
- 28. Главное квантовое число.
- 29. Орбитальное квантовое число. Формы электронных облаков.
- 30. Магнитное и спиновое квантовые числа.
- 31. Много электронные атомы.
- 32. Принцип Паули. Электронная структура атомов и периодическая система элементов.
- 33. Размеры атомов и ионов.
- 34. Энергия ионизации и сродство к электрону.
- 35. Строение атомных ядер. Изотопы.
- 36. Радиоактивные элементы и их распад.
- 37. Искусственная радиоактивность. Ядерные реакции.
- 28. Главное квантовое число.
- § 34. Образование облаков, осадки
- Размеры островов и число видов
- 2.7. Клетка – генетическая единица живого. Хромосомы, их строение (форма и размеры) и функции. Число хромосом и их видов...
- 4. Число активных генов и число копий мРНК
- Юньнань. Рай – это к югу от облаков
- Таблица 3.4. Число открытых АСЗ и потенциально опасных астероидов (на 1 июня 2010 г.)
- Таблица 3.2. Число занумерованных малых планет на начало соответствующего года
- Природа облаков Венеры и их роль в тепловом балансе
- Строение облаков Венеры
- Состав облаков Венеры
- Динамика и химия облаков
