Книга: Общая химия
214. Цинк (Zincum).
| <<< Назад 213. Стронций (Strontium). Барий (Barium). |
Вперед >>> 215. Кадмий (Cadmium). |
214. Цинк (Zincum).
Главные природные соединения цинка, из которых его добывают, — минералы галмей ZnCO3 и цинковая обманка ZnS, Общее содержание цинка в земной коре составляет приблизительно 0,01% (масс.).
Большинство цинковых руд содержат небольшие количества цинка, поэтому их предварительно обогащают, получая цинковый концентрат. Последний подвергают обжигу; при этом сульфид цинка превращается в оксид:
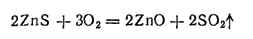
Обжиг ведется в многоподовых или в шахтных печах. В последнее время при обжиге цинковых руд широко применяется обжиг в «кипящем слое».
- 601 -
Метод обработки мелко раздробленных твердых материалов в так называемом «кипящем слое» получил широкое распространение в различных отраслях промышленности. Этот метод заключается в следующем. Через слой порошкообразного материала, помещенного на решетке, продувают снизу воздух (или какой-либо газ) с такой скоростью, что его струи пронизывают и интенсивно перемешивают материал, приводя его как бы в «кипящее» состояние. Такое состояние твердого материала часто называют «псевдоожиженным», так как кипеть могут только вещества, находящиеся в жидком состоянии.
Благодаря тесному соприкосновению твердого материала с газом химические реакции в «кипящем слое» протекают с большой скоростью. Применение обжига в «кипящем слое» дает повышение производительности обжиговых печей в 3—4 раза при более полном извлечении цинка из концентрата.
Метод весьма эффективен при обжиге сульфидных руд и концентратов, сублимации сравнительно летучих металлов, прокаливании, охлаждении и сушке различных веществ.
Из обожженного концентрата цинк извлекают, восстанавливая его коксом и отгоняя образующиеся пары цинка.
Другой метод восстановления цинка заключается в электролитическом выделении его из сульфата. Последний получается обработкой обожженных концентратов серной кислотой.
Цинк — голубовато-серебристый металл. При комнатной температуре он довольно хрупок, но при 100-150°C он хорошо гнется и прокатывается в листы. При нагревании выше 200°C цинк становится очень хрупким. На воздухе он покрывается тонким слоем оксида или основного карбоната, предохраняющим его от дальнейшего окисления. Вода почти не действует на цинк, хотя он и стоит в ряду напряжений значительно раньше водорода. Это объясняется тем, что образующийся на поверхности цинка при взаимодействии его с водой гидроксид практически нерастворим и препятствует дальнейшему течению реакции. В разбавленных же кислотах цинк легко растворяется с образованием соответствующих солей. Кроме того, цинк, подобно бериллию и другим металлам, образующим амфотерные гидроксиды, растворяется в щелочах. Если сильно нагреть цинк в атмосфере воздуха, то пары его воспламеняются и сгорают зеленовато-белым пламенем, образуя ZnO.
Применение цинка очень разнообразно. Значительная часть его идет для нанесения покрытий на железные и стальные изделия, предназначенные для работы в атмосферных условиях или в воде. При этом цинковые покрытия в течение многих лет хорошо защищают основной металл от коррозии. Однако в условиях высокой влажности воздуха при значительных колебаниях температуры, а также в морской воде цинковые покрытия неэффективны. Широкое промышленное использование имеют сплавы цинка с алюминием, медью и магнием. С медью цинк образует важную группу сплавов — латуни (см. § 200). Значительное количество цинка расходуется для изготовления гальванических элементов.
Марганцово-цинковый элемент. Из всех применяемых в настоящее время гальванических элементов маргаицово-цииковые наиболее распространены. Имеется несколько разновидностей элементов этой системы, но в основе действия их всех лежит окислительно-восстановительная реакция между цинком и диоксидом марганца.
- 602 -
В элементах этой системы один электрод цинковый, другой состоит из MnO2. Оба электрода находятся в растворе хлорида аммония.
При работе элемента цинк окисляется:
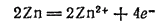
Часть образующихся ионов цинка связывается молекулами аммиака в комплексный ион:
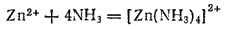
Молекулы аммиака образуются в растворе вследствие гидролиза иона аммония:
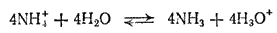
Электроны, получающиеся при окислении цинка, по внешней цепи переходят к диоксиду марганца, который при этом восстанавливается. В результате восстановления MnO2 получается смесь нескольких продуктов. В наибольшем количестве получается соединение MnOOH, в котором степень окисленности марганца равна +3:
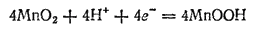
Таким образом, цинковый электрод элемента является анодом и заряжен отрицательно, а электрод из MnO2 служит катодом и заряжен положительно.
Имеющиеся в растворе ионы NH4+ и Cl- при работе элемента движутся в направлениях, обусловленных процессами, протекающими в электродах. Поскольку у цинкового электрода катионы цинка выходят в раствор, а у катода раствор все время обедняется катионами H+, то в создающемся электрическом поле ионы NH4+, движутся при работе элемента к катоду, а ионы Cl- к аноду. Таким образом, раствор во всех его частях остается электро-нейтральным.
Если сложить последние четыре уравнения, отвечающие отдельным протекающим при работе элемента процессам, то получится суммарное уравнение окислительно-восстановительной реакции, идущей в элементе:
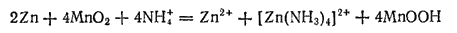
Марганцово-цинковые элементы не содержат в себе раствора в обычном понимании этого слова. Необходимый для их работы раствор NH4Cl в одних конструкциях имеет консистенцию пасты, в других им пропитан пористый картон, помещаемый между электродами. Поэтому эти гальванические элементы носят условное название сухих элементов.
Марганцово-цинковые элементы широко применяются в качестве источников электропитания установок связи, различных измерительных приборов, карманных фонарей.
Воздушно-цинковый элемент. Здесь отрицательным электродом является цинк, а активным веществом положительного электрода служит кислород воздуха (поры электрода, изготовляемого из смеси активного угля с графитом, заполнены воздухом). Кислород диффундирует к поверхности раздела электрод — раствор. В качестве электролита применяются растворы NaOH или NH4Cl.
При работе такого элемента в нем протекает окислительно-восстановительная реакция, которая в случае щелочного электролита выражается уравнением:
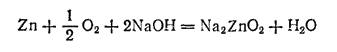
Механические и коррозионные свойства цинка зависят от присутствия в нем небольших количеств примесей других металлов.
- 603 -
Например, примесь железа повышает хрупкость цинка и его сплавов и затрудняет их обработку, а также резко увеличивает скорость коррозии цинка в кислотах. Поэтому высококачественные сплавы цинка содержат очень малые количества примесей других металлов. Например, примесь свинца не должна превышать 0.01%, а железа — 0.1%.
Оксид цинка ZnO — рыхлый белый порошок, желтеющий при нагревании, но при охлаждении снова становящийся белым. Оксид цинка применяется для изготовления белой масляной краски (цинковые белила), в медицине и косметике (для приготовления различных мазей); значительная часть получаемого оксида цинка используется в качестве наполнителя резины.
Гидроксид цинка Zn(OH)2 выпадает в виде белого осадка при действии щелочей на растворы солей цинка:
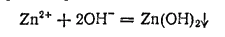
Осадок легко растворяется в кислотах с образованием солей цинка и в избытке щелочей с образованием цинкатов. Таким образом, гидроксид цинка — амфотерное соединение. Так, с NaOH протекает реакция:
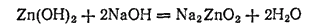
Как и в случае бериллатов (см. § 209), при образовании цинкатов происходит не только замещение водорода в Zn(OH)2 на металл, но и присоединение гидроксид-ионов. В частности, в твердом состоянии выделены гидроксоциикаты, отвечающие формулам Na2[Zn(OH)4], Ba2[Zn(OH)6].
Растворение металлического цинка в щелочах тоже сопровождается образованием гидроксоцинкатов, например:
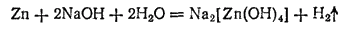
Гидроксид цинка растворяется также в водном растворе аммиака. При этом образуются комплексные ионы [Zn(OH)4]2+:
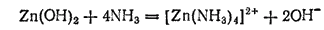
Zn(OH)2 — слабый электролит. Поэтому все соли цинка, в том числе и цинкаты, в водной среде гидролизуются.
Сульфат цинка ZnSO4. Из водного раствора выделяется в виде кристаллогидрата состава ZnSO4·7H2O и в таком виде называется цинковым купоросом. Применяется при крашении и ситцепечатании, при гальваническом цинковании (в качестве главного компонента электролита), в медицине, а также служит исходным веществом для получения других соединений цинка.
Хлорид цинка ZnCl2. Эту соль трудно получить в безводном состоянии. Обычно она содержит около 5% воды и основного хлорида. Раствор ZnCl2 применяется для травления металлов; при паянии он способствует удалению оксидов с поверхности металла в момент пайки.
- 604 -
Для этой же цели при пайке и сварке металлов применяется тетрахлорцинкат аммония (NH4)2[ZnCl4] (или ZnCl2·2NH4Cl).
Сульфид цинка ZnS. Это — один из немногих сульфидов, имеющих белый цвет. Сульфид цинка получается при действии сульфидов щелочных металлов или аммония на соли цинка:
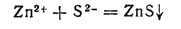
Сульфид цинка, а также оксид цинка входят в группу веществ, обладающих способностью люминесцировать — испускать холодное свечение в результате действия на них лучистой энергии или электронов. Явление люминесценции широко используется в науке и технике. Так, большое значение приобрел люминесцентный анализ, люминесцентные лампы применяются для освещения, люминесцентные экраны — важнейшая часть электронно-лучевых приборов.
Люминесцентный анализ основан на различном характере свечения разных веществ. Он дает возможность устанавливать присутствие очень малых количеств веществ в смесях, а также обнаруживать различия между предметами, которые в видимом свете представляются одинаковыми. С его помощью сортируют стекла, семена, обнаруживают микродефекты в металлических изделиях. Он применяется при поисках битумных и нефтяных месторождений, урановых руд. Люминесцентный анализ играет важную роль в судебной медицине и криминалистике, позволяя устанавливать природу различных пятен, обнаруживать фальсификацию документов и тайнопись. Чувствительность этого вида анализа очень велика. Кроме того, для его проведения не нужно разрушать анализируемое тело, что в некоторых случаях очень важно.
В люминесцентных лампах дневного света находящиеся в них пары ртути при прохождении электрического тока испускают ультрафиолетовое излучение, которое вызывает свечение веществ, покрывающих тонким слоем внутреннюю поверхность лампы. Эти вещества — люминофоры — можно подобрать так, чтобы их излучение по своему спектральному составу приближалось к дневному свету.
Огромное значение имеет применение люминофоров в различных электронно-лучевых приборах: катодных осциллографах, телевизорах и других. Экраны телевизора обычно изготовляют из сульфида цинка.
| <<< Назад 213. Стронций (Strontium). Барий (Barium). |
Вперед >>> 215. Кадмий (Cadmium). |
