Книга: Общая химия
92. Гидролиз солей.
| <<< Назад 91. Смещение ионных равновесий. |
Вперед >>> Глава IX. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ. ОСНОВЫ ЭЛЕКТРОХИМИИ |
92. Гидролиз солей.
Гидролизом* называется взаимодействие вещества с водой, при котором составные части вещества соединяются с составными частями воды. Примером гидролиза может служить взаимодействие хлорида фосфора(III) PCl3 с водой. В результате этой реакции образуются фосфористая кислота H3PO3 и соляная кислота:
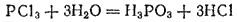
* Гидролиз в переводе означает "разложение водой"
Гидролизу подвержены соединения различных классов. В настоящем параграфе рассматривается один из важнейших его случаев — гидролиз солей.
Мы уже говорили, что в случае реакций нейтрализации, в которых участвуют слабые кислоты и основания, реакции протекают не до конца. Значит при этом в той или иной степени протекает и обратная реакция (взаимодействие соли с водой), приводящая к образованию кислоты и основания. Это и есть гидролиз соли.
В реакции гидролиза вступают соли, образованные слабой кислотой и слабым основанием, или слабой кислотой и сильным основанием, или слабым основанием и сильной кислотой. Соли, образованные сильной кислотой и сильным основанием, гидролизу не подвергаются; нейтрализация в этом случае сводится к процессу
H+ + OH- = H2O
а обратная реакция — диссоциация молекулы воды на ионы — протекает в ничтожно малой степени.
Рассмотрим гидролиз соли, образованной одноосновной кислотой и одновалентным металлом. В качестве примера возьмем ацетат натрия — соль слабой кислоты и сильного основания. Уравнение гидролиза этой соли имеет вид
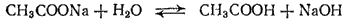
или в ионно-молекулярной форме:
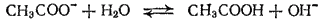
Уравнение показывает, что в данном случае гидролизу подвергается анион соли и что реакция сопровождается образованием ионов OH-. Но поскольку ионное произведение воды [H+][OH-] — величина постоянная, то при накоплении ионов OH- концентрация ионов водорода уменьшается. Следовательно, растворы солей, образованных слабой кислотой и сильным основанием, имеют щелочную реакцию.
- 250 -
Аналогично в случае соли, образованной слабым основанием и сильной кислотой, гидролизу подвергается катион соли и реакция сопровождается образованием ионов H+, например
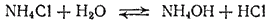
или
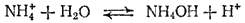
Накопление ионов H+ приводит к уменьшению концентрации ионов OH-. Таким образом, растворы солей, образованных слабым основанием и сильной кислотой, имеют кислую реакцию.
В рассмотренных случаях гидролизу подвергается не все количество находящейся в растворе соли, а только часть его. Иначе говоря, в растворе устанавливается равновесие между солью и образующими ее кислотой и основанием. Доля вещества, подвергающаяся гидролизу, — степень гидролиза — зависит от константы этого равновесия, а также от температуры и от концентрации соли.
Запишем уравнение гидролиза в общем виде. Пусть НА — кислота, МОН — основание, МА — образованная ими соль. Тогда уравнение гидролиза будет иметь вид:
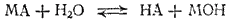
Этому равновесию отвечает константа:
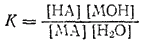
Концентрация воды в разбавленных растворах представляет собою практически постоянную величину. Обозначая
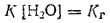
получим:

Величина Kr называется константой гидролиза соли. Ее значение характеризует способность данной соли подвергаться гидролизу; чем больше Kr, тем в большей степени (при одинаковых температуре и концентрации соли) протекает гидролиз.
Для случая соли, образованной слабой кислотой и сильным основанием, константа гидролиза связана с константой диссоциации кислоты Kкисл зависимостью:

Это уравнение показывает, что Kr тем больше, чем меньше Kкисл. Иными словами, чем слабее кислота, тем в большей степени подвергаются гидролизу ее соли.
- 251 -
Для солей, образованных слабым основанием и сильной кислотой, аналогичное соотношение связывает константу гидролиза о константой диссоциации основания Kосн:
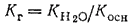
Поэтому, чем слабее основание, тем в большей степени подвергаются гидролизу образованные им соли.
Для солей, образованных слабой кислотой и слабым основанием, константа гидролиза связана с константами диссоциации кислоты и основания следующим соотношением:
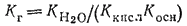
Соотношения, связывающие константу гидролиза с константами диссоциации кислоты и основания, легко получить из выражения константы гидролиза. Выведем первое из них, относящееся к случаю слабой кислоты и сильного основания. Для этого учтем, что основание МОН, от которого образована соль МА, — сильное, т. е. диссоциирует нацело. Поэтому
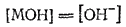
Сама соль также диссоциирует нацело. Следовательно:
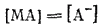
Концентрацию кислоты, пренебрегая диссоциированной ее частью, выразим через константу диссоциации кислоты Kкисл:
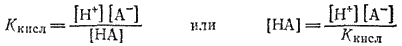
Подставляем найденные значения концентраций МОН, МА и НА в выражение константы гидролиза:
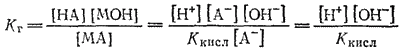
Учитывая, что [H+][OH-] ионное произведение воды, окончательно получим:
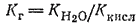
Степень гидролиза определяется природой соли, ее концентрацией и температурой. Природа соли проявляется в величине константы гидролиза. Зависимость от концентрации выражается в том, что с разбавлением раствора степень гидролиза увеличивается. В самом деле, пусть мы имеем, например, раствор цианида калия. В нем устанавливается равновесие
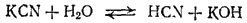
которому отвечает константа:

Разбавим раствор в 10 раз. В первый момент концентрации всех веществ — KCN, HCN и КОН — уменьшаются в 10 раз.
- 252 -
Вследствие этого числитель правой части уравнения константы гидролиза уменьшится в 100 раз, а знаменатель только в 10 раз. Но константа гидролиза, как всякая константа равновесия, не зависит от концентраций веществ. Поэтому равновесие в растворе нарушится. Для того чтобы оно вновь установилось, числитель дробя должен возрасти, а знаменатель — уменьшиться, т. е. некоторое количество соли должно дополнительно гидролизоваться. В результате этого концентрации HCN и КОН возрастут, а концентрация KCN — уменьшится. Таким образом, степень гидролиза соли увеличится.
Влияние температуры на степень гидролиза вытекает из принципа Ле Шателье. Все реакции нейтрализации протекают с выделением теплоты (§ 88), а гидролиз — с поглощением теплоты. Поскольку выход эндотермических реакций с ростом температуры увеличивается, то и степень гидролиза растет с повышением температуры.
Из сказанного ясно, что для ослабления гидролиза растворы следует хранить концентрированными и при низких температурах. Кроме того, подавлению гидролиза способствует падкисление (в случае солей, образованных сильной кислотой и слабым основанием) или подщелачивание (для солей, образованных сильным основанием и слабой кислотой) раствора.
Рассмотрим теперь гидролиз солей, образованных слабой многоосновной кислотой или слабым основанием многовалентного металла. Гидролиз таких солей протекает ступенчато. Так, первая ступень гидролиза карбоната натрия протекает согласно уравнению
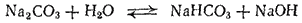
или в ионно-молекулярной форме:
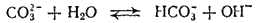
Образовавшаяся кислая соль в свою очередь подвергается гидролизу (вторая ступень гидролиза)
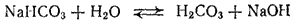
или
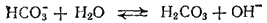
Как видно, при гидролизе по первой ступени образуется ион HCO3-, диссоциация которого характеризуется второй константой диссоциации угольной кислоты, а при гидролизе по второй ступени образуется угольная кислота, диссоциацию которой характеризует первая константа ее диссоциации. Поэтому константа гидролиза по первой ступени Kr, 1 связана со второй константой диссоциации кислоты, а константа гидролиза по второй ступени Kr, 2, — с первой константой диссоциации кислоты.
- 253 -
Эта связь выражается соотношениями:

Поскольку первая константа диссоциации кислоты всегда больше второй, то константа гидролиза по первой ступени всегда больше, чем константа гидролиза по второй ступени:
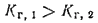
По этой причине гидролиз по первой ступени всегда протекает в большей степени, чем по второй. Кроме того, ионы, образующиеся при гидролизе по первой ступени (в рассмотренном примере — ионы OH-), способствуют смещению равновесия второй ступени влево, т. е. также подавляют гидролиз по второй ступени.
Аналогично проходит гидролиз солей, образованных слабым основанием многовалентного металла. Например, гидролиз хлорида меди(II) протекает по первой ступени с образованием хлорида гидроксомеди
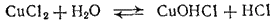
или в ионно-молекулярной форме:
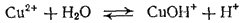
Гидролиз по второй ступени происходит в ничтожно малой степени:
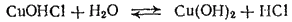
или
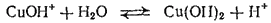
Особенно глубоко протекает гидролиз солей, образованных слабой кислотой и слабым основанием. Согласно вышеприведенному выражению, константа гидролиза в этом случае обратно пропорциональна произведению констант диссоциации кислоты и основания, т. е. ее значение особенно велико. Примером этого случая может служить гидролиз ацетата алюминия, протекающий до основных солей — ацетатов гидроксо- и дигидроксоалюминия:
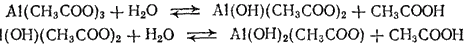
Рассмотрим для данного случая отдельно гидролиз катиона и гидролиз аниона. Эти процессы выражаются ионно-молекулярными уравнениями:
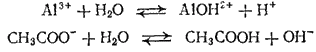
- 254 -
Итак, при гидролизе катиона образуются ионы H+, а при гидролизе аниона — ионы OH-. Эти ионы не могут в значительных концентрациях сосуществовать; они соединяются, образуя молекулы воды. Это приводит к смещению обоих равновесий вправо. Иначе говоря, гидролиз катиона и гидролиз аниона в этом случае усиливают друг друга.
Реакция растворов солей, образованных слабой кислотой и слабым основанием, зависит от соотношения констант диссоциации кислоты и основания, образующих соль. Если константа диссоциации кислоты больше константы диссоциации основания, то раствор имеет слабокислую реакцию, при обратном соотношении констант диссоциации — слабощелочную.
Если кислота и основание, образующие соль, не только слабые электролиты, но и малорастворимы или неустойчивы и разлагаются с образованием летучих продуктов, то гидролиз соли часто протекает необратимо, т. е. сопровождается полным разложением соли. Так, при взаимодействии в растворе соли алюминия, например AlCl3, с карбонатом натрия выпадает осадок гидроксида алюминия и выделяется диоксид углерода
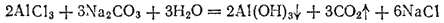
или
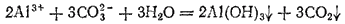
Кислые соли слабых кислот также подвергаются гидролизу. Однако здесь наряду с гидролизом происходит и диссоциация аниона кислой соли. Так, в растворе гидрокарбоната натрия одновременно протекают гидролиз иона HCOJ, приводящий к накоплению ионов OH-
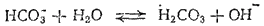
и диссоциация иона HCO3-, в результате которой образуются ионы H+:

Таким образом, реакция раствора кислой соли может быть как щелочной (если гидролиз аниона преобладает над его диссоциацией), так и кислой (в обратном случае). Это определяется соотношением константы гидролиза соли и соответствующей константы диссоциации кислоты. В рассмотренном примере константа гидролиза аниона превышает соответствующую константу диссоциации кислоты, поэтому раствор имеет слабо щелочную реакцию. При обратном соотношении (например, при гидролизе NaHSO3) реакция раствора кислая.
Протонная теория кислот и оснований рассматривает гидролиз как частный случай кислотно-основного равновесия: протон переходит от молекулы воды к данному иону или от данного иона к молекуле воды.
- 255 -
Например, гидролиз иона аммония можно выразить уравнением:
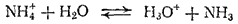
| <<< Назад 91. Смещение ионных равновесий. |
Вперед >>> Глава IX. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ. ОСНОВЫ ЭЛЕКТРОХИМИИ |
- 81. Особенности растворов солей, кислот и оснований.
- 82. Теория электролитической диссоциации.
- 83. Процесс диссоциации.
- 84. Степень диссоциации. Сила электролитов.
- 85. Константа диссоциации.
- 86. Сильные электролиты.
- 87. Свойства кислот, оснований и солей с точки зрения теории электролитической диссоциации.
- 88. Ионно-молекулярные уравнения.
- 89. Произведение растворимости.
- 90. Диссоциация воды. Водородный показатель.
- 91. Смещение ионных равновесий.
- 92. Гидролиз солей.
- 6.10. НЕОБРАТИМЫЙ ГИДРОЛИЗ ХЛОРИДА НАТРИЯ
- Микоплазмы – возбудители артритов
- Микрофлора полости рта
- 6.33. КАК РЖАВЕЕТ АЛЮМИНИЙ
- 151. Висмут (Bismuthum).
- 173. Сложные эфиры карбоновых кислот. Жиры.
- 174. Углеводы.
- 185. Кремнийорганические соединения.
- 110. Ионообменная адсорбция.
- Созданы из фторидов
- Применение висмута
- Родий глазами химика
