Книга: Общая химия
238. Физические свойства железа. Диаграмма состояния системы железо — углерод.
| <<< Назад 237. Значение железа и его сплавов в технике. Развитие металлургии в СССР. |
Вперед >>> 239. Производство чугуна и стали. |
238. Физические свойства железа. Диаграмма состояния системы железо — углерод.
В 30-х годах XIX века русский инженер П. П. Аносов впервые применил микроскоп для изучения структуры стали и ее изменения после ковки и термической обработки. В 30-х годах XIX века подобные исследования стали проводиться и за границей.
В 1868 г. Д. К. Чернов впервые указал на существование определенных температур («критических точек» ), зависящих от содержания углерода в стали и характеризующих превращения одной микроструктуры стали в другую. Этим было положено начало изучению диаграммы состояния Fe-C, а 1868 г. стал годом возникновения металловедения — науки о строении и свойствах металлов и сплавов. Французский исследователь Ф. Осмонд стал пользоваться только что изобретенным Ле Шателье пирометром и уточнил значения «критических точек». Он описал характер микроструктурных изменений, наблюдаемых при переходе через эти точки, и дал названия важнейшим структурам железоуглеродистых сплавов; эти названия употребляются до сих пор. С тех пор учеными различных стран было выполнено огромное количество работ, посвященных изучению сплавов железа с углеродом и диаграммы состояния системы Fe-C. Такого рода работы проводятся и в настоящее время. В них уточняются положения линий на диаграмме состояния в связи с применением более чистых веществ и более точных и современных методов.
Температура плавления железа равна 1539?5°C. Железо об разует две кристаллические модификации: ?-железо и ?-железо. Первая из них имеет кубическую объемноцентрированную решетку, вторая — кубическую гранецентрированную. ?-Железо термодинамически устойчиво в двух интервалах температур: ниже 912°C и от 1394°C до температуры плавления. Между 912 и 1394°C устойчиво ?-железо. Температурные интервалы устойчивости ? и ? железа обусловлены характером изменения энергии Гиббса обеих модификаций при изменении температуры (см. рис. 166).
- 653 -

Рис. 166. Температурная зависимость энергии Гиббса ? железа (G?) и ? -железа (G?).
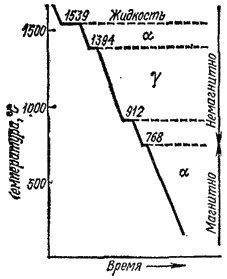
Рис. 167. Кривая охлаждения железа.
При температурах ниже 912 и выше 1394°C энергия Гиббса ?-железа меньше энергии Гиббса ?-железа, а в интервале 912-1394°C больше.
Температуры фазовых превращений железа хорошо видны на кривой охлаждения в виде остановок — горизонтальных площадок (см. рис. 167). Как видно, кроме площадок, отвечающих перечисленным точкам, на кривой охлаждения имеется еще одна остановка — при 768°C. Эта температура связана не с перестройкой решетки, а с изменением магнитных свойств ?-железа. При температурах выше 768°C железо немагнитно, а ниже 768°C — магнитно. Немагнитное ?-железо иногда называют ?-железом, а модификацию ?-железа, устойчивую при температурах от 1392°C до плавления, — ?-железом.
Железо — серебристый пластичный металл. Оно хорошо поддается ковке, прокатке и другим видам механической обработки. Механические свойства железа сильно зависят от его чистоты — от содержания в нем даже весьма малых количеств других элементов.
Твердое железо обладает способностью растворять в себе многие элементы. В частности, растворяется в железе и углерод. Его растворимость сильно зависит от кристаллической модификации железа и от температуры. В ?-железе углерод растворяется очень незначительно, в ?-железе — гораздо лучше. Раствор в ?-железе термодинамически устойчив в более широком интервале температур, чем чистое ?-железо. Твердый раствор углерода в ?-железе называется ферритом, твердый раствор углерода в ?-железе - аустенитом.
Содержанию в железе 6,67% (масс.) углерода отвечает химическое соединение — карбид железа, или цементит, Fe3C.
- 654 -
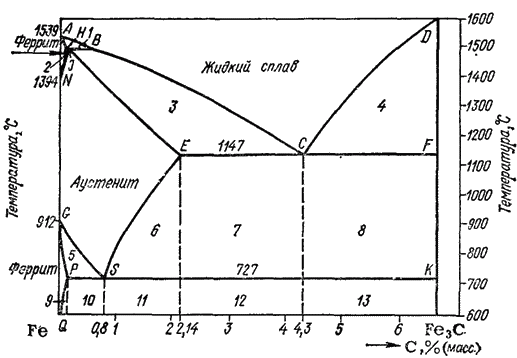
Рис. 168. Диаграмма состояния системы железо — углерод.
Это вещество имеет сложную кристаллическую структуру и характеризуется высокой твердостью (близка к твердости алмаза) и хрупкостью. При температуре около 1600°C цементит плавится.
Механические свойства феррита и аустенита зависят от содержания в них углерода. Однако при всех концентрациях углерода феррит и аустенит менее тверды и более пластичны, чем цементит.
Диаграмма состояния системы железо — углерод, дающая представление о строении железоуглеродных сплавов, имеет очень большое значение. С ее помощью можно объяснить зависимость свойств сталей и чугунов от содержания в них углерода и от термической обработки. Она служит основой при выборе железоуглеродных сплавов, обладающих теми или иными заданными свойствами. На рис. 168 приведена часть диаграммы состояния системы Fe-C, отвечающая содержанию углерода от 0 до 6.67%, или, что то же самое, от чистого железа до карбида Fe3C. Это самая важная часть диаграммы, поскольку практическое применение имеют сплавы железа, содержащие не более 5% углерода.
Диаграмма состояния системы Fe-C сложнее, чем рассмотренные в главе XVI основные типы диаграмм состояния металлических систем. Однако все ее точки, кривые и области подобны тем, которые были описаны в § 195. Особенности ее обусловлены уже упомянутыми обстоятельствами: существованием двух модификаций кристаллического железа, способностью обеих этих модификаций образовывать твердые растворы с углеродом, способностью железа вступать в химическое соединение с углеродом, образуй цементит.
- 655 -
Левая ось диаграммы соответствует чистому железу, правая — карбиду Fe3C(цементиту). Точки А и D показывают температуру плавления железа и карбида, точки G и N — температуры превращений ? и ?-железа друг в друга.
Линия ABCD — это кривая температур начала кристаллизации жидких сплавов, линия AHJECF — кривая температур начала плавления твердых сплавов. Все линии, лежащие ниже последней кривой, отвечают равновесиям между твердыми фазами.
Область, лежащая выше линии ABCD, отвечает жидкому сплаву. Области, примыкающие к левой вертикали, соответствуют твердым растворам углерода в железе: линия AHN ограничивает область твердого раствора углерода в ?-железе при высоких температурах (область высокотемпературного феррита), линия NJESG ограничивает область твердого раствора углерода в ?-железе (область аустенита), линия GPQ — область твердого раствора углерода в ?-железе при низких температурах (область низкотемпературного феррита). Перечисленным областям соответствуют гомогенные системы: структура как расплава, так и твердых растворов однородна в каждой из этих фаз.
Остальным областям диаграммы отвечают гетерогенные системы — смеси кристаллов двух фаз или кристаллов и расплава.
Рассмотрим важнейшие превращения, происходящие при медленном охлаждении расплавов различных концентраций. Это поможет нам разобраться в том, какие сплавы соответствуют областям гетерогенности диаграммы.
Пусть мы имеем расплав, содержащий 0.8% углерода. Его кристаллизация начнется в точке 1 (рис. 169). При охлаждении расплава до температуры, отвечающей этой точке, будут выпадать кристаллы аустенита; их состав отвечает точке 2. Расплав при этом обогащается углеродом, и его состав изменяется по линии ВС. Состав кристаллов в процессе кристаллизации изменяется по кривой JE. Когда состав кристаллов достигнет точки 3, кристаллизация закончится. Как всегда при образовании твердого раствора, одновременно идет процесс диффузии в твердой фазе, в результата чего при медленном охлаждении состав всех кристаллов получается одинаковым.
Далее, образовавшийся аустенит охлаждается без превращения до точки S (рис. 168). Эта точка (температура 727°C) показывает минимальную температуру устойчивого существования аустенита. При 272°C происходит его эвтектоидный распад. Образующийся эвтектоид состоит из чередующихся мелких пластинок феррита и цементита.
- 656 -
На изломе он при рассматривании под микроскопом напоминает перламутр. Поэтому эта структура — эвтектоидная смесь феррита и цементита — получила название перлит.
Если исходный расплав содержит не 0.8% углерода, а несколько меньше, например 0.7%, то образующийся при кристаллизации аустенит начнет распадаться не при 727°C, а при более высокой температуре (точка 1 на рис. 170). Превращение начнется с выделения кристаллов феррита (точка 2 на рис. 170), содержание углерода в котором очень мало. Вследствие этого остающийся аустенит обогащается углеродом и при дальнейшем охлаждении его состав изменяется по кривой GS. По достижении точки S начинается эвтектоидное превращение при постоянной температуре, по окончании которого сталь будет состоять из феррита и перлита. Из сказанного вытекает, что области 3 на диаграмме (см. рис. 168) соответствует смесь жидкого сплава с кристаллами аустенита, области 5 — смесь кристаллов феррита и аустенита и области 10 — смесь перлита с кристаллами феррита.
Если исходный расплав содержит более 0.8% углерода (но менее чем 2.14%), например 1.5%, то распад аустенита начнется с выделения цементита (точка 3 на рис. 170). Вследствие выделения Fe3C — фазы, богатой углеродом — остающийся аустенит обогащается железом, так что при дальнейшем охлаждении его состав изменяется по кривой ES. В точке S начинается выделение перлита. В итоге получается сталь со структурой, состоящей из цементита и перлита. Таким образом, области 6 на диаграмма (рис. 168) отвечает смесь кристаллов цементита и аустенита, а области 11 — смесь перлита с кристаллами цементита.
Обратимся теперь к сплавам, содержащим более 2.14% углерода. Первичная кристаллизация в этом случае заканчивается эвтектическим превращением при 1147°C, когда из расплава, содержащего 4,3% углерода (точка С на рис. 168), выделяется эвтектический сплав аустенита и цементита.
Если при этом исходить из расплава эвтектического состава (4.3% C), то кристаллизация начнется и закончится при одной и той же температуре 1147°C.

Рис. 169. Часть диаграммы состояния системы железо-углерод.
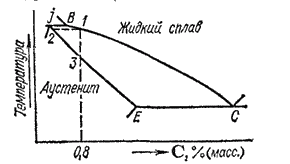
Рис.170. Часть диаграммы, состояния системы железо -углерод.
- 657 -
В случае сплавов, содержащих меньше 4.3% углерода (но больше 2.14%), образованию эвтектики будет предшествовать выделение аустенита. При содержании углерода выше 4.3% кристаллизация начнется с выделения цементита, но по достижении точки С на диаграмме также будет наблюдаться образование эвтектики. Таким образом, в результате кристаллизации жидких сплавов, содержащих более 2.14% углерода, первоначально получается структура, состоящая либо только из эвтектики, либо из эвтектики с кристаллами аустенита или цементита.
В то же время, как мы видели раньше, при кристаллизации жидких сплавов, содержащих меньше 2.14% углерода, первоначально получается аустенит. Это различие в структуре при высоких температурах создает различие в технологических и механических свойствах сплавов. Эвтектика делает сплавы нековкими, но ее низкая температура плавления облегчает применение высокоуглеродистых сплавов как литейных материалов. Железоуглеродные сплавы, содержащие меньше 2.14% углерода, называются сталями, а содержащие больше 2,14% углерода — чугунами.
Эта граница (2.14% углерода) относится к железоуглеродным сплавам, не содержащим других элементов. В присутствии третьего элемента вид диаграммы состояния изменяется, в частности границы устойчивости аустенита в некоторых случаях смещаются в сторону низких температур.
Закончим рассмотрение превращений, совершающихся в чугунах, при их охлаждении ниже 1147°C. При этой температуре растворимость углерода в ?-железе максимальна. Поэтому к моменту окончания первичной кристаллизации содержащейся в чугуне аустенит наиболее богат углеродом (2,14% ). При охлаждении ниже этой температуры растворимость углерода в аустените падает (кривая ES на рис. 168) и углерод выделяется из него, превращаясь обычно в цементит. По достижении температуры 727°C весь остающийся аустенит, в том числе входящий в состав эвтектики, превращается в перлит. Из сказанного следует, что области 7 отвечает смесь эвтектики с кристаллами аустенита и цементита, образовавшегося при распаде аустенита, области 8- смесь эвтектики с кристаллами цементита. Поскольку при температурах ниже 727°C аустенит эвтектики превращается в перлит, то областям 12 и 13, подобно области 11, отвечает смесь перлита и цементита. Однако сплавы, принадлежащие к той и другой области, несколько различаются по структуре. Это различие обусловлено тем, что цементит сплавов области 13 образуется при первичной кристаллизации, в области 12 — при распаде аустенита. Таким образом, при температурах ниже 727°C чугун состоит из цементита и перлита. Как мы увидим ниже (см. § 241), в некоторых случаях чугун может иметь и другую структуру.
Рассматривая превращения, происходящие при охлаждении расплавов различного состава, мы смогли выяснить, какие сплавы соответствуют различным областям диаграммы.
- 658 -
Но мы рассмотрели не все области диаграммы. Пользуясь тем же методом, нетрудно показать, какие сплавы отвечают остальным ее областям: области 1 соответствует смесь жидкого расплава и кристаллов высокотемпературного феррита, области 2 — смесь кристаллов высокотемпературного феррита и аустенита, области 4 — смесь жидкого сплава и кристаллов цементита, области 9 — смесь кристаллов феррита и цементита.
| <<< Назад 237. Значение железа и его сплавов в технике. Развитие металлургии в СССР. |
Вперед >>> 239. Производство чугуна и стали. |
- 233. Общая характеристика благородных газов.
- 234. Гелий (Helium).
- 235. Неон. Аргон.
- ПОБОЧНАЯ ПОДГРУППА ВОСЬМОЙ ГРУППЫ
- 236. Железо (Ferrum).
- 237. Значение железа и его сплавов в технике. Развитие металлургии в СССР.
- 238. Физические свойства железа. Диаграмма состояния системы железо — углерод.
- 239. Производство чугуна и стали.
- 240. Термическая обработка стали.
- 241. Сплавы железа.
- 242. Химические свойства железа. Соединения железа.
- 243. Кобальт (Cobaltum).
- 244. Никель (Niccolum).
- Платиновые металлы 245. Общая характеристика платиновых металлов.
- 246. Платина (Platinum).
- 247. Палладий (Palladium). Иридий (Iridium).
- 71. Диаграмма состояния воды.
- 237. Значение железа и его сплавов в технике. Развитие металлургии в СССР.
- Герцшпрунг, Расселл и диаграмма
- § 17. Физические свойства и химический состав Земли
- Климат и общие физические условия экваториального пояса
- 4.2. Физические характеристики, строение ядра
- § 13. Явления природы. Физические явления
- Физические поля как один из видов материи.
- § 27 Физические поля
- Физические характеристики волны.
- Физические свойства морской воды
- 1.3. Физические условия формирования биосферы
