Книга: Энергия жизни. От искры до фотосинтеза
Глава 5. ТЕПЛОВЫЕ ПОТОКИ
| <<< Назад Глава 4. ИЗМЕРЯЕМОЕ ТЕПЛО |
Вперед >>> Глава 6. ДВИЖУЩИЕСЯ ЧАСТИЦЫ |
Разделы на этой странице:
Глава 5.
ТЕПЛОВЫЕ ПОТОКИ
Принятие представления о сохранении энергии стало в некоторой степени фундаментальной переменой в системе взглядов человека на Вселенную, переменой, которая даже сейчас не полностью проникла в образ человеческой мысли. Люди всегда верили, что вера может двигать горами; что с помощью волшебной палочки или лампы Аладдина можно построить дворец во мгновение ока; что сапоги-скороходы могут за считаные минуты переносить своего владельца через леса и горы…
А теперь все эти картинки исчезают, стоит лишь задать простой вопрос: где взять на это энергию?
Если уж нам приходится разбить радужные мечты и настоять на том, что все сводится к балансу поступления и потери энергии, то давайте уж убедимся, что мы действительно имеем на это право. Иными словами, насколько мы можем быть уверены в действенности закона сохранения энергии? Можем ли мы доказать, что этот закон действительно существует?
Если честно — нет. По крайней мере, на данный момент. Убедительных причин, которые однозначно не позволяли бы создавать или уничтожать энергию, никто еще не сформулировал. Мы можем утверждать лишь, что ни в одном из тщательнейших наблюдений, ни в одном из самых разнообразных экспериментов, от Джоуля до наших дней, не было зафиксировано ни одного случая, когда энергия возникала бы ниоткуда или исчезала в никуда.
Пока не будет отмечен хоть один такой случай и пока на практике допущение, что закон сохранения энергии действует, приносит неоценимую пользу в неисчислимом количестве сфер деятельности, ученые от него не откажутся. Они не могут доказать существование этого закона, но уверены в нем, как мало в чем другом.
Лишь однажды глубокая убежденность в существовании закона сохранения энергии была поколеблена. Это произошло в 1896 году, когда было открыто явление радиоактивности. Именно тогда обнаружилось, что некоторые элементы, например уран, непрерывно производят энергию, казалось бы, ниоткуда.
Однако уже в 1905 году физик Альберт Эйнштейн опубликовал новую, в огромной степени фундаментальную, теорию строения Вселенной (ныне обычно именуемую «специальной теорией относительности»), где все прояснилось за счет того, что в расчет была включена и масса.
Дело в том, что масса сама по себе также представляет собой сохранное явление. Этот факт ученые с большим удивлением обнаружили только в конце XVIII века. Неискушенному наблюдателю кажется, что, например, горящая свечка постепенно тает и ее масса исчезает. А когда железо ржавеет — оно, наоборот, набирает вес, и это кажется примером «появления» массы. Такие выводы вполне возможно сделать, если упустить из виду переход твердого или жидкого вещества в газ или, в противоположном случае, поглощение газов из атмосферы.
В 1770-х годах французский химик Антуан Лоран Лавуазье возвел в систему применение количественных измерений к химическим экспериментам, и полученные им результаты быстро убедили прочих химиков в необходимости взвешивать и измерять все, что только можно взвесить и измерить. Проводя реакции горения и ржавления в замкнутых емкостях, Лавуазье доказал, что если учитывать массу газов, которые производятся в результате горения или поглощаются в результате ржавления, то каких-либо заметных изменений массы реагентов не происходит!
Таким образом был провозглашен «закон сохранения массы», гласящий, что масса может переходить из одной формы вещества в другую, но не может быть ни создана, ни уничтожена. Иными словами, общее количество массы во Вселенной всегда одинаково.
Законы сохранения массы и энергии формулируются схожим образом, и всю вторую половину XIX века эти два закона считали аналогичными, но независимыми друг от друга обобщениями.
И только Эйнштейн в 1905 году сумел показать, на основе немногих базовых принципов, что массу можно рассматривать как одну из форм энергии. По его теории выходило, что крайне малое количество массы соответствует весьма большому количеству энергии. Этот принцип выражен в знаменитой формуле Эйнштейна е = mс2, где е — это энергия, m — масса, а с — скорость света. Из этой формулы видно, что 1 грамм массы соответствует примерно 21 500 000 000 000 джоулей энергии.
Таким образом, энергия, высвобождаемая при проявлениях радиоактивности, перестала быть загадкой. Стало ясно, что она появляется за счет потерь массы, столь малых, что приборы того времени не могли их зафиксировать. С тех пор появились гораздо более точные приборы, и с их помощью теория Эйнштейна обрела документальное подтверждение.
Высвобождение энергии при взрыве атомных бомб и выработка ее в ядерных реакторах тоже происходит за счет потерь массы. Еще важнее, что таким же образом объясняется и способность Солнца на протяжении множества веков выплескивать в пространство энергию в огромных количествах. Этот вопрос очень интересовал Гельмгольца, и в итоге ученый пришел к предположению, что Солнце постепенно сжимается, таким образом, потенциальная энергия его уменьшается и переходит в тепло и свет. Такая картина не лишена логики, но если бы она соответствовала реальности, то в истории Солнечной системы пришлось бы предположить некоторые факты, которых быть не могло в принципе; астрономы эту теорию принимать отказались.
Когда же выяснилось, что солнечный водород можно превратить в гелий с некоторой потерей массы, а следовательно — с высвобождением большого количества энергии, то феномен солнечного излучения (равно как и феномен излучения звезд вообще) стало возможным объяснить исходя из закона сохранения энергии.
Сейчас уже понятно, что, говоря «энергия», мы включаем в это понятие и массу; чтобы это стало очевидным, зачастую говорят о «законе сохранения массы-энергии».
Таким образом открытие радиоактивности, сперва пошатнувшее закон сохранения энергии, в конечном итоге еще прочнее утвердило его в более стойком и незыблемом виде.
На самом деле практики интуитивно использовали этот принцип еще задолго до того, как физики сумели убедительно доказать его на экспериментальном материале. Еще в 1775 году Парижская академия наук отказалась рассматривать какие бы то ни было проекты устройств, о которых заявлялось, что они будут производить энергии больше, чем потреблять. Такое устройство, если бы его существование было возможным, могло бы производить работу и вместе с тем продолжать работать за счет энергии, производимой им же самим. Получился бы пресловутый «вечный двигатель». И сейчас Патентное бюро США не будет рассматривать вопрос о патентовании устройств, включающих в себя «вечный двигатель», если только податель заявки не предъявит действующую модель своего изобретения. Надо ли говорить, что такого ни разу до сих пор не произошло?
Закон сохранения энергии подвел черту, провозгласив, что ни одно устройство не может вырабатывать больше энергии, чем тратит, однако не исключил надежды на то, что можно хотя бы получать столько же энергии. Если уж нельзя ничего выиграть у природы, то, может быть, получится хотя бы остаться при своих?
Именно эта надежда стала основной движущей силой всех теоретических исследований начала XIX века, связанных с работой паровой машины. В массовом сознании принято недооценивать значение прогресса в области теории, необходимого для того, чтобы изобретатель мог представить работающий механизм. Сам Уатт опирался в своих разработках паровой машины на работы Блэка, посвященные латентному теплу, о которых говорилось в предыдущей главе. А кто из слышавших об изобретении Уатта знает, что оно стало возможным только благодаря теории Блэка?
Эффективность самых лучших машин Уатта, какими бы полезными и незаменимыми они ни были, не превышает 5 процентов. Это значит, что работы они могут производить только на 5 процентов от получаемой ими тепловой энергии. Поэтому казалось очевидным, что, и не нарушая закона сохранения энергии, можно добиться значительного повышения производительности. Даже учитывая неизбежность каких-то потерь на трение, теплопроводность и тому подобное, логично было предположить, что эффективность вполне возможно поднять до близкого к 100 процентам показателя.
Так считали до тех пор, пока французский физик Николя Леонар Сади Карно не принялся всерьез изучать движения тепловых потоков, основав таким образом науку термодинамику (что по-древнегречески и означает «движение тепла»).
В течение всего XIX века значение этой науки все более возрастало, поэтому к тому моменту, как был четко сформулирован закон сохранения энергии, по причине своей фундаментальной важности для всего, что касается перехода энергии в работу и обратно, он получил название «первый закон термодинамики».
Карно основал науку, но времени на то, чтобы внести в нее большой вклад, у него оставалось уже очень мало. Ученый умер в возрасте тридцати шести лет во время эпидемии холеры в Париже. Однако кое-что он все же успел. В возрасте двадцати восьми лет в 1824 году он опубликовал небольшую книжку под названием «Размышления о движущей силе огня», где привел описания своих опытов и собственные рассуждения о том, до какой степени тепло может быть преобразовано в работу. В этой книге Карно ясно показал, что даже при идеальных условиях (то есть при отсутствии трения и потерь энергии в направлении окружающей среды) лишь строго определенная доля тепловой энергии может преобразовываться в работу. Эта доля определялась разностью температур пара и конденсируемой воды по абсолютной шкале температур, выведенной с помощью закона Шарля. Если первую определить как T1 а вторую — как Т2, то наибольшая доля тепла, которую можно перевести в работу, определяется по формуле:
(T2 — T1)/ T2
Доля преобразуемого тепла, то есть, иными словами, эффективность системы, одинакова, независимо от того, какие именно вещества подвергаются нагреву и охлаждению, будь то вода, ртуть или что угодно; важна только его температура. Поэтому формула Карно справедлива для любой «тепловой машины», а не только для паровой.
Допустим, например, что в машине Уатта используется пар, нагретый до 100 °С (373 °К), а температура конденсируемой воды — 5 °С (278 °К). Тогда по формуле Карно получаем:
(373 — 278)/373 = 0,255.
Лишь примерно четверть, и не больше, производимой тепловой энергии может быть преобразована в работу, как бы идеально ни работала машина. Повысить эффективность помогло бы использование раскаленного пара (чтобы Т2 была побольше) или жидкости, имеющей более высокую температуру кипения и более низкую температуру плавления, чем вода. Пробовали и то и другое, но даже современные паровые машины не имеют эффективности выше, чем 0,25.
* * *
Формула Карно не только указала путь к тому, как можно увеличить эффективность паровой машины, но и привела к открытию одного крайне важного обобщения.
Если формула Карно верна, то получается, что машина, в которой горячая и холодная камера имеют одну и ту же температуру, никакой работы произвести не способна. Ведь в таком случае Т2 будет равна Т1 соответственно, формула Карно приобретет вид:
(T2 — T1)/ T2 = 0/ T2 = 0.
Например, представим себе энергию, содержащуюся в океанской воде, пусть даже в ледяной. Когда эта вода замерзает, каждый грамм ее отдает 80 калорий тепла (как показал в свое время Блэк, измеряя латентное тепло). Почему бы тогда, скажем, океанскому лайнеру не собирать это тепло и не использовать для работы своих двигателей? Вода возле лайнера остужалась бы, возможно, вплоть до замерзания, но общий объем воды в океанах, а значит и содержащегося в ней тепла, настолько огромен, что для обеспечения работы всех океанских лайнеров (да и вообще всех механизмов) в мире потребовалась бы крайне незначительная ее доля. К тому же и эту потерю быстро возмещало бы солнечное тепло.
Такое предположение никоим образом не нарушает первого закона термодинамики. Энергия в данной схеме не берется из ниоткуда — она просто переводится из одной формы (из тепла, содержащегося в океанской воде) в другую (кинетическую энергию вращающихся винтов), а переход энергии из одной формы в другую в первом законе термодинамики оговорен отдельно.
Однако ни одна схема такого рода не оказалась работоспособной. Так и не удалось разработать ни одного способа использовать тепловую энергию какого-либо вещества, температура которого была бы равномерной. Иными словами, общий опыт всего человечества свидетельствует о том, что формула Карно справедлива для любых условий, которые когда-либо были испытаны. Для того чтобы тепло можно было преобразовать в работу, где-то в системе должна существовать разность температур.
Лорд Кельвин объяснял это так: «Трансформация, в результате которой должно быть преобразовано в работу тепло, извлеченное из источника, имеющего однородную равномерно распределенную температуру, — невозможна».
Это — одна из формулировок утверждения, получившего название «второй закон термодинамики».
Этот второй закон не кажется таким очевидно неизбежным, как первый. С некоторым сожалением мы чувствуем себя вынужденными признать, что энергию нельзя создавать из ничего (первый закон), но почему же мы не можем использовать ту энергию, которая у нас есть? Пусть мы не можем получить выгоду, но можно же хотя бы остаться при своих?
Давайте рассмотрим этот момент на примере энергии движения, с которой мы имеем дело ежедневно. Должно быть, второй закон термодинамики станет несколько нагляднее, если рассмотреть его по аналогии с падающими телами.
Достигая земли, падающее тело может совершать работу. Оно может убить человека, расколоть орех или просто пробить дырку в земле, но в любом случае — это очевидная работа. Достигнув же поверхности, тело больше никакой работы совершать не способно, по крайней мере до тех пор, пока продолжает лежать неподвижно. Соответственно своей способностью совершить ту работу, которую оно совершило, это тело обязано тому факту, что оно переместилось из точки с большим потенциалом энергии (к примеру — с вершины километровой скалы) в точку с меньшим потенциалом (к подножию той же скалы).
Но и покоящееся на поверхности земли тело тоже обладает некоей энергией. Если под ним выкопать шахту в километр глубиной и сбросить его в эту шахту, то тело вновь сможет проделать работу, такую же как и когда падало со скалы. Это происходит потому, что вновь создана разность потенциалов.
То же самое происходит и в отношении тепла. Тепло, содержащееся в океанской воде, нельзя перевести в работу без помощи камеры, содержащей нечто более холодное или более теплое, чем океанская вода. Если выразиться логичнее, то можно сказать, что работу совершает не камень, а падение камня, не тепло, а тепловой поток.
Далее, как каждому известно на собственном опыте, падающие тела двигаются только в одном направлении — вниз. Если бы тело могло падать в обоих направлениях, то один и тот же предмет мог бы совершать бесконечную работу, просто двигаясь туда-сюда — то с вершины скалы в долину, то из долины на вершину скалы. Однако на самом деле предметы падают только из точки с высоким потенциалом энергии в точку с низким.
То же самое происходит и с другими формами энергии, и в частности с теплом. В 1850 году немецкий физик Рудольф Юлиус Эмануэль Клаузиус дал однозначную формулировку этого процесса, сказав, что при любом спонтанном процессе (то есть таком, который происходит сам по себе, без внешнего вмешательства) тепло всегда переходит от более горячего тела к более холодному и никогда — от более холодного к более горячему.
На самом деле мы все это прекрасно знаем и принимаем как должное, что чайник с водой над горящим газом в итоге закипит, а теплая вода — всегда растопит лед. То есть тот факт, что тепло будет переходить от более горячего тела к более холодному, а не наоборот, нам хорошо известен.
То же самое утверждение и является само собой разумеющимся для формулы Карно, поскольку если бы тепло не перетекало от более горячего тела к более холодному, то оно могло бы перетекать и внутри равномерно нагретого резервуара с водой от одной его части к другой, и из этого перетекания можно было бы получать работу. Таким образом, утверждение Клаузиуса — это одна из формулировок правила Карно—Кельвина о невозможности получения работы из равномерно нагретой системы, то есть одна из формулировок второго закона термодинамики.
Клаузиус не только сформулировал это утверждение по поводу тепловых потоков (суть которого известна нам по бытовому опыту и без каких-либо научных формулировок), но и увидел в нем повод для масштабного обобщения, которое можно распространить на все процессы, в которых используется энергия, при любых условиях и в любом месте Вселенной. По этой причине именно ему приписывают честь «открытия» второго закона термодинамики.
Это подводит нас к интересному моменту. Любой тепловой машине для преобразования тепла в работу требуется некоторое время. Ни одна из них не способна производить работу мгновенно. За время работы тепло перетекает из горячей камеры в окружающую среду (которая, как правило, сама по себе холоднее, чем горячая камера) и никогда — наоборот. Таким образом', горячая камера охлаждается, а холодная камера нагревается. Разность температур становится со временем все меньше и производит все меньше работы по сравнению с изначальной разностью температур[2].
Можно придумать тепловую машину, в которой и горячая и холодная камеры имели бы более высокую температуру, чем окружающая среда, но в этом случае горячая камера теряла бы тепло быстрее, чем холодная. Если же, наоборот, температура обеих камер будет ниже температуры окружающей среды, то горячая камера будет нагреваться медленнее холодной. И в том и в другом случае разность температур будет уменьшаться. На самом деле в любой системе, переводящей в любой форме энергию в работу, со временем разность потенциалов уменьшается, или, иначе говоря, часть потенциально выполнимой разностью потенциалов энергии работы остается невыполненной на практике из-за необходимости преодолевать трение или иные формы сопротивления естественному потоку энергии.
Клаузиус еще в 1875 году изобрел параметр, включающий в себя и неизбежно теряемую энергию, и абсолютную температуру, — параметр этот получил название «энтропия системы».
Можно, конечно, представлять себе совершенные тепловые машины, настолько хорошо изолированные, что тепло не будет ни перетекать в них извне, ни тратиться на нагревание окружающей среды, машины, в которых будут отсутствовать потери на трение, и так далее. При таких условиях выполняться будет вся работа, на которую способна заданная разность температур. Энергия будет тратиться полностью, без потерь. Однако в реальности и трение, и теплообмен с внешней средой всегда имеют место, а значит — и энергопотери, причем их объем будет увеличиваться со временем (рис. 4).
В свете теории Клаузиуса можно сказать: при любом спонтанном процессе энтропия либо остается неизменной (в идеальном случае), либо возрастает (в реальных случаях).
Однако забудем об идеале — приходится признать, что в реальном мире вокруг нас энтропия всегда увеличивается.
Поскольку все это — неизбежные последствия однонаправленности тепловых потоков, то существует еще один способ выражения второго закона термодинамики.
Строго говоря, отдавая должное законам термодинамики, мы всегда должны помнить о том, что эти законы применимы только к замкнутым системам — то есть к тем частям Вселенной, которые можно рассматривать как не испытывающие никакого влияния извне со стороны других ее частей. Если же рассматривать открытые системы, то часто может казаться, что законы термодинамики нарушаются.
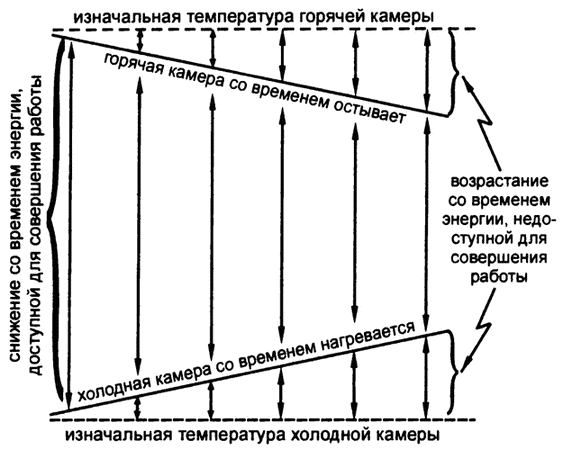
Рис. 4. Изменение количества доступной энергии со временем
Например, предположим, что вы ведете наблюдения за котелком с водой, стоящим на плите. Вы видите, что энергетическое содержание воды в котелке постепенно возрастает, пока вода не начнет кипеть и пока, наконец, вся не выкипит. Если рассматривать один лишь котелок с водой, вне его связей с плитой, то может показаться, что энергия, дерзко нарушая первый закон термодинамики, появилась из ниоткуда. Однако вы прекрасно понимаете, что это не так, поскольку под котелком находится горячая плита или газовый рожок. Если принять во внимание, что система складывается из обеих этих частей, то вопрос о том, почему на закипающий котелок не действует первый закон термодинамики, снимается сам собой.
Что касается второго закона термодинамики в отношении открытых систем, то представьте себе — тело действительно может подниматься с земли на высоту, а тепло — перетекать от более холодных тел к более горячим. В быту вы часто являетесь свидетелем подобных «феноменов», и если сосредоточить внимание только на поднимающемся теле или только на тепловом потоке, то вполне возможно сделать вывод о нарушении второго закона термодинамики.
Однако рассматривать систему надо в целом. Тело может подниматься с земли на крышу дома только тогда, когда оно находится, скажем, в лифте, движимом электрическим мотором. Тепло утекает из холодной камеры холодильника в более теплую окружающую среду тоже благодаря электрическому двигателю. Если включить в расчет двигатель и поток энергии внутри его, то вы увидите, что имеется и поток энергии в «правильном» направлении, причем превышающий по объему поток в «неправильном», действие которого мы видим как подъем тела или охлаждение камеры.
Другими словами, локальное уменьшение энтропии (являющееся результатом потока энергии в направлении, противоположном указанному вторым законом термодинамики) в одной из частей системы всегда более чем уравновешивается возрастанием энтропии в другой части системы. Если брать в расчет всю систему целиком, то общие изменения всегда происходят в направлении увеличения энтропии.
На самом деле, если мы имеем дело не с воображаемыми системами, существующими только в умах физиков-теоретиков, а с реальностью, то представить себе действительно замкнутую систему очень сложно. Внешняя среда всегда оказывает некоторое действие, которое необходимо учитывать.
Все вышеописанное справедливо и в отношении человеческого организма. Если его вдруг сделать замкнутой системой, лишенной энергообмена с окружающей средой, то он умрет в течение нескольких минут (ведь воздух — тоже часть окружающей среды). Направление естественных изменений в человеческом организме, сопровождающихся, как уже было сказано, возрастанием энтропии, ведет к смерти. Мы, конечно, живем, не умирая, иногда по целой сотне лет, но это происходит только потому, что наш организм является не замкнутой системой, а частью большей системы, в которую входят и воздух, которым мы дышим, и пища, которую мы едим. Сложность общего взаимодействия всех форм жизни и всей неодушевленной окружающей среды на планете, на которой мы живем, не позволяет считать замкнутой системой что-либо меньшее, чем всю Землю в целом.
Но и этого мало. Если бы Земля была замкнутой системой, то жизнь на ней очень быстро закончилась бы, поскольку поверхность планеты остыла бы, океаны — замерзли и так далее. Это тоже естественные изменения, соответствующие возрастанию энтропии. Этого не происходит только благодаря тому, что Земля является частью более крупной системы, в которую входит еще и Солнце, тепло которого и не дает Земле замерзнуть.
Даже Солнечная система не является полностью замкнутой. На нее действует сила притяжения со стороны других тел Галактики и много других не так ярко выраженных сил. Каждая часть Вселенной тем или иным образом влияет на остальные, и логично предположить, что на свете существует только одна действительно замкнутая система — это сама Вселенная. Если же рассматривать любую ее часть, то появляется вероятность того, что в этой отдельно взятой части энтропия может уменьшаться — за счет еще большего ее увеличения во всей остальной Вселенной.
Ясно, что если общее количество тепла во Вселенной ограниченно, а энтропия продолжает возрастать, то в конце концов она достигнет максимума, то есть такого состояния, что никакой разности температур не будет вообще. Вся энергия во Вселенной станет недоступной для совершения работы — все спонтанные процессы прекратятся и какие-либо изменения перестанут происходить вообще. Эта картина получила название «тепловая смерть Вселенной», и теория о тепловой смерти приобрела большую популярность во второй половине XIX века.
Теперь давайте вернемся к началу нашего повествования и посмотрим, можно ли выразить в терминах термодинамики то различие между живой и неживой материей, которое я высказал в первой главе. Я сказал, что живые существа могут совершать усилия, а неживые — нет.
Понятно, что «совершение усилия» подразумевает локальное уменьшение энтропии. Для того чтобы опустить висящий в воздухе камень вниз, усилия не требуется — его достаточно отпустить, и он упадет. А вот для того, чтобы поднять его вверх, усилие необходимо.
Сам по себе камень может двигаться только вниз, в том направлении, где усилия не нужно. Он не может совершить усилие, чтобы подняться наверх. С точки зрения термодинамики это будет звучать так: камень сам по себе может быть подвержен только увеличению энтропии, но не ее уменьшению.
Живой же организм способен совершать усилия по уменьшению энтропии по крайней мере на одном участке системы, частью которой он является (разумеется, за счет еще большего ее увеличения в других частях системы). Даже простейшие живые существа способны создавать локальное уменьшение энтропии, когда они прыгают, летят, лезут, идут, ползут или плывут вверх, против силы притяжения. Даже не сдвигающиеся с места организмы, например устрицы, тоже могут производить локальное уменьшение энтропии различными другими способами.
Удовлетворимся ли мы заявлением, что различие между живыми и неживыми организмами заключается в том, что живые организмы могут производить локальное уменьшение энтропии, а неживые — нет?
Что ж, выдвинув это утверждение, мы явно встали на верный путь, но, к сожалению, такого определения пока недостаточно. Солнечное тепло тоже может вызывать локальное уменьшение энтропии, когда выпаривает воду из океана, то есть поднимает в воздух огромные массы водяного пара. Силы, задействованные в геологических процессах, происходящих в земной коре, способны воздвигать горы в несколько миль высотой, что тоже подразумевает масштабное уменьшение энтропии. Однако ни Солнце, ни Земля не являются живыми ни в одном из смыслов, которые вкладывает в это понятие человек.
Надо еще поработать над нашим определением. Итак, продолжим.
| <<< Назад Глава 4. ИЗМЕРЯЕМОЕ ТЕПЛО |
Вперед >>> Глава 6. ДВИЖУЩИЕСЯ ЧАСТИЦЫ |
- Глава 1. УСИЛИЯ, КОТОРЫЕ МЫ СОВЕРШАЕМ
- Глава 2. ПЛОДЫ ОГНЯ
- Глава 3. ИЗМЕРЯЕМОЕ ДВИЖЕНИЕ
- Глава 4. ИЗМЕРЯЕМОЕ ТЕПЛО
- Глава 5. ТЕПЛОВЫЕ ПОТОКИ
- Глава 6. ДВИЖУЩИЕСЯ ЧАСТИЦЫ
- Глава 7. ЧАСТИЦЫ, УДЕРЖИВАЕМЫЕ ВМЕСТЕ
- Глава 8. ТЕПЛО И ХИМИЧЕСКИЕ РЕАКЦИИ
- Глава 9. НАПРАВЛЕНИЕ РЕАКЦИИ
- Глава 10. ЭЛЕКТРИЧЕСКИЙ ПУТЬ
- Глава 11. КАК ПОДТОЛКНУТЬ РЕАКЦИЮ
- Глава 12. СТИМУЛЯЦИЯ БЕЗ ПРИЛОЖЕНИЯ ЭНЕРГИИ
- 4.4. Тепловые колонки
- Тепловые источники света
- Глава шестая Тепловые явления
- Обморожения, тепловые и солнечные удары
- Глава 5. ТЕПЛОВЫЕ ПОТОКИ
- 4.3. Термики
- О том, что мы знаем пока на «тройку с минусом»
- Влияние топливно-энергетического комплекса на климат
- Инфракрасная астрономия
- Занимательные опыты и задачи по физике
- Часть шестая
- От чайного стакана к водомерной трубке
