Книга: Общая химия
221. Лантаноиды.
| <<< Назад 220. Подгруппа скандия. |
Вперед >>> 222. Актиноиды. |
221. Лантаноиды.
К семейству лантаноидов принадлежат четырнадцать f-элементов, следующих в периодической системе после лантана:
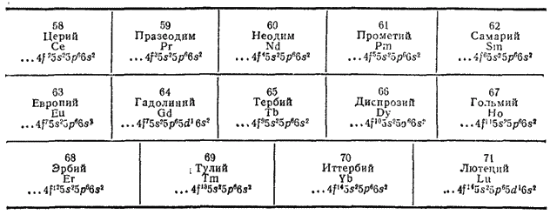
С возрастанием порядкового номера элементов этого семейства происходит заполнение электронами подуровня третьего снаружи электронного слоя ( 4f-подуровня), строение же наружного, а у большинства элементов и следующего за ним слоев остается неизменным. По этой причине все лантаноиды очень близки друг к другу по химическим свойствам.
Электроны заполняют 4f-, а не 5d-подуровень потому, что в этом случае они обладают меньшей энергией. Однако разница в энергиях 4f- и 5d-состояний очень мала. Благодаря этому один из 4f-электронов (а в некоторых случаях, например, у церия, два 4f-электрона) легко возбуждается, переходя на 5d-подуровень, и становится, таким образом, валентным электроном. Поэтому в большинстве своих соединений лантаноиды имеют степень окисленности +3, а не +2. Это обстоятельство объясняет близость свойств лантаноидов к свойствам элементов подгруппы скандия.
В § 34 говорилось, что в пределах одного периода с возрастанием порядкового номера размеры атомов элементов уменьшаются. Подобная закономерность наблюдается не только для элементов главных подгрупп, но, за немногими исключениями, и для элементов побочных подгрупп. Такое же уменьшение радиусов атомов имеет место и в случае лантаноидов (лантаноидное сжатие).
Это явление имеет одно важное следствие. В результате лантаноидного сжатия размеры атомов и иоиов элементов шестого периода, расположенных сразу после лантаноидов (Hf, Ta, W и далее), очень близки к размерам атомов и ионов соответствующих элементов пятого периода (Zr, Nb, Mo и т. д.); в то же время для элементов четвертого и пятого периодов эти характеристики заметно различаются (табл. 37).
- 622 -
Таблица 37. Радиусы атомов (в нм) некоторых элементов побочных подгрупп
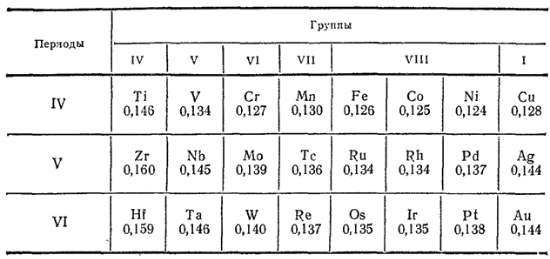
Благодаря тому, что атомы и ионы аналогичных элементов побочных подгрупп пятого и шестого периодов имеют не только сходное электронное строение, но и практически совпадающие размеры, в их химических свойствах наблюдается гораздо более близкое сходство, чем в случае элементов четвертого и пятого периодов. Так, цирконий по своим свойствам значительно ближе к гафнию, чем к титану, ниобий сходен с танталом в большей степени, чем с ванадием и т. д.
В свободном состоянии лантаноиды представляют собою типичные металлы, сходные с лантаном или с иттрием. Их оксиды нерастворимы в воде, но легко присоединяют воду с образонием гидроксидов. Последние лишь незначительно растворяются в воде и имеют основной характер. Соли лантаноидов по своей растворимости подобны соответствующим солям лантана или иттрия.
Прометий не имеет стабильных изотопов и в природе не обнаружен.
Вследствие очень большой близости химических свойств соединений лантаноидов, выделение их в чистом виде из природных смесей очень затруднено. Лишь в последние 20—30 лет разработаны эффективные методы разделения лантаноидов. В настоящее время все они получены в виде чистых металлов.
Многие лантаноиды и их соединения нашли применение в различных областях науки и техники. Они применяются в производстве стали, чугуна и сплавов цветных металлов. При этом используется главным образом мишметалл — сплав лантаноидов с преобладающим содержанием церия и лантана. Добавка малых количеств редкоземельных металлов повышает качество нержавеющих, быстрорежущих, жаропрочных сталей и чугуна. При введении 0,35% мишметалла в нихром срок его службы при 1000°C возрастает в 10 раз. Добавка лантаноидов к сплавам алюминия и магния увеличивает их прочность при высоких температурах.
- 623 -
Один из крупных потребителей редкоземельных металлов — стекольная промышленность. Стекло, содержащее церий, не тускнеет под действием радиоактивных излучений и применяется в атомной технике. Оксиды лантана и неодима входят в состав многих оптических стекол. Небольшие добавки оксидов лантаноидов используются для обесцвечивания стекол и для придания им окраски. Так, Nd2O3 придает стеклу ярко-красный цвет, а Pr2O3 - зеленый. Оксиды лантаноидов используются также для окраски фарфора, глазури, эмали.
Радиоактивный изотоп тулия 170Tm применяется для изготовления портативных генераторов рентгеновских лучей медицинского назначения
| <<< Назад 220. Подгруппа скандия. |
Вперед >>> 222. Актиноиды. |
