Книга: Происхождение жизни. От туманности до клетки
Разнообразие электрон-транспортных цепей
| <<< Назад Разнообразие и эволюция хинонов |
Вперед >>> Модульная структура окислительно-восстановительных ферментов |
Разнообразие электрон-транспортных цепей
В предыдущих главах мы познакомились с двумя самыми распространенными вариантами электрон-транспортных цепей, работающими в аэробном дыхании и в кислородном фотосинтезе. На самом деле разнообразие гораздо шире, потому что бактерии и археи используют множество разных окислителей и восстановителей (см. главу 16). Кроме упомянутых в прошлой главе окислителей (кислород, сульфат, нитрат, нитрит) разные бактерии могут использовать серу, хлорат, перхлорат, арсенат, селенат, растворенное трехвалентное железо (в кислой среде), твердые оксиды Fe2O3 и MnO2, хлорорганические соединения и другие вещества. В качестве восстановителей может использоваться такая экзотика, как фосфит, арсенит, соединения сурьмы и даже урана. Более того, существуют разные неродственные варианты ферментных комплексов для одной и той же реакции. Например, для окисления железа у разных микробов известно четыре разных ферментных системы. Описание всего этого разнообразия заняло бы целую книгу, поэтому мы ограничимся здесь разбором двух электрон-транспортных цепей: денитрификации и сульфатного дыхания/окисления серы. Первая интересна тем, что некоторые ее ферменты эволюционно родственны ферментам кислородного дыхания, а вторая, по-видимому, одна из древнейших.
В ходе денитрификации нитрат восстанавливается до азота в четыре стадии:
NO3- ? NO2- ? NO ? N2O ? N2.
Каждая из четырех реакций катализируется своим ферментом. Типичная дыхательная цепь денитрификации похожа на цепь, работающую в аэробном дыхании: в ее составе тоже есть комплекс I (НАДН-дегидрогеназа) и комплекс III (цитохромный комплекс bc1, в состав которого входят цитохромы b и с), между которыми электроны переносятся при помощи хинонов. Однако если аэробная дыхательная цепь линейна, то дыхательная цепь денитрификации разветвляется в двух местах. Хиноны в ней переносят электроны не только к цитохрому bc1, но и к нитрат-редуктазе, а после цитохрома bc1 подвижный малый цитохром с доставляет электроны по трем разным адресам: на нитрит-редуктазу, NO-редуктазу и N2O-редуктазу (рис. 17.5).
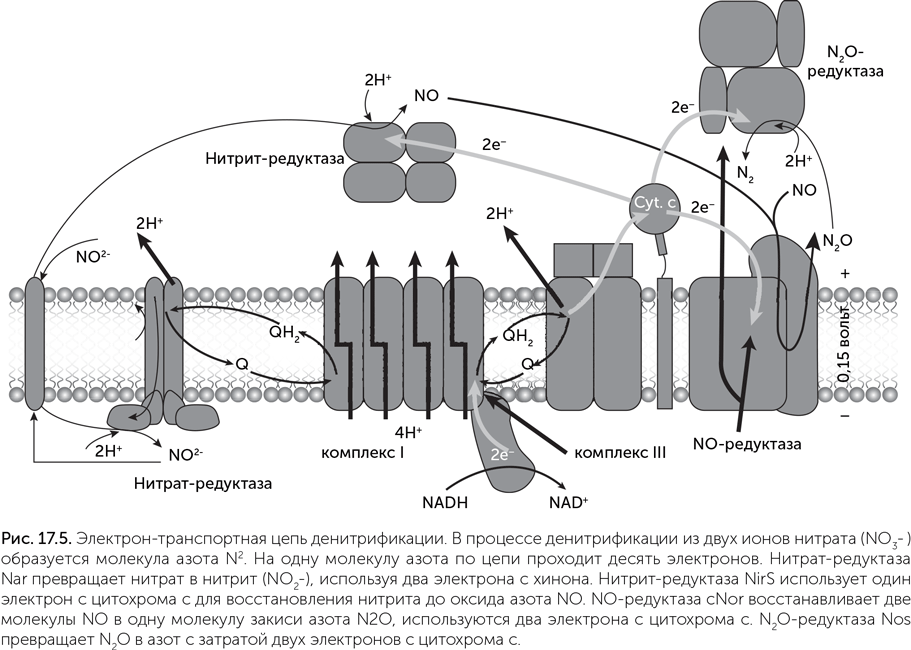
Из-за разветвления дыхательная цепь денитрификации нуждается в тонком управлении распределения тока. Например, нитрит-редуктаза производит ядовитый оксид азота NO. В норме его концентрация очень мала, потому что NO-редуктаза быстро превращает NO в безопасный N2O. Но если NO-редуктазе не хватит электронов, клетка отравит сама себя оксидом азота. Поэтому дыхательная цепь денитрификации качает меньше протонов, чем могла бы, – меньшая эффективность оказывается платой за безопасность. Кроме изображенного на рисунке варианта существуют более простые денитрификационные дыхательные цепи, в которых нет комплекса III, а все четыре редуктазы получают электроны прямо с хинона. Они проще в управлении, но переносят меньше протонов через мембрану.
Все известные варианты дыхательных цепей денитрификации, аммонификации и других окислительно-восстановительных превращений соединений азота используют компоненты, возникшие в эволюции после LUCA: цитохромы c и медьсодержащие ферменты. Медь входит в состав активного центра N2O-редуктазы и вспомогательных субъединиц NO-редуктазы. Так что их появление в эволюции, видимо, произошло уже после возникновения основных групп бактерий.
Восстановление сульфата, как и нитрата, происходит в несколько этапов. Поскольку сульфат – очень слабый окислитель, то он нуждается в активации с помощью АТФ. Сульфат превращается в аденозил-фосфосульфат, который далее восстанавливается до сульфита, серы и сероводорода:
SO42- ? аденозил-фосфо-SO4- ? SO32- ? S ? H2S.
Аденозил-фосфосульфат-редуктаза (Apr) получает электроны не от обычных переносчиков, а от белкового комплекса-партнера, который называется Qmo (рис. 17.6). Даже с учетом активации АТФ сульфат – слишком слабый окислитель, чтобы принимать электроны с хинона. Поэтому комплекс Qmo объединяет в один ток электроны из двух источников с разным напряжением: от хинона (слабый восстановитель) и от ферредоксина (сильный восстановитель). Благодаря этому Apr может восстановить сульфат до сульфита. Работа комплекса Qmo называется «электронная конфуркация».
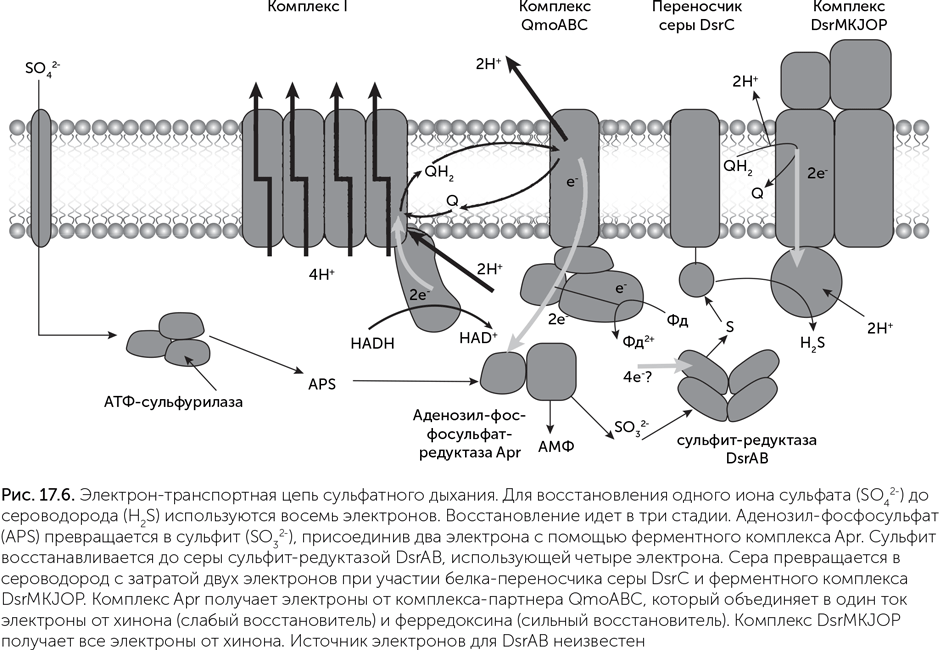
Дальше работает диссимиляторная сульфит-редуктаза (DsrAB), которая восстанавливает сульфит до серы, перенося четыре электрона. В клетках сера из активного центра сульфит-редуктазы выходит при помощи вспомогательного белка DsrC, молекула которого имеет длинную «ручку» с двумя остатками цистеина. Сера реагирует с этими цистеинами, превращаясь в H2S, а цистеины окисляются в дисульфидный мостик. Другой ферментный комплекс, гетеродисульфид-редуктаза (DsrMKJOP), восстанавливает этот дисульфидный мостик обратно, получая электроны с хинона. У многих бактерий эта система работает в обратном направлении, окисляя сероводород и серу до сульфита, например, в процессах фотосинтеза и диспропорционирования серы.
Комплексы сульфатного дыхания устроены достаточно однотипны у разных организмов, кроме того, сульфатное дыхание – признак нескольких древних, рано ответвляющихся групп архей и бактерий. Оно обходится без меди и обычно без цитохромов c. Субъединицы одного из его ферментов, сульфит-редуктазы DsrAB, судя по филогенетическому дереву, появились при дупликации генов еще до LUCA. Все это говорит о большой древности этого пути метаболизма.
| <<< Назад Разнообразие и эволюция хинонов |
Вперед >>> Модульная структура окислительно-восстановительных ферментов |
- Разнообразие и происхождение гемов, хлорофиллов и родственных коферментов
- Разнообразие и эволюция гем-содержащих белков
- Разнообразие и эволюция хинонов
- Разнообразие электрон-транспортных цепей
- Модульная структура окислительно-восстановительных ферментов
- Происхождение комплекса I (НАДН-хинон-оксидоредуктаза)
- Происхождение цитохромных комплексов bc1 (комплекс III) и b6f
- Происхождение цитохром-с-оксидазы
- Эволюция фотосистем
- Доступность окислителей и восстановителей на древней Земле
- Энергетика LUCA, первых бактерий и архей
- Разнообразие и эволюция хинонов
- Глава восьмая. Электрон в разреженном газе
- Глава 11 От Левенгука до электронного микроскопа
- § 74. Разнообразие биоценозов
- Электронный микроскоп и вирусы
- Решение транспортных проблем
- 1. Бесконечное разнообразие
- Атомные реакторы и электронные кристаллы
- § 37. Разнообразие растительного мира
- 7.3. Разнообразие экосистем (биогеоценозов). Саморазвитие и смена экосистем. Выявление причин устойчивости и смены экоси...
- Поразительное разнообразие геномов
- Диапазон сложности геномов, их функционального содержания и разнообразие геномной архитектуры вирусов
