Книга: Происхождение жизни. От туманности до клетки
Разнообразие и происхождение гемов, хлорофиллов и родственных коферментов
| <<< Назад Глава 17 Происхождение компонентов биоэнергетических систем |
Вперед >>> Разнообразие и эволюция гем-содержащих белков |
Разнообразие и происхождение гемов, хлорофиллов и родственных коферментов
Основной пигмент современного фотосинтеза – хлорофилл, как и основной компонент электрон-транспортных цепей, гем, относится к группе веществ, называемых порфиринами. Широкие плоские молекулы порфиринов, содержащие в центре атом какого-либо металла, легко могут окисляться и восстанавливаться, поглощать свет и проводить электроны от одной соседней молекулы к другой. Также они могут быть эффективными катализаторами химических реакций.
К порфиринам, кроме хлорофилла и обычных гемов (a и b), относятся некоторые другие молекулы, работающие в клетках, например гем d1 и сирогем. Последние по сравнению с обычным гемом имеют в своей структуре меньше двойных связей и больше боковых карбоксильных (СООН) групп. Сирогем входит в состав двух типов ферментов: сульфит-редуктаз и ассимиляторных нитрит-редуктаз. Оба этих класса ферментов проводят реакции восстановления с переносом в общей сложности до шести электронов, восстанавливая сульфит до сероводорода и нитрит до аммиака. Гем d1 входит в состав единственного фермента, диссимиляторной нитрит-редуктазы, которая восстанавливает нитрит до оксида азота, NO, с переносом одного электрона.
Более далекие родственники гемов – кофермент F430 и витамин В12. Кофермент F430 содержит никель и участвует в процессах метаногенеза. Ни у каких других организмов, кроме архей-метаногенов, он не встречается. Витамин В12 же есть почти у всех организмов, содержит кобальт и участвует в реакциях переноса метильных групп. Его строение несколько отличается от типичных порфиринов: в нем отсутствует один из метиленовых мостиков, соединяющих малые кольца в большое порфириновое кольцо. Вместо этого два малых кольца из четырех связаны напрямую; такие молекулы называются «коррины» (рис. 17.1).
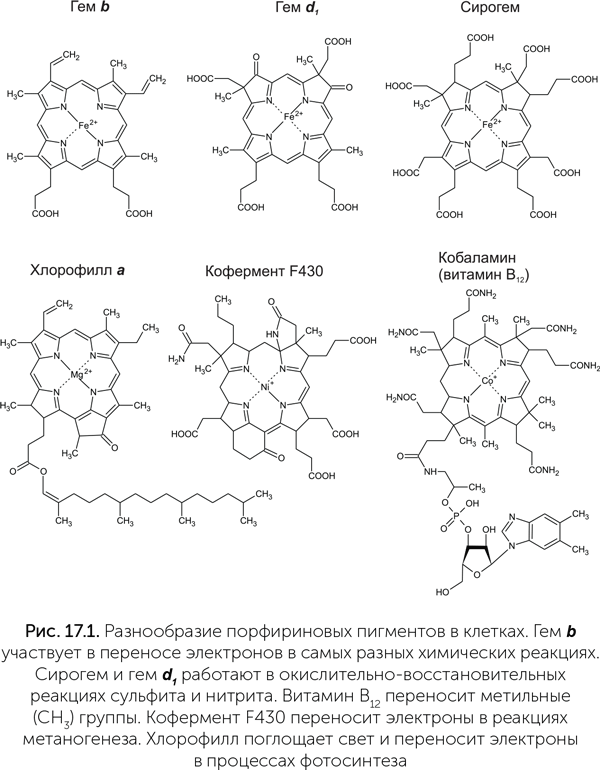
Синтез всех порфиринов и витамина В12 начинается одинаково (рис. 17.2). Глутаминовая кислота восстанавливается до альдегида, потом аминогруппа переносится на конец молекулы, и получается дельта-аминолевулиновая кислота. Две ее молекулы реагируют друг с другом, образуя порфобилиноген – вещество с пятичленным пиррольным кольцом в молекуле. Затем четыре молекулы порфобилиногена объединяются в цепочку (гидроксиметилбилан), которая замыкается в кольцо (уропорфириноген III). Отсюда пути синтеза разных порфиринов расходятся.
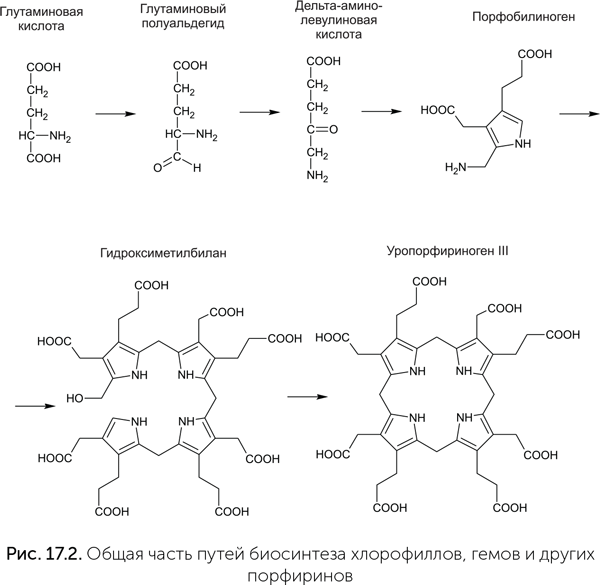
Известно несколько разных путей синтеза гемов и витамина В12 из уропорфириногена III. Их эволюционные отношения долго не удавалось распутать. Лишь недавно, с описанием всех ферментов и реакций пути синтеза витамина В12 у архей (Moore et al., 2013), удалось разобраться в этом разнообразии. Эти цепочки реакций делятся на две группы: аэробные (работающие в присутствии кислорода) и анаэробные. Их главное различие состоит в том, что в аэробных путях синтеза гема и В12 атом металла вставляется в молекулу на последней стадии, а в анаэробных – ближе к началу и участвует в последующих реакциях. Смысл этих различий, видимо, в том, что металлсодержащие промежуточные продукты в кислородной среде могут легко окисляться и быть источниками повреждающих активных форм кислорода.
Превращение уропорфириногена III в гемы и хлорофиллы сводится к восстановлению части двойных связей, вставке железа или магния и «обработке краев напильником» – отщеплению или укорочению боковых цепей. В аэробных путях синтеза порядок реакций с боковыми цепями может различаться в разных организмах (Dailey et al., 2015). У многих архей, а также у части анаэробных бактерий (сульфатвосстанавливающих, например Desulfovibrio, и некоторых денитрифицирующих) обнаружен, по-видимому, древнейший путь синтеза гема (Bali et al., 2011). Гемы b и d1 у них образуются из сирогема, причем на всех стадиях превращений атом железа остается в центре молекулы. По-видимому, это означает, что и в эволюции сирогем был предшественником этих гемов (рис. 17.3).
| <<< Назад Глава 17 Происхождение компонентов биоэнергетических систем |
Вперед >>> Разнообразие и эволюция гем-содержащих белков |
- Разнообразие и происхождение гемов, хлорофиллов и родственных коферментов
- Разнообразие и эволюция гем-содержащих белков
- Разнообразие и эволюция хинонов
- Разнообразие электрон-транспортных цепей
- Модульная структура окислительно-восстановительных ферментов
- Происхождение комплекса I (НАДН-хинон-оксидоредуктаза)
- Происхождение цитохромных комплексов bc1 (комплекс III) и b6f
- Происхождение цитохром-с-оксидазы
- Эволюция фотосистем
- Доступность окислителей и восстановителей на древней Земле
- Энергетика LUCA, первых бактерий и архей
- Разнообразие и эволюция гем-содержащих белков
- Происхождение Рюриковичей: ДНК-генеалогия доказывает
- Происхождение растений
- Глава 7. Происхождение человека и половой отбор
- 2. ПРОИСХОЖДЕНИЕ ВОДОРОСЛЕЙ
- 3. ПРОИСХОЖДЕНИЕ ГРИБОВ
- 4. ПРОИСХОЖДЕНИЕ ЖЕНСКОГО ГАМЕТОФИТА ЦВЕТКОВЫХ РАСТЕНИЙ
- 3. ПРОИСХОЖДЕНИЕ СТЕБЛЯ
- 6. ПРОИСХОЖДЕНИЕ ПАПОРОТНИКООБРАЗНЫХ РАСТЕНИИ
- 8. ПРОИСХОЖДЕНИЕ ЦВЕТКОВЫХ РАСТЕНИЙ
- 4. ВЫХОД РАСТЕНИЙ НА СУШУ И ПРОИСХОЖДЕНИЕ НАЗЕМНОЙ РАСТИТЕЛЬНОСТИ
- 9. ПРОИСХОЖДЕНИЕ КУЛЬТУРНЫХ РАСТЕНИЙ
