Книга: Общая химия
121. Соединения галогенов с водородом.
| <<< Назад 120. Получение и применение галогенов. |
Вперед >>> 122. Кислородсодержащие соединения галогенов. |
121. Соединения галогенов с водородом.
Из соединений галогенов наиболее важное практическое значение имеют галогеноводороды и соли галогеноводородов.
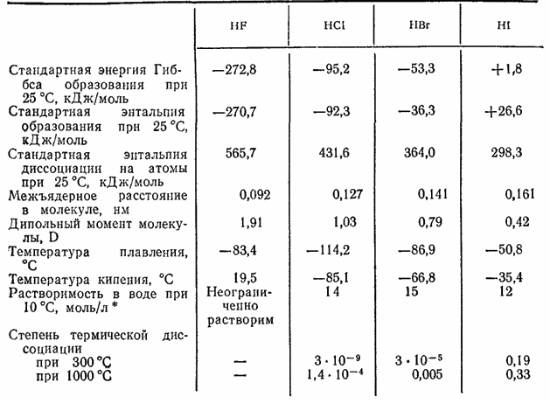
Химическая связь в молекулах галогеноводородов — полярная ковалентная: общая электронная пара смещена к атому галогена как более электроотрицательному. Некоторые свойства галогеноводородов приведены в табл. 24.
Прочность химической связи в молекулах галогеноводородов закономерно падает в ряду HF-HCl-HBr-HI: это проявляется в изменений энтальпии диссоциации молекул на атомы (табл. 24). Связь здесь ослабляется по тем же причинам, которые были рассмотрены при сопоставлении прочности молекул свободных галогенов (см. § 118). Как показывает схема (рис. 107), при переходе, например, от HF к HI уменьшается степень перекрывания электронных облаков атомов водорода и галогена, а область перекрывания располагается на большем расстоянии от ядра атома галогена и сильнее экранируется возросшим числом промежуточных электронных слоев. Кроме того, в ряду F—Cl—Br—I электроотрицательность атома галогена уменьшается. Поэтому в молекуле HF электронное облако атома водорода смещается в сторону атома галогена в наибольшей степени, а в молекулах HCl, HBr и HI все меньше и меньше. Это также приводит к уменьшению перекрывания взаимодействующих электронных облаков и, тем самым, к ослаблению связи между атомами.
С уменьшением прочности связи в молекулах галогеноводородов падает и их устойчивость к нагреванию. Термическая диссоциация фтороводорода происходит лишь при очень высоких температурах (более 3500°C), тогда как иодоводород уже при 300°C значительной степени распадается на иод и водород:
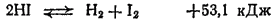
Все галогеноводороды — бесцветные газы с резким запахом.
- 348 -
Таблица 24. Некоторые свойства галогеноводородов
Галогеноводороды очень хорошо растворимы в воде. При 0°C один объем воды растворяет около 500 объемов HCl, 600 объемов HBr и около 425 объемов HI (при 10°C); фтороводород смешивается с водой в любых соотношениях.
Растворение галогеноводородов сопровождается их диссоциацией по кислотному типу, причем только фтороводород диссоциирован сравнительно слабо, остальные же принадлежат к числу наиболее сильных кислот.
На воздухе концентрированные растворы галогеноводородов дымят вследствие выделения галогеноводородов, образующих с водяными парами воздуха туман, который состоит из мелких капелек соответствующих кислот.

Рис. 107. Схема перекрывания электронных облаков при образовании молекул HF и НI. Пунктиром условно показано смещение электронного облака атома водорода в сторону атома галогена.
- 349 -
В ряду HI-HBr-HCl температуры кипения и плавления изменяются весьма закономерно (табл. 24), тогда как при переходе к HF они резко возрастают. Как уже говорилось в § 47, это обусловлено ассоциацией молекул фтороводорода в результате возникновения между ними водородных связей. Как показывает определение плотности пара, вблизи температуры кипения газообразный фтороводород состоит из агрегатов, имеющих средний состав (HF)4. При дальнейшем нагревании эти агрегаты постепенно распадаются, причем лишь около 90°C газообразный HF состоит из простых молекул.
При растворении в воде молекулы фтороводорода диссоциируют с образованием ионов H+ и F- . При этом частично разрываются водородные связи, так что диссоциация HF на ионы требует значительной затраты энергии. Поэтому фтороводород диссоциирует в водных растворах в значительно меньшей степени, чем другие галогеноводороды, константа диссоциации фтороводорода равна 7·10-4 так что по силе эта кислота лишь ненамного превосходит уксусную.
Образовавшиеся при диссоциации HF ионы F- в значительной степени связываются с недиссоциированными молекулами HF, причем образуется HF2-, в котором атомы фтора связаны друг с другом водородной связью:
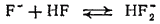
Поэтому при нейтрализации фтороводорода сначала образуются кислые соли, например, KHF2.
Отрицательные ионы галогеноводородов, за исключением фторид-иона, обладают восстановительными свойствами, возрастающими по ряду Cl-, Br-, I-.
Хлорид-ион окисляется фтором, перманганатом калия, диоксидом марганца и другими сильными окислителями, например:
16HCl + 2KMnO4 = 5Cl2 + 2KCl + 2MnCl2 +8H2O
Еще легче окисляются бромид- и, в особенности, иодид-ионы. Последние также легко окисляются бромом, нитратами, солями Fe(III), например:
2FeCl3 +2HI = 2FeCl2 + I2 + 2HCl
Поскольку галогенид-ионы обладают восстановительными свойствами, то при действии галогеноводородов на металлы последние могут окисляться лишь ионами водорода H+. Поэтому галогеноводороды могут реагировать в растворе только с металлами, стоящими в ряду напряжений до водорода.
Раствор фтороводорода в воде называется плавиковой кислотой. Это название происходит от плавикового шпата, из которого обычно получают фтороводород действием концентрированной серной кислоты:
- 350 -
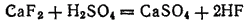
Продажный раствор фтороводорода содержит обычно 40% HF. Фтороводород реагирует с большинством металлов. Однако во многих случаях образующаяся соль малорастворима, вследствие чего на поверхности металла образуется защитная пленка. Так ведет себя, в частности, свинец, что и позволяет использовать его для изготовления аппаратуры, устойчивой к действию HF.
Соли фтороводорода называются фторидами. Большинство их малорастворимы в воде; хорошо растворимы лишь фториды Na, К, Al, Sn и Ag. Все соли плавиковой кислоты ядовиты.
Замечательным свойством фтороводорода и плавиковой кислоты является их способность взаимодействовать с диоксидом кремния SiO2, входящим в состав стекла; в результате образуется газообразный фторид кремния SiF4:
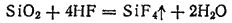
В растворе плавиковой кислоты выделения фторида кремния не происходит, так как он взаимодействует с молекулами HF с образованием хорошо растворимой комплексной гексафторокремниевой (кремнефтороводородной) кислоты:
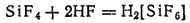
На взаимодействии HF с диоксидом кремния основано применение плавиковой кислоты для вытравливания на стекле различных меток, надписей и рисунков.
Ввиду того, что фтороводород разрушает стекло, в лаборатории его хранят в сосудах из специальных сортов пластмасс. Его можно хранить также в сосудах из свинца или в стеклянных сосудах, покрытых изнутри слоем парафина.
Применение фтороводорода довольно разнообразно. Безводный HF используют, главным образом, при органических синтезах, а плавиковую кислоту — при получении фторидов, травлении стекла, удалении песка с металлических отливок, при анализах минералов.
Пары фтороводорода очень ядовиты. Попадая на кожу, концентрированная плавиковая кислота вызывает тяжелые ожоги.
Соляная кислота получается растворением в воде хлороводорода. В настоящее время основным способом промышленного получения хлороводорода является синтез его из водорода и хлора:
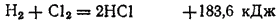
Этот процесс осуществляют в специальных установках, в которых смесь водорода и хлора непрерывно образуется и тут же сгорает ровным пламенем. Тем самым достигается спокойное (без взрыва) протекание реакции.
- 351 -
Исходным сырьем для получения хдороводорода служат хлор и водород, образующиеся при электролизе раствора NaCl(§ 197).
Большие количества HCl получают также в качестве побочного продукта хлорирования органических соединений согласно схеме

где R — органический радикал.
Соляная кислота — бесцветная жидкость с резким запахом. Обычно концентрированная соляная кислота содержит около 37% HCl, плотность ее 1,19 г/см2.
Прежний «сульфатный» метод получения HCl, применяемый в настоящее время только в лабораторной практике, основан на взаимодействии NaCl и концентрированной H2SO4 согласно уравнениям:
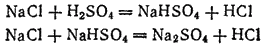
Первая из этих реакций протекает в значительной степени уже при слабом нагревании; вторая осуществляется лишь при более высоких температурах. В качестве побочного продукта получается сульфат натрия Na2SO4.
При нагревании концентрированной соляной кислоты вначале улетучивается хлороводород с небольшим количеством воды. Это происходит до тех пор, пока в остатке не получится 20.2%-ный раствор; последний перегоняется уже без изменения состава при постоянной температуре 110°C. Наоборот, если нагревать разбавленную HCl, то отгоняется преимущественно вода. Когда концентрация HCl в остатке достигает 20,2 %, жидкость начинает перегоняться без изменения состава, как и в предыдущем случае. Подобные растворы, характеризующиеся одинаковым составом жидкости и насыщенного пара и поэтому перегоняющиеся без изменения состава, называются постояннокипящимв или азеотропными растворами.
Подобно другим сильным кислотам, HCl энергично взаимодействует со многими металлами и оксидами металлов. Соли ее называются хлоридами. Большинство их хорошо растворимы в воде. Малорастворимы AgCl, PbCl2, CuCl, Hg2Cl2.
Соляная кислота — одна из важнейших кислот в химической практике. Ежегодное мировое производство соляной кислоты исчисляется миллионами тонн. Широкое применение находят также многие ее соли. Отметим важнейшие из хлоридов.
Хлорид натрия NaCl, или поваренная соль, служит сырьем для получения хлора, соляной кислоты, едкого натра и карбоната натрия (соды), применяется в красильном деле, в мыловарении и во многих других производствах. Он служит также приправой к пище и применяется в качестве средства, предохраняющего пищевые продукты от порчи.
Хлорид калия KCl в больших количествах потребляется сельским хозяйством в качестве удобрения.
- 352 -
Хлорид кальция CaCl2·6H2O употребляется для приготовления охлаждающих смесей. Безводный CaCl2 широко применяют в лабораторной практике для осушения газов и обезвоживания жидких органических веществ.
Хлорид ртути(II) HgCl2, или сулема, очень сильный яд. Разбавленные растворы сулемы (1:1000) используются в медицине как сильнодействующее дезинфицирующее средство (см. также стр. 607).
Хлорид серебра AgCl — наименее растворимая соль соляной кислоты. Образование осадка AgCl при взаимодействии ионов Cl- с ионами Ag+ служит характерной реакцией на хлорид-ионы. Хлорид серебра применяют в фотографической промышленности при изготовлении светочувствительных материалов.
Бромоводород и иодоводород очень похожи по своим свойствам на хлороводород, но отличаются более выраженными восстановительными свойствами. Молекулярный кислород постепенно окисляет иодоводород уже при комнатной температуре, причем под действием света реакция сильно ускоряется:
4HI + O2 = 2I2 +2H2O
Бромоводород взаимодействует с кислородом гораздо медленнее, в то время как при обычных условиях соляная кислота вовсе с ним не взаимодействует.
Восстановительные свойства бромоводорода и иодоводорода заметно проявляются и при взаимодействии с концентрированной серной кислотой. При этом HBr восстанавливает H2SO4 до SO2:
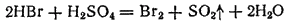
а HI — до свободной серы или даже до H2S:
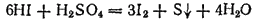
или
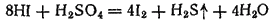
Поэтому HBr трудно, a HI практически невозможно получить действием серной кислоты на бромиды или иодиды. Обычно эти галогеноводороды получают действием воды на соединения брома и иода с фосфором — PBr3 и PI3. Последние подвергаются при этом полному гидролизу, образуя фосфористую кислоту и соответствующий галогеноводород:
PBr3 + 3H2O = H3PO3 + 3HBr
PI3 + 3H2O = H3PO3 + 3HI
Раствор иодоводорода (вплоть до 50%-ной концентрации) можно получить, пропуская H2S в водную суспензию иода. Реакция идет согласно схеме:
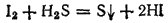
- 353 -
Соли бромоводорода и иодоводорода называются соответственно бромидами и йодидами. Растворимость бромидов и иодидов в большинстве случаев подобна растворимости соответствующих хлоридов.
Растворы бромидов натрия и калия под химически неправильным названием «бром» применяются в медицине как успокаивающее средство при расстройствах нервной системы. Бромид серебра в больших количествах идет на изготовление фотоматериалов. Иодид калия применяют в медицине — в частности, при заболеваниях эндокринной системы.
| <<< Назад 120. Получение и применение галогенов. |
Вперед >>> 122. Кислородсодержащие соединения галогенов. |
- § 58 Соединения, необходимые для существования жизни: белки, липиды
- § 56 Высокомолекулярные соединения
- § 57 Соединения, необходимые для существования жизни: нуклеиновые кислоты, полисахариды
- § 55 Циклические органические соединения
- Органические соединения в космосе
- 910. Почему не следует сбрасывать в океан азотистые и фосфатные соединения, а также органические вещества?
- 3.2. Комплексные соединения и живое вещество
- 2.35. АВГУСТ КЕКУЛЕ, БЕНЗОЛЬНОЕ КОЛЬЦО И АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- Глава XVIII. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- 119. Химические свойства галогенов.
- 242. Химические свойства железа. Соединения железа.
- 134. Соединения серы с галогенами.
