Книга: Общая химия
120. Получение и применение галогенов.
| <<< Назад 119. Химические свойства галогенов. |
Вперед >>> 121. Соединения галогенов с водородом. |
120. Получение и применение галогенов.
В природных соединениях галогены содержатся (за редким исключением) в виде отрицательно заряженных ионов, поэтому почти все способы получения свободных галогенов сводятся к окислению их ионов. Это осуществляется или при помощи окислителей, или действием электрического тока.
Фтор, вследствие своей высокой электроотрицательности, может быть выделен из соединений только путем электролиза. Впервые он был получен в 1886 г. путем разложения электрическим током смеси безводного жидкого фтороводорода с KF. Этот метод применяется в настоящее время для промышленного получения фтора. Расплав состава KF+2HF (температура плавления 70°C) подвергают электролизу. Электролиз ведут в никелевом сосуде, который является катодом, а анодом служит уголь. Катодное и анодное пространства разделены диафрагмой для предотвращения взрыва при смешивании продуктов электролиза — водорода и фтора.
Хлор получают в настоящее время в больших количествах путем электролиза водных растворов хлоридов натрия или калия. Хлор выделяется у анода, а у катода образуется соответственно гидроксид натрия или калия (см. § 197).
В лабораториях хлор получают действием различных окислителей на соляную кислоту. Напомним, например, известный из школьного курса лабораторный способ получения хлора действием диоксида марганца на соляную кислоту:
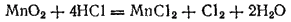
В ионно-молекулярной форме эта реакция выразится уравнением
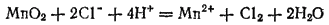
из которого видно, что здесь происходит окисление ионов Cl- в атомы хлора (образующие затем молекулы Cl2) и восстановление марганца, входящего в состав MnO2, до степени окисленности +2 (ионы Mn2+ ). При помощи этой реакции хлор был впервые получен К. В. Шееле (Швеция) в 1774 г.
- 346 -
Аналогично можно получить хлор из соляной кислоты, действуя на нее такими окислителями, как PbO2, KClO3, KMnO4.
Кислород в обычных условиях не взаимодействует с HCl в сколько-нибудь заметной степени. Но если пропускать HCl и O2 через трубку, нагретую до 400 содержащую кусочки пемзы, на которых распределен в качестве катализатора хлорид меди(II) CuCl2, то происходит окисление хлороводорода кислородом
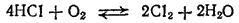
причем выход хлора достигает 80%. Этой реакцией раньше пользовались для промышленного получения хлора.
Бром и иод могут быть получены аналогично хлору окислением HBr и HI различными окислителями. В промышленности их обычно получают из бромидов или иодидов, действуя на их растворы хлором. Таким образом, получение брома и иода тоже основано на окислении их ионов, причем в качестве окислителя применяется хлор.
В СССР бром добывают главным образом из подземных буровых вод, а также из «рапы» (насыщенного раствора) некоторых соляных озер. Главным источником получения иода в СССР служат подземные буровые воды.
Галогены, особенно хлор, широко применяются в химической промышленности.
Фтор используют для получения некоторых ценных фторопроизводных углеводородов, обладающих уникальными свойствами, как, например, смазочных веществ, выдерживающих высокую температуру, пластической массы, стойкой к химическим реагентам (тефлон), жидкостей для холодильных машин (фреонов, или хладонов).
Хлор служит для приготовления многочисленных неорганических и органических соединений. Его применяют в производстве соляной кислоты, хлорной извести, гипохлоритов и хлоратов и др. Большое количество хлора используется для отбелки тканей и целлюлозы, идущей на изготовление бумаги. Хлор применяют также для стерилизации питьевой воды и обеззараживания сточных вод. В цветной металлургии его используют для хлорирования руд, которое является одной из стадий получения некоторых металлов.
Особенно большое значение приобрели за последнее время различные хлорорганические продукты. Хлорсодержащие органические растворители — например, дихлорэтан, четыреххлористый углерод — широко применяются для экстракции жиров и обезжиривания металлов. Некоторые хлорорганические продукты служат эффективными средствами борьбы с вредителями сельскохозяйственных культур. На основе хлорорганических продуктов изготовляют различные пластические массы, синтетические волокна, каучуки, заменители кожи (павинол).
С развитием техники область применения хлорорганических продуктов расширяется; это ведет к непрерывному увеличению производства хлора.
Широкое использование хлора в различных отраслях народного хозяйства, а также масштабы его производства и потребления позволяют отнести хлор, наряду с серной кислотой, аммиаком и содой, к числу важнейших продуктов, выпускаемых химической промышленностью.
Бром необходим для выработки различных лекарственных веществ, некоторых красителей, а также бромида серебра, потребляемого при производстве фотоматериалов.
Иод применяют в медицине в виде так называемой йодной тинктуры (10% раствор иода в этиловом спирте), превосходного антисептического и кровоостанавливающего средства. Кроме того, иод входит в состав ряда фармацевтических препаратов.
| <<< Назад 119. Химические свойства галогенов. |
Вперед >>> 121. Соединения галогенов с водородом. |
- Применение бамбука
- Глава 6. Самое главное применение
- § 53 Соли и их применение
- Получение и использование синтетических полимеров
- Применение солей.
- Глава 7 Получение нуклеотидов из продуктов атмосферной фотохимии
- Получение нуклеотидов
- Глава 21 По ту сторону физики Получение знания, имеющего смысл, но неизмеримого экспериментально…
- Применение рентгеновских лучей
- Применение коронного разряда
- Практическое применение фагов
- Получение кристаллов с определенными свойствами
