Книга: Происхождение жизни. От туманности до клетки
Альтернативные варианты биохимии на древней Земле. Ксенонуклеиновые кислоты
| <<< Назад Альтернативная биохимия на тех же элементах |
Вперед >>> Треозонуклеиновые и гликоленуклеиновые кислоты |
Альтернативные варианты биохимии на древней Земле. Ксенонуклеиновые кислоты
Мир РНК, который мы рассматривали в предыдущих главах, тоже является альтернативным вариантом биохимии по сравнению с современной земной жизнью. В самом деле, мир РНК не использует белки, которые стали важнейшей и неотъемлемой частью современной биохимии. Однако РНК не очень устойчива, а ее получение полностью абиогенным путем (без участия каких-то ферментов белковой, РНК или другой природы) очень сложно и наталкивается на много препятствий, часть которых была преодолена совсем недавно, а другие остаются актуальными до сих пор.
Многие ученые пошли дальше и предположили, что миру РНК тоже предшествовала какая-то другая, более простая жизнь, использующая другие молекулы. Эти предшественники РНК должны были легче получаться абиогенно и обладать большей устойчивостью по сравнению с РНК. Чтобы хранить генетическую информацию и со временем уступить место РНК, эти молекулы должны были содержать те же азотистые основания, что и РНК, или хотя бы совместимые с ними по комплементарным парам, а остов этих молекул должен допускать их соединение с РНК в двойную спираль, состоящую из двух химически различных цепей (такая конструкция называется «гетеродуплекс»). Молекулы, удовлетворяющие этим требованиям, получили название «ксенонуклеиновые кислоты».
В разделе «Пребиотическая химия альтернативных нуклеиновых кислот» (Cleaves II and Bada, 2012) сборника «Бытие – что было в начале» (Genesis – In the Beginning) собрана информация о свойствах различных ксенонуклеиновых кислот и об их возможных образованиях на древней Земле. Идеи о замене азотистых оснований, хотя и высказывались, но не получили широкого распространения. Во-первых, стандартные азотистые основания легко и с высоким выходом получаются абиогенно (из синильной кислоты или из формамида) и достаточно устойчивы для накопления. Во-вторых, альтернативные азотистые основания, как правило, несовместимы со стандартными, а для тех, что совместимы, сложно найти какие-то преимущества по сравнению с обычным набором. В-третьих, высокая устойчивость к ультрафиолету (см. главу 6) уникальна для стандартных оснований и не встречается ни у каких их аналогов.
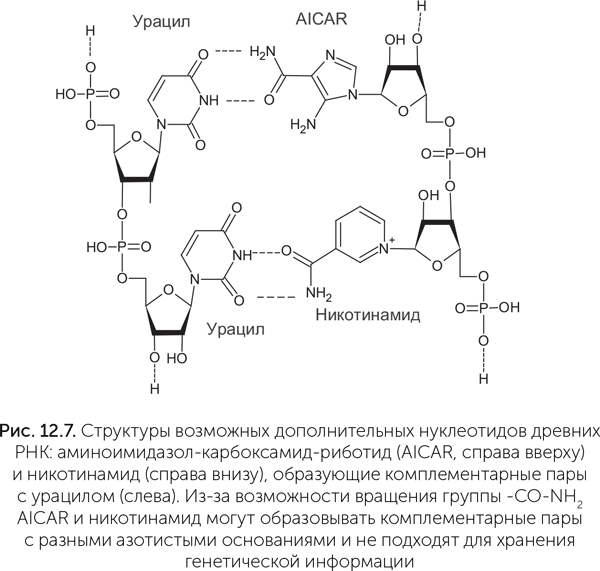
По этим причинам сейчас серьезно обсуждаются только два варианта расширения (не замены) набора азотистых оснований. Первым таким кандидатом в древние азотистые основания РНК является никотинамид, производное витамина РР, входящий в состав кофермента НАД. Как обсуждалось в главе 10, никотинамид в НАД связан с рибозой и фосфатом как обычное азотистое основание и придает рибозимам новые полезные свойства. В составе генетической молекулы никотинамид может замещать гуанин, образуя пару с цитозином (Liu and Orgel, 1995). Другое возможное дополнение к набору азотистых оснований – группа предшественников аденина и гуанина. Это прежде всего аминоимидазол-карбоксамид-риботид (AICAR), который получается как промежуточный продукт в ходе их синтеза. Эта молекула содержит пятичленное имидазольное кольцо с двумя атомами азота (рис. 12.7) и в составе РНК образует комплементарную пару с аденином (Bernhardt, Sandwick, 2014). AICAR является предшественником не только пуринов, но и важной аминокислоты – гистидина. Чаще всех других аминокислот гистидин встречается в активных центрах ферментов, и AICAR, сходный с ним по строению, мог выполнять аналогичные функции в древних рибозимах. AICAR образуется в небольших количествах при нагревании и облучении формамида, наряду со стандартными азотистыми основаниями. Иначе говоря, расширение набора азотистых оснований имеет смысл для улучшения каталитических свойств РНК, но при этом для хранения наследственной информации стандартный набор А, Г, Ц, У, по-видимому, лучший из всех веществ, которые были доступны на древней Земле.
Почему для хранения наследственной информации используются четыре вида азотистых оснований, а не два, шесть или восемь? Как мы помним из главы 6, синтетические азотистые основания позволяют расширить алфавит ДНК до шести букв. Более того, получены синтетические основания, образующие пару только сами с собой, и с ними можно получить алфавит с нечетным числом знаков, например, три или пять. Возможно, дело в устойчивости к ультрафиолету: в природе только четыре основания оснований оказались устойчивыми. Но почему природа не ограничилась двухбуквенным алфавитом?
Как обсуждается в обзоре Эёша Шатмари (Szathmary, 2003), двухбуквенный алфавит можно копировать более точно, чем четырехбуквенный. Четыре азотистых основания отличаются двумя параметрами: размером (A и Г большие, Ц и T маленькие) и положением водородных связей. Размер – более важное различие. Замены основания на другое такого же размера (A на Г или Ц на T) в геномах большинства организмов происходят от двух до пяти раз чаще, чем замены с изменением размера. Синтез четырех нуклеотидов требует больше ферментов, чем двух. Для точного копирования ДНК концентрации всех нуклеотидов в клетке должны быть по возможности равными. Поддерживать равные концентрации четырех нуклеотидов сложнее, чем двух. Получается, что для основной современной функции ДНК – хранения информации о последовательности белков – четырехнуклеотидный алфавит подходит хуже, чем двухнуклеотидный.
Четырехнуклеотидный алфавит оказывается лучше, чем все прочие, когда дело доходит до образования шпилечной структуры РНК. Математическое моделирование показывает, что РНК-подобная молекула с двумя типами оснований, как правило, имеет множество вариантов сворачивания в различные шпилечные структуры. Для РНК с четырьмя типами оснований обычно есть одна или две устойчивые структуры (Valba et al., 2012). Эксперименты с созданием рибозимов из РНК с ограниченным выбором нуклеотидов (три или даже два из четырех) это подтверждают: при меньшем разнообразии звеньев рибозимы возникают с меньшей вероятностью, и их эффективность ниже, чем у четырехнуклеотидных аналогов (Reader and Joyce, 2002).
| <<< Назад Альтернативная биохимия на тех же элементах |
Вперед >>> Треозонуклеиновые и гликоленуклеиновые кислоты |
- Определение жизни
- Химические свойства биомолекул, которые важны для их функции
- Выбор химических элементов
- Альтернативная биохимия на тех же элементах
- Альтернативные варианты биохимии на древней Земле. Ксенонуклеиновые кислоты
- Треозонуклеиновые и гликоленуклеиновые кислоты
- Пептидо-нуклеиновые кислоты
- Жизнь без полимеров
- Треозонуклеиновые и гликоленуклеиновые кислоты
- Глава 11 Альтернативные человечества
- Бактерии, вырабатывающие аминокислоты
- …и другие варианты
- Древнейшие следы жизни
- Г. Ш. Асылгараева К вопросу о формах животноводческой деятельности булгаро-татарского населения (на примере древней Каза...
- 9. Органические вещества. Нуклеиновые кислоты
- 2.3.4.Нуклеиновые кислоты
- § 52 Строение и свойства неорганических веществ. Кислоты и основания
- Философы Древней Греции
- Сложные неорганические вещества: кислоты и основания.
- 2.6. Органические вещества. Нуклеиновые кислоты
