Книга: Энергия жизни. От искры до фотосинтеза
Глава 19. ДЛЯ ЧЕГО ЖЕ ОНИ НУЖНЫ?
| <<< Назад Глава 18. КАК РАБОТАЮТ ФЕРМЕНТЫ |
Вперед >>> Глава 20. ЖИЗНЬ БЕЗ ВОЗДУХА |
Разделы на этой странице:
Глава 19.
ДЛЯ ЧЕГО ЖЕ ОНИ НУЖНЫ?
Теперь, после того, как мы подробно выяснили, почему присутствие ферментов в ящерице и их отсутствие в камне так важно, разумно поинтересоваться: какие же именно химические реакции катализируют ферменты, если уж эти реакции являются отличительным признаком живой материи?
На самом деле еще задолго до того, как было достигнуто сколь бы то ни было серьезное понимание природы ферментов и подробностей их функционирования, химики уже проявляли интерес к химическим реакциям жизни. В конце концов, суть происходящей реакции можно уловить и не зная подробностей ее осуществления, подставив вместо них уклончивое «ну, как-то чем-то катализируется, наверное».
Как уже говорилось в главе 14, все химические реакции, происходящие в процессе жизнедеятельности, именуются одним емким словом «метаболизм», или «обмен веществ».
Обратите внимание, что я определил метаболизм как химические изменения, происходящие «в процессе жизнедеятельности», а не «внутри живой ткани»! Это очень важно, потому что существует ряд химических реакций, происходящих вне живой ткани, и тем не менее крайне важных для нее.
Я имею в виду пищеварение. Когда вы глотаете пищу, она движется вниз по пищеводу, попадая оттуда в желудок, а затем — в кишечник. В ходе этого процесса она претерпевает существенные изменения, и то, что в итоге выбрасывается через анус, принципиально отличается от того, что было поглощено через рот. Во время нахождения в пищеварительном канале (общее название для всей системы труб от рта до ануса; см. рис. 40) пища не находится внутри организма в строгом смысле. Она продолжает оставаться частичкой внешнего мира, зажатой между ртом и анусом. Различные железы, от крупных вроде печени и поджелудочной до многочисленных мелких, выделяют в пищеварительный канал свои соки. Соки эти перемешиваются с перемолотой пищей, и содержащиеся в них ферменты катализируют все те реакции обмена веществ, которые мы называем общим словом «пищеварение».
Именно благодаря тому, что реакции пищеварения происходят вне самого организма, они первыми и попали в поле зрения ученых (как об этом говорилось в главе 15). Пищеварительные соки можно извлечь из канала с помощью трубок, не нанося обследуемому никакого вреда, кроме легкого неудобства, а затем тщательно изучить их действие на пищу в лабораторных условиях. Нет причин полагать, что в пробирке и в пищеварительном канале одна и та же реакция будет проходить по-разному, ведь и в том и в другом случае она проходит вне самого организма.
Счастливый случай для великого дела изучения процессов пищеварения произошел в 1822 году, когда американскому хирургу по имени Уильям Бомон попался уникальный больной — Алекс Сен-Мартин, канадский путешественник, получивший в результате огнестрельного ранения необычную травму — не-зарастающее отверстие в животе (фистулу), ведущее прямо в желудок. Бомон получил, таким образом, возможность в течение десяти лет непосредственно наблюдать, как желудок вырабатывает свои пищеварительные соки и какое воздействие они оказывают на различную пищу при тех или иных обстоятельствах. В 1833 году Бомон опубликовал результаты своих наблюдений, и физиологи пришли в полный ажиотаж.
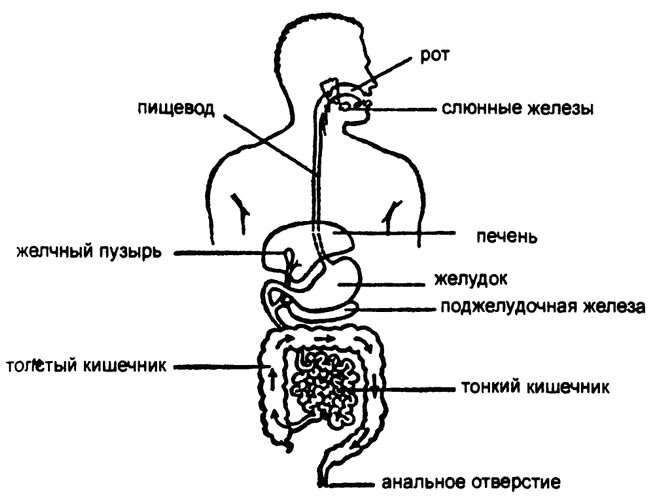
Рис. 40. Пищеварительный канал
Такие больные, как Сен-Мартин, встречаются крайне редко, и сотворить такое с человеком специально — дело немыслимое. Поэтому физиологам 40-х годов XIX века по всей Европе пришлось выбрать максимально приближенный к этому вариант — они стали создавать искусственные фистулы у собак, и изучение процессов пищеварения приобрело массовый характер.
С помощью таких методов исследования в XIX веке был собран достаточно полный свод представлений о биохимии пищеварения, и хотя это было знание только о «внешних рубежах» метаболизма, для начала получилось очень неплохо.
В целом была собрана следующая информация: по мере продвижения пищи по пищеварительному каналу она подвергается воздействию одного за другим различных соков, каждый из которых содержит свойственный только ему набор ферментов — по конвейерному принципу. Давайте рассмотрим этот процесс на примере углеводов.
Основные углеводы, содержащиеся в нашей пище, — это целлюлоза, крахмал, сахароза и лактоза. Целлюлозу организм человека расщеплять не умеет, и она выходит с фекалиями практически в нетронутом виде. А вот крахмал начинает распадаться на более мелкие части, именуемые декстринами, уже под воздействием фермента, присутствующего в слюне, птиалина.
Но птиалин не может обрабатывать пищу долго — еда проглатывается и опускается в желудок, кислотное содержимое которого быстро разрушает птиалин. Однако как только пища из желудка попадает в тонкий кишечник, там она снова подвергается действию уже другой амилазы (так называются все ферменты, катализирующие процесс распада крахмала, в том числе и птиалин), слегка щелочной, производимой поджелудочной железой. Здесь процесс распада крахмала продолжается — медленно, но непрерывно. Крахмал продолжает распадаться на декстрины, а декстрины — на более мелкие, пока не получатся фрагменты, состоящие всего из двух молекул глюкозы. Они называются мальтозой.
Дальше в пищеварительном тракте пища подвергается обработке другими пищеварительными соками, содержащими, в частности, фермент «мальтазу», катализирующую распад мальтозы на отдельные молекулы глюкозы.
Есть в пищеварительных соках и такие ферменты, как «сахараза» и «лактаза», катализирующие расщепление, соответственно, сахарозы на глюкозу и фруктозу и лактозы на глюкозу и галактозу. Таким образом, посредством скоординированной деятельности ферментов расщепляемые углеводы из исходной пищи превращаются в простые вещества с шестью атомами углерода — глюкозу (в основном), фруктозу и галактозу.
Жиры попадают в ежовую рукавицу жирорасщепляющих ферментов («липаз»), одной из которых является желудочный сок, ферментативная деятельность которого, впрочем, не очень активна ввиду его высокой кислотности, и сок поджелудочной железы, который как раз очень активен в этом отношении. Сок печени (желчь) не содержит ферментов, зато содержит определенные вещества (соли желчных кислот), которые облегчают перемешивание жиров с водянистыми пищеварительными соками, а значит, и сам процесс их переваривания. К тому времени, когда жиры достигают нижней части тонкого кишечника, они уже разложены на глицерин (трехуглеродный спирт) и жирные кислоты (длинные углеводные цепочки с карбоксильной группой на конце).
Белкам, как и следовало ожидать, предстоит самая сложная обработка. Пепсин, содержащийся в желудочном соке, чувствует себя в кислотной среде как дома — это редкий случай среди ферментов, его активность вне кислотной среды невозможна. Он катализирует процесс распада определенных пептидных связей, а соляная кислота желудочного сока катализирует распад всех пептидных связей без исключения. Трипсин и химотрипсин сока поджелудочной железы тоже являются расщепляющими белок ферментами («протеазами»), и их черед наступает, когда пища покидает желудок и переходит в тонкий кишечник. Они катализируют распад пептидных связей, с которыми не справились ни пепсин, ни соляная кислота. В результате в основную часть тонкого кишечника белки попадают в виде множества мелких пептидов, состоящих из двух-трех-четырех аминокислот. А соки кишечника содержат множество «пептидаз», которые и завершают работу по катализированию распада различных пептидов на одиночные аминокислоты.
У всех этих пищеварительных изменений есть общие детали. Прежде всего, все они заключаются в превращении больших молекул в маленькие. Такие метаболические превращения сравнительно больших и сложных молекул в маленькие и простые именуются словом «катаболизм». Следовательно, можно сказать, что пищеварение — это ряд катаболических изменений.
Далее, различные катаболические преобразования, происходящие при пищеварении, всегда подразумевают расщепление некоторых химических связей и присоединение в месте расщепления молекулы воды. Такой способ разрывать связь с помощью добавления воды — вполне естественное изобретение, если принять во внимание, что живая ткань большей частью из воды и состоит — на 60 процентов, если мерить по весу, и на 98 процентов, если считать по количеству отдельных молекул (это то, что касается именно человека). Такой процесс получил название «гидролиз» (от греческих слов, означающих «терять с водой»), а подробности гидролитических изменений, происходящих при переваривании пищевых веществ каждого из трех классов, приведены на рис. 41.
Итоговые продукты пищеварения — единицы строения, полученные путем катализируемого ферментами гидролиза из сложных веществ, изначально присутствующих в пище, — могут проходить сквозь мембрану кишечника («абсорбироваться», или «впитываться») и попадать таким образом уже непосредственно внутрь организма. Более сложные молекулы этого сделать, как правило, не могут.
Таково значение пищеварения: оно превращает невпитываемые питательные вещества во впитываемые единицы, из которых они состоят. Более того, для организма крайне важно, чтобы исходные питательные вещества во всей своей сложности не впитывались. Набор углеводов и жиров, естественный для каждого организма, в мелочах отличается от набора углеводов и жиров, естественных для других организмов. А уж про белки и говорить нечего. Организму нечего и пытаться внедрить в свою структуру чужие молекулы, все сразу и в неизмененном виде. На самом деле, даже когда такое происходит, и чужие белки или сложные углеводы по какой-то причине в нетронутом виде попадают в организм, он тут же начинает вырабатывать особые белковые молекулы (антитела), которые связывают посторонние молекулы и быстро выводят их из строя.
В дальнейшем антитела не исчезают из организма, что обеспечивает человеку иммунитет против болезни в будущем, если белок, на который они выработаны, является частью вредоносного микроорганизма или производимым таким микроорганизмом токсином. Однако антитела могут сослужить и плохую службу, сделав человека «гиперчувствительным» к присутствию чужеродных белков вполне безобидной природы — в виде наступления аллергических реакций, вроде сенной лихорадки, астмы или пищевой аллергии.
Если же организм имеет дело не со сложными веществами, а всего лишь с их структурными единицами, то таких проблем не возникает. Не важно, сколь различны между собой белки коровы, утки или пшеницы и насколько все они вместе отличаются от человеческих белков, — все они состоят из одних и тех же аминокислот. Будучи разложенными в организме, они предоставляют для впитывания организмом именно аминокислоты — прекрасный строительный материал для человеческих белков. Точно так же и чужеродные углеводы разлагаются на глюкозу, из которой строятся уже человеческие углеводы, а чужеродные жиры — на глицерин и жирные кислоты, из которых создаются человеческие жиры.
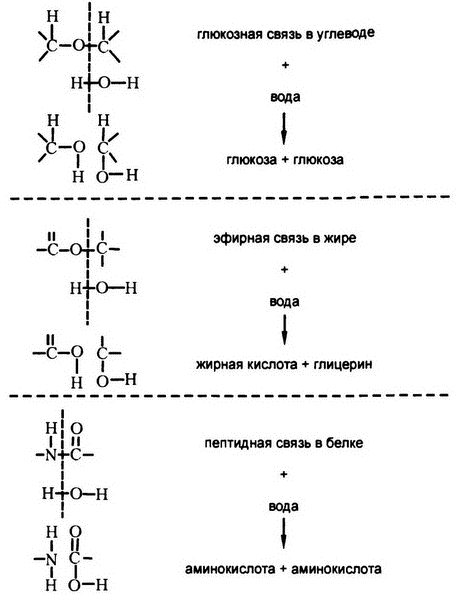
Рис. 41. Гидролиз в процессе пищеварения
Пройдя сквозь кишечную мембрану и будучи впитанными, структурные единицы попадают уже непосредственно в организм. Таким образом, из вида биохимиков и физиологов XIX века они после этого пропадали. О процессе метаболических изменений, происходящих в самом организме (промежуточном метаболизме), можно было судить лишь по косвенным признакам.
Точнее говоря, природа конкретных изменений в целом была уже понятна. Ясно, что глюкозе и жирным кислотам предстояло подвергнуться, хотя бы частично, дальнейшему разложению на еще более мелкие молекулы углекислоты и воды. Аминокислоты тоже должны превратиться, хотя бы частично, в углекислоту, воду и азотсодержащую мочевину. Эти процессы должны происходить хотя бы потому, что в моче имеется мочевина, а в выдыхаемом воздухе — газообразная углекислота, а вода вообще выделяется организмом всеми возможными способами — и с мочой, и с дыханием, и через кожу с потом (рис. 42).
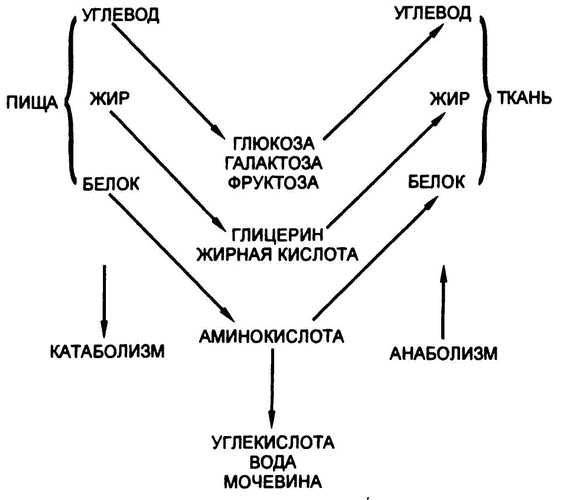
Рис. 42. Общая схема метаболизма
Кроме того, различные структурные единицы должны, хотя бы частично, подвергнуться изменениям, которые вновь построят из них сложные молекулы. В отношении аминокислот и жирных кислот это казалось однозначным, поскольку в человеческом организме содержатся строго специфические, человеческие белки и жиры, которые можно сформировать только из структурных единиц.
Присутствие в организме специфических человеческих углеводов — менее очевидно. Точнее, в 1844 году немецкий биохимик К. Шмидт обнаружил, что в крови содержится в небольшом количестве глюкоза, но речь шла именно о самой глюкозе как о структурной единице. Однако в 1856 году французский физиолог Клод Бернар увенчал свои многолетние исследования открытием того факта, что в печени содержится склад крахмалоподобных углеводов, имеющих некоторые отличия от самого крахмала. Бернар назвал этот углевод «гликогеном», от греческого «производить сахар», поскольку в процессе гидролиза именно это с углеводом и произошло бы.
Происходящие в организме метаболические реакции, в ходе которых производятся большие и сложные молекулы из маленьких и простых — белки из аминокислот, жиры из жирных кислот, гликоген из глюкозы, — являются примерами анаболизма.
Понятно, что как анаболитические, так и катаболитические реакции, включенные в процесс промежуточного метаболизма, неизбежно имеют место именно таким образом, как описано выше. Поняв это, можно приступать к их изучению, даже не зная химических подробностей.
К примеру, концентрация глюкозы в крови всегда постоянна. Каждый кубический сантиметр крови содержит, грубо округляя, один миллиграмм глюкозы, служащей промежуточным запасом пищи для омываемых кровью клеток. Когда происходит расщепление большого объема пищи и в организм одновременно поступает много глюкозы, ее уровень в крови не испытывает скачкообразного возрастания. И точно так же он не падает, когда в результате долгого голодания организм расходует глюкозу, не получая компенсирующего притока ее извне.
Такая гармония является возможной благодаря уравновешенности анаболитических и катаболитических процессов. Глюкоза, получаемая в ходе расщепления пищи (катаболизм), проходит сквозь стенки кишечника в кровеносные сосуды, сходящиеся в так называемую «воротную вену». Воротная вена доставляет глюкозу в печень, где распадается на сеть «синусоид», омывающих клетки печени. Глюкоза переходит из крови в клетки печени, и там из нее формируется гликоген (анаболизм), в виде которого она и хранится для последующего использования.
После того как кровь покидает печень, концентрация глюкозы в ней уже соответствует норме. По печеночной вене кровь попадает из печени в сердце, откуда разносится по всему организму. Содержащаяся в ней глюкоза впитывается различными клетками организма и в них уже разлагается на углекислоту и воду (катаболизм).
Общего уменьшения уровня глюкозы в крови из-за впитывания клетками не происходит, потому печень постоянно обеспечивает свежий ее приток.
Однако по окончании переваривания пищи глюкоза перестает поступать в организм через стенки кишечника, и, если голодание затянется, нового поступления ее не будет в течение нескольких часов, а то и дней. И что тогда? Что ж, в такой ситуации, когда воротная вена вынуждена гнать в синусоиды кровь, лишенную глюкозы, срабатывают обратные механизмы. В гликоген превращать больше нечего, но сам-то гликоген в печени еще хранится! И вот теперь организм начинает его потихоньку расщеплять (катаболизм), ровно с такой скоростью, чтобы обеспечить кровь в печеночной вене строго рассчитанным количеством глюкозы.
Балансируя, таким образом, между катаболизмом и анаболизмом, печень превращает масштабные колебания уровня глюкозы в крови в ровную линию. Можно сказать, что она оказывает то же действие на уровень глюкозы, что банковский счет — на уровень финансов преуспевающего семейства, где в успешные периоды деньги оседают и откуда в неудачные периоды они берутся, так чтобы уровень жизни при всех этих колебаниях особенно не менялся.
Поддержание баланса глюкозы в организме — на самом деле процесс очень тонкий. Он осуществляется с помощью двух гормонов — инсулина и глюкагона, каждый из которых производится определенными клетками поджелудочной железы и выделяется напрямую в кровь. (Таким образом, поджелудочную железу можно рассматривать как железу двойного назначения — она является и пищеварительной, выделяя соки в тонкий кишечник через проток, и эндокринной, выделяя гормоны непосредственно в кровь.)
Наличие в крови инсулина стимулирует реакцию анаболизма, то есть превращение глюкозы в гликоген, что приводит к снижению уровня глюкозы в крови. Глюкагон же, наоборот, стимулирует реакцию катаболизма, то есть превращение гликогена в глюкозу, и повышает уровень последней в крови.
Если, по какой-либо причине, баланс реакций в организме смещается в сторону катаболизма так, что печень выпускает в кровь слишком много глюкозы, то, попадая в клетки поджелудочной железы, кровь с высоким содержанием глюкозы начинает стимулировать производство инсулина, что, в свою очередь, приводит к моментальному снижению уровня глюкозы. Если снижение заходит слишком далеко, то кровь с низким содержанием глюкозы стимулирует производство уже глюкагона, что приводит к повышению ее уровня. Таким образом, постоянный уровень глюкозы обеспечивается благодаря тому, что сейчас принято называть «механизмом обратной связи».
Случается так, что поджелудочная железа человека оказывается не в состоянии производить инсулин. В результате мы имеем дело с заболеванием под названием «сахарный диабет». Если действие глюкагона не сдерживается антагонистом, то уровень глюкозы в крови начинает повышаться сверх нормы и достигает опасных значений. Организм начинает пытаться избавиться от лишней глюкозы через почки—и появление глюкозы в моче свидетельствует уже о достаточно далеко зашедшем диабете.
До начала XX века лечить это заболевание не умели. Да, врачи и биологи XIX века сумели с помощью вакцин и антитоксинов победить множество инфекционных заболеваний, но перед диабетом они оставались бессильными. Его ведь вызывает не микроб и не яд — он является следствием сбоев в работе внутренней химии организма, расстройства обмена веществ.
Доказательство тому было получено в 1889 году, когда двое немецких физиологов, Й. фон Меринг и О. Минковски, обнаружили, что для того, чтобы вызвать у собаки диабет, достаточно просто удалить у нее поджелудочную железу. Ученые пустились в поиски содержащегося в поджелудочной железе вещества, которое могло бы произвести противоположное действие, будучи введенным в кровоток, но первые двадцать лет исследований ни у кого ничего не получалось.
В 1921 году канадский врач Фредерик Грант Бентинг предположил, что причина неудач может крыться в белковой природе искомого вещества, благодаря чему после извлечения поджелудочной железы из организма оно могло очень быстро разлагаться под воздействием протеаз поджелудочной. С помощью молодого студента по имени Чарльз Герберт Бест Бентинг попробовал извлечь поджелудочную железу для исследования по-новому — перевязав предварительно проток. Это помогло исключить из общей картины действие пищеварительных соков железы — производящие их части железы атрофировались. После этого уже была извлечена оставшаяся часть железы, и из нее было извлечено вещество, впоследствии названное инсулином.
С помощью инсулина, изготавливаемого из поджелудочной железы забитого скота — коров и свиней, можно сдерживать проявления диабета (но, увы, добиться полного излечения, то есть научить организм снова вырабатывать инсулин, — нельзя), и сейчас диабетики могут вести полноценную жизнь.
Вернемся к балансу глюкозы. Печень может содержать лишь ограниченный объем гликогена. Когда количество гликогена доходит до 10—15 процентов от ее общего веса, то больше она принять на хранение уже не может. Кроме того, гликоген может храниться и в мышцах — до количества не более 1 процента. Мышц в организме гораздо больше, чем печени, так что общее количество гликогена, содержащегося в мышцах, гораздо больше, чем содержащегося в печени, несмотря на более низкую концентрацию. В целом печень может хранить около 250 граммов гликогена, а мышцы — около 350. То есть всего в организме может храниться около 600 граммов гликогена.
Теперь давайте вспомним содержание главы 14, где я писал, что энергетическая ценность углеводов при превращении их в углекислоту и воду составляет около 4 килокалорий на грамм. Таким образом, если все 600 граммов гликогена израсходовать, организм получит 2400 килокалории. В принципе этого может хватить на день обычного энергорасхода, но ведь известно, что человек может не есть несколько недель и не только не умирает при этом, но и уровень глюкозы в его крови остается на допустимом уровне.
Возникает и еще один вопрос, близкий по сути к предыдущему: известно, что можно постоянно съедать больше крахмала, чем его расходуется на энергетические цели. Куда же девается при этом вся глюкоза, на которую этот крахмал распадается, если организм может хранить ее лишь в таких скромных объемах?
Ответ на эти вопросы кроется в веществах другого класса — в жирах. Всем нам известно, что от картошки, да и вообще от любой насыщенной крахмалом пищи толстеют, а что это может означать, кроме того, что организм умеет превращать углеводы в жиры? Очевидно, глюкоза тоже расщепляется на какие-то более мелкие единицы, которые превращаются организмом в жирные кислоты, из которых в дальнейшем строятся жиры. Это вполне экономичный подход с точки зрения организма, поскольку один грамм жиров содержит 9 килокалорий, а не 4, как углеводы. Соответственно, при одном и том же весе жир является в два с четвертью раза более вместительным хранилищем энергии, чем углевод. Переедающие и располневшие люди выглядели бы куда более страшно, если бы хранили весь своей энергетический запас не в жировом, а в углеводном виде, например в виде крахмала, как это делают картошка или рис.
Более того, этот процесс обратим. Известно, что при длительном голодании вес теряется. Поскольку жировой запас, в отличие от углеводного, не ограничен в объеме, то и голодать человек может неделями.
Если же ситуация совсем критическая и даже жировые запасы исчерпаны, то в энергетическую топку идут уже белки. От аминокислот отрезается азотная часть, а все остальное превращается организмом в глюкозу. В результате при затянувшейся голодовке ткани начинают пожирать сами себя.
Все это наталкивает на мысли о том, что на каком-то уровне катаболизма все виды питательных веществ приходят к одним и тем же структурным единицам. У глюкозы и жирных кислот должны быть какие-то общие «кирпичики», более простые, чем оба этих вещества. И аминокислоты, избавленные от азотной части, тоже должны в процессе катаболизма распадаться на те же «кирпичики», чем бы они ни оказались (рис. 43).
То есть создается впечатление полной универсальности биохимии в организме. Кажется, что из одних и тех же «кирпичиков» он может анаболичес-ки создавать все, что угодно.
Но надо иметь в виду и ограничения. Организм не может подменять один химический элемент другим, значит, эти «кирпичики» могут состоять только из углерода, водорода и кислорода, поскольку при их формировании из белков удаляется азот.
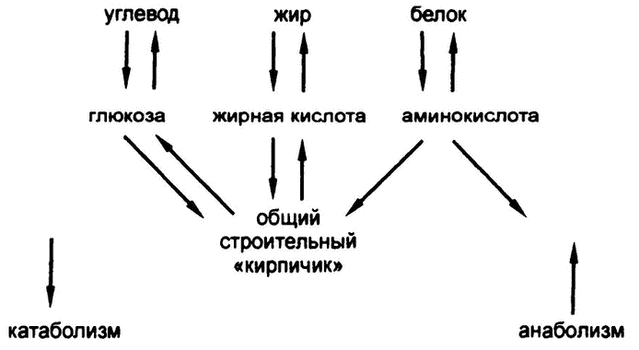
Рис. 43. Общий строительный «кирпичик»
А если азота в этом веществе не содержится, значит, и аминокислоты из него создавать уже не получится без привлечения дополнительного источника азота, каковым в общем случае может служить только белковая пища.
Отсюда вывод: можно прожить на диете с низким содержанием углеводов и жиров, поскольку при достаточном поступлении белков некоторые аминокислоты будут анаболизированы в белки организма, а остальные — очищены от азота, низведены до состояния общего «кирпичика», а затем анаболизированы в необходимые организму жиры и углеводы.
А вот без белков прожить не получится. Диета с низким белковым содержанием приведет к тому, что организм начнет расщеплять собственные ткани, и в конце концов человек умрет, сколько бы ни было в его пище жиров и углеводов. В отсутствие источника азота собрать из общих «кирпичиков» полноценный белок невозможно.
Но ограничения на гибкость биохимии организма не исчерпываются необходимостью источника азота. Как я уже говорил в предыдущей главе, организм не способен самостоятельно вырабатывать некоторые витамины. Да, они не требуются в больших количествах, и организму можно было бы простить подобную ограниченность, просто не обращая на нее внимания, но в более крупном масштабе она сказывается и на самих белках.
В начале XIX века во Франции было предпринято много попыток добиться получения дешевой пищи путем варки костей и соединительной ткани (неперевариваемой в общем случае) для получения желатина, который вполне хорошо усваивается организмом. Единственная проблема заключалась в том, что желатин, будучи единственным присутствующим в пище белком, не может поддерживать жизнедеятельность.
В течение XIX века химики выяснили, что белки состоят из множества различных аминокислот, и в 1872 году немецкий биохимик О. Нассе сумел продемонстрировать, что одна из них, тирозин, в желатине отсутствует. Позже обнаружилось, что в нем отсутствуют и другие аминокислоты — цистин, триптофан и метионин. Но ведь белок в пищеварительном тракте распадается на аминокислоты, и именно они впитываются организмом! Следовательно, оставалось предположить, что оценивать надо не питательные свойства белка, а питательные свойства аминокислот, а белок рассматривать уже с точки зрения того, какие именно аминокислоты в нем присутствуют.
Эксперименты диетологов, при которых источником азота служили не белки, а смеси аминокислот, ясно показали, что жизнедеятельность и рост тканей могут продолжаться и без белков, если в пище присутствуют все аминокислоты. Когда американский биохимик Уильям Роуз зафиксировал некоторые проблемы у испытуемых при проведении подобного эксперимента, он предположил, что причина проблем в том, что в его смесь не попала некая неизвестная доселе аминокислота. Он стал искать ее и в 1935 году открыл треонин — последнюю по времени обнаружения значимую аминокислоту. С добавлением треонина в питательную смесь все пошло на лад (что является дополнительным косвенным свидетельством в пользу того факта, что других аминокислот в составе белков не встречается).
Роуз проводил свои эксперименты на взрослых людях — аспирантах, для которых не самая увлекательная диета из крахмала, кукурузного масла, смеси аминокислот и витаминноминерального комплекса воспринималась как возможность послужить науке, ну и, несомненно, завершить собственное образование. В качестве критерия оценки достаточности диеты Роуз использовал нечто, что он сам называл «азотным балансом».
Содержание азота в пище может уравновешиваться содержанием азота в фекалиях (та часть азота из пищи, которая не впиталась) и в моче (так часть, которая впиталась, но впоследствии была отсечена по той или иной причине от белков организма и отправлена в отбросы). В обычных условиях у взрослого человека количество азота, содержащегося в пище, равно количеству азота, выделяемого с мочой и фекалиями. Содержание азота в организме при этом остается неизменным — соблюдается кислотный баланс.
Однако азот всегда в какой-то степени теряется. Даже если организм получает достаточно калорий, так что необходимости в расщеплении белков для получения энергии нет, все равно белки с некоторой скоростью избавляются от азотного содержимого (иногда этот процесс называют «износом»). Если не возмещать эти потери, то количество выделяемого организмом азота превысит количество азота поглощаемого и содержание азота в организме будет снижаться. Это называется «отрицательным азотным балансом».
Может случиться и так, что приток азота будет превышать его исход, так что содержание азота в организме будет возрастать — это называется «положительным азотным балансом». Для растущих детей положительный азотный баланс — норма, так же как и для выздоравливающих больных или оправляющихся после голодовки людей. В их организмах идет активный процесс строительства тканей после длительного периода отрицательного азотного баланса.
Для того чтобы в организме поддерживался азотный баланс, анаболизм и катаболизм белков должны протекать скоординированно. Скорость синтеза белков из аминокислот должна соответствовать скорости износа белков. Но для синтеза необходимо, чтобы в организме в достаточных количествах присутствовали все аминокислоты, входящие в состав требуемого белка (как правило, это все 19 аминокислот). Диетологические эксперименты показали, что недостаток даже одной аминокислоты приводит к невозможности формирования белка — организм не умеет собирать белки с гнездом для недостающей аминокислоты «на потом».
Если одна из аминокислот отсутствует, изнашивающиеся и уничтожаемые организмом белки не заменяются и все остальные аминокислоты, присутствующие в достаточном количестве, могут сгодиться только на производство энергии. Организм очищает, их от азота и катаболизирует. В результате мы имеем отрицательный азотный баланс.
Таким образом, понятно, что в организме должны присутствовать все аминокислоты — но значит ли это, что все они должны присутствовать именно в диете? Нет. Роуз установил, что некоторые аминокислоты вполне можно исключать из диеты аспирантов, не вызывая у них при этом отрицательного азотного баланса. Например, совершенно безо всяких последствий можно удалить из смеси аланин. Но ведь аланин является необходимым элементом строения белка, и он просто обязан присутствовать в организме! Вывод ясен: значит, организм каким-то образом сам синтезирует аланин, используя для этого азот из других аминокислот.
Таблица 8
НЕОБХОДИМЫЕ АМИНОКИСЛОТЫ
Аминокислота … Ежедневная норма (г)
Фенилаланин … 1,1
Метионин … 1,1
Лейцин … 1д
Лизин … 0,8
Валин … 0,8
Изолейцин … 0,7
Треонин … 0,5
Триптофан … 0,25
Таким образом, часть аминокислот можно исключить из пищи и организм сам будет синтезировать их в достаточном количестве.
С другой стороны, если исключался из диеты, например, лизин, то у обследуемого тут же фиксировался отрицательный азотный баланс. Лизин необходимо получать с пищей; организм явно не умеет производить его самостоятельно, независимо от наличия в нем других аминокислот. Поэтому лизин входит в число «необходимых» аминокислот.
Роуз установил, что «необходимых» аминокислот, то есть таких, которые организм должен получать с пищей, — всего восемь, и подсчитал минимальную ежедневную норму потребления каждой из них, при которой в организме не наблюдается отрицательного азотного баланса и расщепления собственных тканей. Аминокислоты и их ежедневная норма потребления приведены в таблице 8.
Таков еще один пример ограничений, налагаемых природой на гибкость химических процессов живого организма, помимо невозможности производить витамины. Витаминов достаточно потреблять в день по нескольку миллиграммов, а вот аминокислоты необходимо получать в количествах, превышающих аналогичные цифры для витаминов в сотни и даже тысячи раз.
| <<< Назад Глава 18. КАК РАБОТАЮТ ФЕРМЕНТЫ |
Вперед >>> Глава 20. ЖИЗНЬ БЕЗ ВОЗДУХА |
- Глава 13. И СНОВА О ЖИВОЙ И НЕЖИВОЙ МАТЕРИИ
- Глава 14. С МАЛОЙ СКОРОСТЬЮ
- Глава 15. КАТАЛИЗАТОРЫ ЖИЗНИ
- Глава 16. ПОДРОБНЕЕ О БЕЛКАХ
- Глава 17. СЛАБОЕ ПРИТЯЖЕНИЕ
- Глава 18. КАК РАБОТАЮТ ФЕРМЕНТЫ
- Глава 19. ДЛЯ ЧЕГО ЖЕ ОНИ НУЖНЫ?
- Глава 20. ЖИЗНЬ БЕЗ ВОЗДУХА
- Глава 21. ЗНАЧЕНИЕ ФОСФАТОВ
- Глава 22. ПЕРЕДАЧА ЭЛЕКТРОНОВ
- Глава 23. ЖИЗНЬ С ВОЗДУХОМ
- Глава 24. ГДЕ СХОДЯТСЯ ВСЕ ПУТИ
- Глава 25. ОСНОВНОЙ И ГЛАВНЫЙ ИСТОЧНИК
- Муравей, семья, колония
- Межклеточное вещество
- 04. На что влияет нагрев планет звездами, звезд Ядрами Галактик, Ядер Галактик Ядрами Сверхгалактик
- Список литературы
- Разные человечества
- Красные тучи, закрывающие солнце
- Московская белая
- Примерные рационы для котят от месяца до пяти и старше
- Голосеменные растения завоевывают мир
- Пароль скрещенных антенн
- Позор страны
- Что такое водопад?
