Книга: Самое грандиозное шоу на Земле
Радиоактивные «часы»
| <<< Назад Годичные кольца |
Вперед >>> Углерод |
Радиоактивные «часы»
Теперь перейдем к радиометрическому датированию. Нам есть из чего выбирать: радиоактивные «часы» отмеряют время от веков до миллиардов лет. У каждых есть погрешность, обычно не превышающая 1 %. Таким образом, если вы измеряете возраст горной породы в миллиардах лет, то должны принимать в расчет погрешность в десятки миллионов лет. Если определяете возраст породы, которой сотни миллионов лет, погрешность не будет превышать миллиона лет. Если породе десятки миллионов лет, делайте поправку на сотни тысяч лет.
Чтобы понять, как работают радиоактивные «часы», необходимо прежде узнать, что такое радиоактивный изотоп. Материя состоит из химических элементов, как правило, химически связанных с другими элементами. Всего существует около ста элементов (чуть больше, если прибавить элементы, которые существуют только в лабораторных условиях, и чуть меньше, если сосчитать только элементы, встречающиеся в природе): углерод, железо, азот, алюминий, магний, фтор, аргон, хлор, натрий, уран, свинец, кислород, калий, олово и так далее. Атомная теория строения вещества, с которой, думаю, согласны даже креационисты, утверждает, что каждому элементу соответствует собственный атом, являющийся самой маленькой частицей, на которую возможно разделить элемент без утраты им своих свойств. Как выглядит атом свинца, меди или углерода? Безусловно, не как медь, свинец или уголь. Он вообще никак не выглядит, поскольку слишком мал для того, чтобы броситься вам в глаза, каким бы мощным микроскопом вы ни пользовались. Поэтому мы прибегаем к аналогиям или моделям. Самая известная была предложена великим датским физиком Нильсом Бором. Модель Бора, сегодня уже устаревшая, похожа на Солнечную систему. Вместо Солнца — ядро, вокруг которого обращаются электроны, играющие роль планет. Как и в Солнечной системе, практически вся масса атома содержится в ядре («Солнце»), а практически весь объем занят пространством между электронами («планетами»). Каждый из электронов в сравнении с размером ядра пренебрежимо мал, а расстояние от него до ядра намного больше размеров самого ядра. Известная аналогия — ядро атома, как муха в центре футбольного стадиона. Тогда ядро соседнего атома будет мухой в центре соседнего стадиона. Электроны кружат по орбитам вокруг мух, они меньше самых мелких мошек, слишком маленькие для того, чтобы увидеть их в одном масштабе с мухами. Когда мы берем в руки кусок металла или камня, мы на самом деле смотрим на предмет, состоящий в основном из пустоты. Мы ощущаем его как плотное и непрозрачное тело потому, что наши органы чувств и мозг находят удобным воспринимать этот объект как твердый и непрозрачный. Наш мозг находит это удобным потому, что мы не можем пройти сквозь камень. «Твердый» — это характеристика, которую мы присваиваем веществам и материалам, через которые не можем пройти или в которые не можем провалиться из-за электромагнитных взаимодействий между их атомами. «Непрозрачный» — воспринимаемая нами картина света, отражающегося от поверхности объекта и не проходящего сквозь него.
Согласно модели Бора, в состав атома входят три вида частиц. С электронами мы уже знакомы. Две другие частицы, существенно превосходящие по размеру электрон, но по-прежнему настолько малые, что мы не можем увидеть их, называются протон и нейтрон. Они почти одинакового размера. Число протонов в атоме любого химического элемента постоянно и равно числу электронов. Оно называется атомным числом и является уникальным свойством химического элемента. Нет никаких промежутков в последовательности атомных чисел в знаменитой периодической таблице элементов[52]. Каждый номер в ряду соответствует одному и только одному химическому элементу. Элемент с атомным числом 1 — водород, 2 — гелий, 3 — литий, 4 — бериллий, 5 — бор, 6 — углерод, 7 — азот, 8 — кислород, и так далее.
Протоны и электроны несут электрические заряды противоположных знаков — мы называем их положительными и отрицательными. Эти заряды становятся важными, когда элементы составляют химические соединения. Основными проводниками взаимодействий являются электроны. Нейтроны в атомах связаны в ядре с протонами. В отличие от протонов, они не имеют заряда и не участвуют в химических реакциях.
Протоны, нейтроны и электроны любого химического элемента ничем не отличаются от таких же частиц, составляющих атомы других элементов. Никаких «золотых» протонов, «медных» электронов и «калиевых» нейтронов не существует. Атом меди делает атомом меди только наличие 29 протонов и электронов. Все, что мы привыкли считать свойствами меди, — вопрос химии. Химия — нескончаемый танец электронов. Все химические реакции — взаимодействие атомов при помощи электронов. Химические связи сравнительно легко образуются и распадаются, поскольку обмениваются или отделяются только электроны. Силы взаимного притяжения, образующие ядро атома, преодолеть существенно сложнее. Вот почему термин деление атома имеет зловещую окраску. Однако оно возможно, и в результате начинаются ядерные реакции — в противоположность химическим. На этом и основана работа радиоактивных «часов».
Масса электрона пренебрежимо мала, поэтому общая масса атома — его массовое число — равна суммарному числу протонов и нейтронов в ядре. Как правило, массовое число чуть более чем вдвое превосходит порядковый номер элемента, поскольку нейтронов обычно чуть больше, чем протонов. В отличие от числа протонов, число нейтронов не определяет, к какому элементу относится атом. Атомы любого элемента могут существовать в различных вариантах, именуемых изотопами, у которых одинаковое число протонов, но разное число нейтронов. У некоторых элементов, например фтора, имеется только один природный изотоп. Фтор — элемент с порядковым номером 9 и массовым числом 19. Отсюда следует, что ядро атома фтора состоит из девяти протонов и десяти нейтронов. Другие элементы, однако, имеют множество изотопов. У свинца пять широко распространенных изотопов. Все они имеют одно и то же число протонов и электронов (82 — атомное число свинца) и массовое число (от 202 до 208). Углерод имеет три природных изотопа. Углерод-12 — самый распространенный, он имеет по шесть протонов и нейтронов. Реже встречается углерод-13. Углерод-14 тоже редок, но его все же достаточно для использования в датировании образцов органического происхождения.
Одни изотопы стабильны, другие — нет. Свинец-202 нестабилен. Стабильными являются: свинец-204, свинец-206, свинец-207 и свинец-208. Нестабильность означает, что атомы данного изотопа спонтанно распадаются с образованием других атомов. Распадаются они с известной скоростью, но момент начала распада непредсказуем. Именно предсказуемость скорости распада служит основой радиоактивных «часов». Нестабильные изотопы иначе называют радиоактивными. Существует несколько видов радиоактивного распада, каждый из которых имеет ценность в качестве «часов». Нам не требуется понимание этих механизмов, но я постараюсь объяснить их, чтобы показать замечательный уровень детализации, которого физики достигли в ходе изучения этого вопроса. Этот уровень детализации придает комический оттенок попыткам креационистов доказать ненадежность радиометрического метода датирования и сохранить Землю вечно молодой, как Питер Пэн.
Все механизмы радиоактивности зависят от поведения нейтронов. Первый тип представляет собой превращение нейтрона в протон. Это означает, что массовое число не изменяется (поскольку масса протонов и нейтронов, как мы помним, одинакова), а атомное число увеличивается на единицу. Таким образом, атом превращается в другой элемент, на один дальше в периодической таблице. Например, атом натрия-24 становится атомом магния-24. В другом механизме протон превращается в нейтрон. Массовое число не изменяется, а атомное уменьшается на единицу, и в периодической таблице атом перемещается на клетку назад. Третий механизм, когда свободный нейтрон ударяет в ядро атома, выбивает один протон и занимает его место, приводит к такому же результату. Массовое число не изменяется, атомный номер уменьшается на единицу.
Более сложный тип распада связан с испусканием ядром альфа-частицы, состоящей из двух протонов и двух нейтронов. При альфа-распаде, таким образом, массовое число уменьшается на четыре, а атомное — на два. Атом переходит в химический элемент, находящийся на две позиции позади в периодической таблице. Примером такого распада может служить превращение радиоактивного изотопа уран-238 (92 протона, 146 нейтронов) в торий-234 (90 протонов, 144 нейтрона).
Подходим к сути. Все нестабильные изотопы распадаются с постоянной, хорошо известной скоростью. Более того, скорость распада некоторых изотопов существенно меньше, чем у других. Распад во всех случаях описывается экспонентой. Это значит, что если в начале эксперимента есть 100 г радиоактивного изотопа, то за единицу времени в другой химический элемент будет превращаться не фиксированное количество изотопа (скажем, 10 г), а строго определенная доля оставшегося количества. Здесь следует сказать о так называемом периоде полураспада — времени, за которое распадается половина атомов радиоактивного изотопа. Период полураспада не изменяется в зависимости от того, сколько атомов распалось прежде — это и означает, что процесс идет экспоненциально. Естественно, что при таком последовательном «ополовинивании» мы никогда не узнаем наверняка, что атомов начального элемента не осталось. Тем не менее, мы можем сказать, что спустя некоторое достаточно долгое время — например, десять периодов полураспада — останется так мало атомов исходного элемента, что в практических целях этим количеством можно пренебречь. Например, период полураспада углерода-14 составляет 5730±40 лет. Следовательно, для ископаемых образцов старше 50–60 тысяч лет радиоуглеродное датирование не подходит, и необходимо пользоваться более медленными «часами».
Период полураспада рубидия-87 составляет 49 миллиардов лет, фермия-244–3,3 миллисекунды. Впечатляет, не так ли? Этот разброс прекрасно отражает спектр доступных нам радиометрических методов датирования. Несмотря на то, что время полураспада углерода-15, составляющее 2,4 секунды, слишком коротко для прояснения вопросов эволюции, углерод-14 с его 5730 годами отлично подходит для датирования археологических находок. В датировке палеонтологических находок часто используется калий-40 (период полураспада 1,26 миллиарда лет), и я воспользуюсь им в качестве примера для объяснения принципа работы радиоактивных «часов». Часы, «работающие» на калии-40, часто называют калий-аргоновыми, поскольку именно аргон-40, находящийся в периодической таблице элементов клеткой раньше, является продуктом распада калия-40. Также калий-40 путем другого типа радиоактивного распада может превращаться в кальций-40, стоящий в таблице Менделеева на клетку правее.
Предположим, что в начале эксперимента у нас есть некоторое количество калия-40. Исходя из периода полураспада, через 1,26 миллиарда лет половина этого калия-40 превратится в аргон-40. Спустя еще 1,26 миллиарда лет в аргон превратится половина остатка, то есть четверть начального количества, и так далее. К любому моменту времени, меньшему 1,26 миллиарда лет, в аргон превратится соответствующая часть начального количества калия-40. Теперь представьте, что мы помещаем некоторое количество калия-40 в закрытый контейнер, в котором нет аргона-40. Спустя несколько сотен миллионов лет к контейнеру приходит ученый и измеряет соотношение калия-40 и аргона-40. Исходя из этого соотношения и зная, что аргона-40 в начале эксперимента не было, даже при неизвестном начальном количестве калия-40 можно вычислить, сколько времени прошло с момента начала распада, то есть с «обнуления» радиоактивных «часов». Нам необходимо и достаточно знать только соотношение родительских (калий-40) и дочерних (аргон-40) изотопов. Кроме того, как мы уже обсуждали, необходимо, чтобы «часы» обнулялись. Как это может произойти? Ответ дает понимание процесса кристаллизации.
Как и все радиоактивные «часы», используемые геологами, калий-аргоновые часы работают только на магматических породах. Магматические породы образуются при затвердевании расплавленной породы — подземной магмы (гранит) или вулканической лавы (базальт). Когда расплавленная порода застывает, она кристаллизуется. Обычно это некрупные прозрачные кристаллы наподобие кварца — как правило, они слишком малы, чтобы без помощи микроскопа распознать в них кристаллы. Кристаллы бывают разные, и некоторые из них (например, слюда) содержат атомы калия. Среди этих атомов есть и атомы радиоактивного изотопа калий-40. В момент образования кристалла, когда затвердевает расплавленная порода, аргона в ней нет, и, соответственно, «часы» обнуляются. Проходят миллионы лет, атомы калия-40 постепенно распадаются и заменяются в кристалле на атомы аргона-40. Количество образовавшегося аргона-40 соответствует времени, прошедшему с момента образования породы. Но, как я отмечал выше, имеет смысл не количество аргона, а только соотношение числа атомов калия и аргона. В момент обнуления «часов» соотношение составляло 100 % в пользу калия-40. Через 1,26 миллиарда лет соотношение будет равно 50 %, еще через 1,26 миллиарда лет — 25 %, и так далее. Промежуточные значения будут соответствовать промежуточным значениям времени, прошедшего с момента обнуления «часов». Таким образом, геолог, измеряя соотношение между калием-40 и аргоном-40 во фрагменте вулканической породы, может определить, как давно эта порода кристаллизовалась. Как правило, вулканические породы содержат не только калий-40, но и другие радиоактивные изотопы. Весьма удачно, что вулканические породы застывают почти мгновенно[53] — следовательно, все радиоактивные «часы» в куске породы обнуляются одновременно.
Радиоактивные «часы» существуют только в породах вулканического происхождения, в которых почти никогда не бывает окаменелостей. Ископаемые остатки живых существ сохраняются в осадочных породах — известняках и песчаниках, которые не имеют отношения к лаве. Осадочные породы — слои грязи, ила, песка, постепенно накапливающиеся на дне моря, озера или залива. Проходят эпохи, и слои песка и грязи слеживаются, становясь твердыми как камень. Остатки живых существ, похороненные в иле, имеют шанс окаменеть. Окаменевают далеко не все остатки, но только осадочные породы содержат окаменелости, о которых вообще есть смысл разговаривать.
К сожалению, датировка осадочных пород радиометрическим методом невозможна. Вероятно, отдельные песчинки и частицы ила, из которых формируются осадочные породы, содержат калий-40 и другие радиоактивные изотопы и, таким образом, имеют встроенные радиоактивные «часы». Однако этими «часами» нельзя пользоваться, поскольку они не обнуляются (или обнуляются в разное время). С точки зрения датировщика, осадочная порода — настоящий хаос, пользоваться ею нельзя. Лучшее, что мы можем сделать — и это совсем не так плохо! — это определить возраст вулканических пород, обнаруживаемых рядом с исследуемой осадочной породой или включенных в нее.
Чтобы определить возраст находки, она необязательно должна быть заключена между слоями вулканической породы, как ветчина в сандвиче. По всему миру встречаются очень похожие слои осадочных пород. Задолго до возникновения радиометрических методов датирования эти слои были идентифицированы и названы: кембрий, ордовик, девон, юра, мел, эоцен, олигоцен, миоцен. Девонские осадочные породы обнаруживают не только в Девоншире, графстве на юго-западе Англии, но и в других частях света. Они похожи друг на друга и содержат сходные наборы ископаемых. Порядок, в котором откладывались эти осадочные слои, известен геологам очень давно. До изобретения радиоактивных «часов» мы не знали только, когда именно возник каждый слой. По порядку их можно расставить хотя бы потому, что старшие слои залегают глубже молодых. Так, девонские отложения старше карбоновых (названных так потому, что в карбоновых отложениях обнаруживается каменный уголь). Мы знаем это потому, что в тех частях света, где эти слои встречаются вместе, девонский слой расположен под карбоновым (за исключением регионов, где мы на основании других признаков можем сказать, что осадочные слои были смяты, наклонены или даже перевернуты). Как правило, мы не настолько удачливы, чтобы найти полную последовательность слоев от кембрия до современности. Но благодаря тому, что слои легко узнаваемы, вы можете прослеживать цепочки из последовательных слоев по всему миру, сравнивать их между собой и таким образом устанавливать их взаиморасположение.
Итак, задолго до того, как мы узнали, сколько лет ископаемым, мы знали порядок, в котором они были захоронены, или, по крайней мере, в каком порядке откладывались содержащие их слои осадочных пород. Мы знали, что кембрийские ископаемые из любой части света старше ордовикских, которые, в свою очередь, старше силурийских (затем следуют девонские, карбоновые, пермские, триасовые, юрские, меловые и так далее). Внутри слоев геологи различают подслои: верхняя юра, средняя юра, нижняя юра и тому подобные. Указанные слои, как правило, можно опознать по содержащимся в них ископаемым. И мы воспользуемся послойным расположением окаменелостей как одним из доказательств эволюции. Нет ли опасности, что мы угодим в порочный круг? Нет. Кембрийские окаменелости — это характерный набор ископаемых, безошибочно опознаваемых как кембрийские. Эти окаменелости в настоящее время используются как маркеры пород кембрийского возраста. Именно поэтому нефтедобывающие компании нанимают палеонтологов, способных по микроскопическим ископаемым остаткам животных (как правило, фораминифер или радиолярий) идентифицировать слои осадочных пород.
Для каждого слоя — ордовикского, девонского и прочих — характерен свой набор ископаемых. До сих пор мы пользовались ими только для того, чтобы определить, к какому слою относится данная порода — пермского или, скажем, силурийского периода. Теперь мы воспользуемся прослеженным по всему миру порядком отложения геологических слоев, чтобы установить, какие слои образовались раньше, а какие позднее. Используя эти два блока информации, мы можем проследить, двигаясь вверх по слоям, образуют ли найденные в них ископаемые осмысленную с эволюционной точки зрения последовательность. Развиваются ли они в каком-то определенном направлении? Появляются ли некоторые разновидности ископаемых (например, млекопитающие) только после определенного момента (слоя) и никогда — раньше? Ответ на все подобные вопросы — да. Всегда. Никаких исключений. Это одно из главных свидетельств в пользу эволюции, поскольку оно не является необходимым фактом и никак не следует ни из нашего метода идентификации слоев, ни из способа, позволившего нам установить хронологический порядок их формирования.
Остатков животных, хотя бы отдаленно похожих на млекопитающих, никогда не обнаруживали в девонских или более ранних слоях. Млекопитающие не просто статистически реже встречаются в девоне. Они никогда не встречались в слоях старше определенного возраста. Не то чтобы это обязательно было так — могло бы быть иначе: копая все глубже и глубже от девона, раскрывая все более ранние слои (силур и ордовик), мы докопались бы до кембрия и с удивлением обнаружили бы там изобилие млекопитающих. На самом деле ничего подобного мы в кембрийских слоях, конечно, не обнаружим, но этот пример прекрасно иллюстрирует, что наши рассуждения не заводят нас в порочный круг. В тот момент, когда кто-либо извлечет остатки млекопитающего из кембрийской породы, теория эволюции рассыплется в прах. Таким образом, теория эволюции может быть опровергнута и, следовательно, является научной теорией. Я вернусь к этому вопросу в главе 6.
Попытки креационистов объяснить подобную последовательность находок выглядят комично. Нам авторитетно сообщают, что ключом к пониманию последовательности захоронения ископаемых является Всемирный потоп. Привожу цитату с одного заслуженного креационистского сайта[54]:
В геологических слоях наблюдается следующая последовательность ископаемых остатков:
1. Беспозвоночные (малоподвижные морские животные). Во время Всемирного потопа они должны были погибнуть первыми, следом — более подвижные рыбы, которых завалило илом.
2. Амфибии (живут близко к морю) — вымерли, когда вода начала подниматься.
3. Рептилии (медленно движущиеся наземные животные).
4. Млекопитающие — могли убегать от наступающей воды, при этом чем крупнее и быстрее животное, тем дольше оно продержалось.
5. Человек — должен был проявить наибольшую изобретательность, цепляясь за плавающие бревна и тому подобное, чтобы спастись от наводнения.
Эта последовательность полностью объясняет порядок, в котором различные ископаемые обнаруживаются в геологических слоях. Это никоим образом НЕ порядок, в котором животные появлялись в процессе эволюции — это порядок, в котором они были погребены во время Ноева потопа.
Замечательное объяснение! Оставив прочие причины, по которым с ним невозможно согласиться, замечу только, что млекопитающие в таком случае должны быть только статистически, то есть в среднем успешнее убегать от воды, чем, например, рептилии. На самом деле, как и предсказывает теория эволюции, в более древних геологических слоях млекопитающих вообще нет. Теория «бегства в горы» была бы более обоснованной, если бы с глубиной залегания слоев количество остатков млекопитающих убывало статистически, постепенно. Однако выше перми нет трилобитов, а выше мела нет динозавров (кроме птиц). Теория «бегства в горы» в этих случаях предсказывает постепенное убывание.
Но вернемся к датированию и радиоактивным «часам». Поскольку последовательность расположения слоев осадочных пород хорошо известна и одинакова во всем мире, можно использовать вулканические породы, залегающие непосредственно над или под этими слоями (или внутри них) для датирования осадочных слоев и, соответственно, обнаруженных в них окаменелостей. Усовершенствовав метод, мы сможем датировать ископаемые остатки, находящиеся, скажем, в верхней части карбона или мела, как более ранние, чем окаменелости, лежащие чуть глубже в этих же слоях. Нет необходимости искать прослой вулканической породы в непосредственной близости от ископаемого, возраст которого мы хотим определить. Исходя лишь из того, что окаменелость найдена в определенной части девонского слоя, ее возраст можно определить, скажем, как верхнедевонский. Анализ возраста вулканических пород, обнаруживаемых рядом с девонскими осадочными породами по всему миру, показывает, что девон окончился около 360 миллионов лет назад.
Калий-аргоновые «часы» — только одни из многих радиоактивных «часов», доступных геологам. Все они работают по одному и тому же принципу, хотя шкала у них разная. Ниже приведена таблица, в которой «часы» ранжированы от медленных к быстрым. Еще раз отметим огромный разброс периодов полураспада — от 49 миллиардов лет до 6 тысяч лет. Быстрые «часы» (например, углерод-14) имеют особый механизм обнуления. Все атомы быстро распадающихся изотопов, которые были на Земле в момент ее возникновения, давным-давно распались. Прежде чем перейти к рассказу о радиоуглеродном датировании, есть смысл остановиться еще на одном доказательстве древности Земли — планеты, возраст которой составляет миллиарды лет.
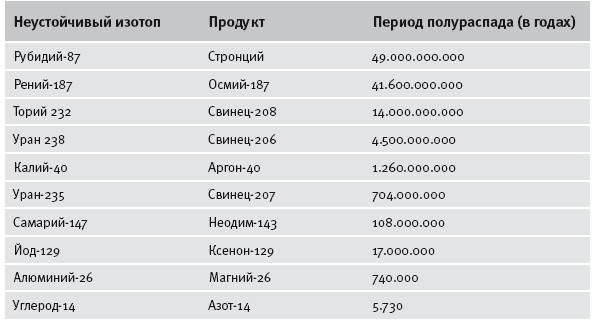
Радиоактивные «часы»
У всех химических элементов, встречающихся на Земле, есть 150 стабильных изотопов и 158 нестабильных, всего 308. Из 158 нестабильных изотопов 121 полностью исчез или существует, как углерод-14, только из-за постоянного обновления (мы увидим это чуть позднее). Теперь, если мы рассмотрим оставшиеся 37 существующих на Земле нестабильных изотопов, мы обнаружим важную и интересную вещь. Период полураспада каждого из них превышает 700 миллионов лет. У каждого из исчезнувших изотопов время полураспада не превышает 200 миллионов лет. Эти цифры не должны сбивать вас с толку — помните, что мы говорим о периоде полураспада. Рассмотрим судьбу радионуклида с периодом полураспада в 100 миллионов лет. Исходя из того, что мы обсуждали в середине главы, можно заключить: изотопы, период полураспада которых в десять и более раз уступает возрасту Земли, фактически исчезли, их больше нет на планете нигде, за исключением некоторых особых условий. Учитывая исключения, причины которых ясны, на Земле обнаруживаются только изотопы, период полураспада которых позволяет им сохраниться на очень старой планете. Углерод-14 представляет собой одно из вышеупомянутых исключений, потому что его запас на Земле постоянно пополняется. Следовательно, углерод-14 в качестве радиоактивных «часов» надо воспринимать отдельно от прочих. Что это означит — обнулить углеродные часы?
| <<< Назад Годичные кольца |
Вперед >>> Углерод |
- 945. Безопасно ли сбрасывать радиоактивные отходы в глубоководных районах океана?
- 941. Какие радиоактивные отходы могут служить потенциальным источником загрязнения Океана?
- 4.16. ЕСТЕСТВЕННО РАДИОАКТИВНЫЕ
- 36. Радиоактивные элементы и их распад.
- Радиоактивные свойства фермия
- Защита и контратака
- Рациональное и нерациональное природопользование
- Из чего сделаны гены?
- 955. Как влияет загрязнение вод на разведение устриц и ракообразных?
- Космическая история углеродных молекул
- 930. Как влияют разливы нефти на морских птиц?
- 936. Каким образом ядохимикаты, пестициды и другие загрязнители, содержащиеся в воде в ничтожных концентрациях, достигаю...
