Книга: Земля и космос. От реальности к гипотезе
Глава 12 Заполняя пробелы
| <<< Назад Глава 11 Умножение элементов |
Вперед >>> Переходные элементы |
Глава 12
Заполняя пробелы
В 1969 году Хугтон Миффлин опубликовал мою сотую книгу. (Если возник вопрос какую, то название этой книги — «Опус 100». Это что-то вроде литературной автобиографии, с подборкой иллюстраций из ранних работ. — Примеч. авт.) «Бостон глоб» решил отметить это событие пространной статьей, следом за которой появилась еще одна статья в «Нью-Йорк таймс». Кроме того, в день публикации Хугтон Миффлин притащил меня на вечеринку с коктейлем.
От всего этого у любого закружилась бы голова, и, чтобы не забыть о скромности, которая была всегда моей добродетелью, я постоянно напоминал себе случай, произошедший с моей матерью.
В начале 1950-х годов мои родители наконец продали свой кондитерский магазин и ушли на пенсию. Естественно, отец не мог сидеть без дела, потому нанялся на работу с сокращенным рабочим днем, а мать стала учиться в вечерней школе.
Мать всегда тяжело переживала свое неумение писать по-английски. Она могла делать это по-русски и на идише, но ни на одном языке с латинским алфавитом. Умела читать по-английски, но не знала, как писать. И потому мать стала брать уроки письма и скоро добилась впечатляющих успехов. Прошло совсем немного времени, и она написала мне письмо ясным почерком.
Однажды вечером ее остановил в вестибюле один из учителей вечерней школы с ее факультета и задал вопрос, который мы дома называем «этим старым добрым вопросом»: «Извините, миссис Азимов, но вы, случайно, не родственница Айзека Азимова?»
Моя мать немедленно ответила: «Да, в самом деле. Айзек Азимов — мой сын».
Учитель воскликнул: «О! Тогда неудивительно, почему вы так хорошо пишете!»
На это моя мать, вспомнив поговорку: яблоко от яблони недалеко падает, выпрямилась во все свои сорок футов и холодно произнесла: «Прошу прощения, сэр. Неудивительно, почему он — хороший писатель».
Напомнив себе об этом, дабы призвать свою скромность, я перейду к своему предмету, который начнется с той точки, на которой окончилась предыдущая глава.
В середине XIX столетия было обнаружено примерно тридцать элементов, и это начало внушать химикам тревогу. Каждое десятилетие число элементов возрастало: три было открыто в 1770-х годах, пять — в 1780-х, пять — в 1790-х, четырнадцать — в 1800-х, четыре — в 1810-х, пять — в 1820-х и так далее.
Возникала мысль: когда же это кончится? Ученые ценят простоту, а то, что казалось им простым, становилось все сложнее и сложнее. Требовался какой-то новый порядок, в котором бы все снова стало простым. Для этого необходимо было найти некую закономерность в запутанном списке элементов, так чтобы можно было разбить элементы на отдельные «семейства». Это могло бы как-то «расчистить джунгли».
В самом деле, если бы элементы были правильно организованы, стало бы ясно, сколько элементов существует всего и сколько, таким образом, элементов осталось неоткрытыми. В середине XIX столетия, однако, это казалось невыполнимой задачей.
В то время было известно, что атомы разных элементов имеют свои атомные веса. Так, если вес атома водорода (самого легкого из известных, как тогда, так и сейчас) равен 1, атом углерода, который массивнее в 12 раз, соответственно, должен иметь атомный вес 12, атом кислорода — 16 и так далее.
Тогда для начала можно попытаться организовать элементы в порядке атомных весов, чтобы определить, будут ли у них схожими какие-нибудь семейства. Оказалось, что прямоугольная таблица может быть создана таким образом, чтобы схожие элементы распределялись столбцами или колонками (в зависимости от того, вертикально или горизонтально размещаются элементы). К сожалению, на самых первых таблицах объединялись друг с другом очень несхожие элементы, а в науке половинное решение — это не решение вообще.
Ясно, что главная проблема с организацией по атомным весам заключалась в том, что нельзя было определить, когда список завершится. Оказалось, что атомная масса углерода равна 12, азота — 14, а кислорода — 16. Как можно быть уверенным, что между ними не существует неоткрытых элементов с атомными массами 13 и 15? Кому нужна таблица, в которой зияют пустоты?
Конечно, можно возразить, что разница в 2 атомные массы очень мала, и вряд ли здесь есть промежуточный элемент, но уверенным в этом быть нельзя. Никель имеет атомную массу 58,7, а кобальт — 58,9. С такой разницей в атомной массе между углеродом и азотом могло бы уместиться девять элементов и еще девять между азотом и кислородом.
Это говорит о том, что полагаться только на атомные массы нельзя. Требуются еще какие-либо свойства, и лучше всего, если эти свойства будут представлены целыми числами, чтобы, переходя, скажем, от 1 к 2 и от 2 к 3, мы знали, что между ними ничего нет.
Первые результаты такого подхода появились в 1852 году. Английский химик Эдуард Франкланд заметил, что в химических формулах, которые были созданы к этому времени, один атом одного элемента, похоже, всегда связан с фиксированным числом атомов других элементов.
Таким образом, атом водорода никогда не связан более чем с определенным числом атомов другого вещества. Это можно назвать степенью комбинирования единицы (или валентностью, от латинского слова, обозначающего «степень»). Атом кислорода может комбинироваться с двумя атомами водорода, атом азота с тремя атомами, а атом углерода — с четырьмя, так что кислород, азот и углерод имеют валентности в 2, 3 и 4 соответственно. Эти валентности работают очень четко. Таким образом, атом углерода (валентность 4) может комбинироваться с двумя атомами кислорода (2 + 2) или с одним атомом кислорода и двумя атомами водорода (2 + 1 + 1).
Концепция валентности не только отличается простотой, ясностью и явной полезностью, но и вводит целые числа, поскольку валентностей 1,5 или 2,32 — или какой-либо в этом духе — не существует. (В действительности наука XX века дала новую концепцию, которая в самом деле ввела что-то вроде дробных валентностей, но это не влияет на систему доказательств в данной главе. — Примеч. авт.)
В 1869 году русский химик Дмитрий Иванович Менделеев попытался организовать элементы согласно молекулярной массе и валентности. Результатом стала система, очень упрощенную и неполную версию которой я привожу в таблице 1 с атомными весами, округленными до одной десятой после запятой.
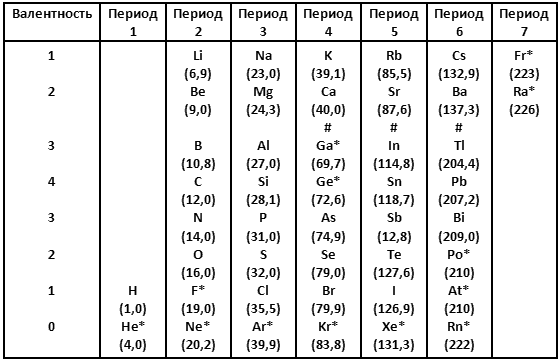
В таблице 1 я даю химические элементы так, чтобы сэкономить место; это не повлияет на систему доказательств и ни в коей мере не запутает, даже если вы не знаете, каким символом какой элемент обозначен. Когда мне придется упомянуть определенный элемент, я дам его полное название, вместе с символом.
Строки в таблице 1 содержат тесно связанные семейства элементов. К примеру, верхняя строка содержит литий (Li), натрий (Na), калий (К), рубидий (Rb), цезий (Cs) и франций (Fr), которые имеют одинаковые свойства. Эти элементы медленно плавятся, исключительно активны и при определенных условиях реагируют примерно одинаково. Более того, там, где различия существуют, они проявляют себя постоянным изменением вдоль строки. От лития к натрию, калию и так далее точка плавления вещества становится ниже, а активность его возрастает. Эти шесть элементов называют щелочными металлами.
Вторая строка содержит шесть щелочноземельных элементов, которые тоже имеют сходные свойства. И так далее на протяжении таблицы.
Заметим, что в периоде 5 теллур (Те) идет перед йодом (I), хотя теллур имеет большую атомную массу, а значит, должен находиться после йода, если бы классификация шла только по атомной массе.
Именно Менделееву принадлежит великая заслуга в том, что валентность (как и химические свойства в целом) стала учитываться в первую очередь по отношению к атомной массе. Для того чтобы поместить теллур и йод в надлежащее семейство с надлежащей валентностью, пришлось поменять порядок следования атомной массы. Более сложное знание атомной структуры, обретенное химиками в дальнейшем, доказало, что в этом отношении интуиция Менделеева оказалась абсолютно правильной.
Когда мы перемещаемся вниз по списку элементов согласно их молекулярной массе, периодически повторяется определенный набор свойств — по этой причине этот список, организованный так, что определенные наборы укладываются точно в строки или колонки, называются периодической таблицей.
В то время, когда Менделеев впервые выдвинул свою Периодическую систему, значительное число элементов, приведенных в таблице 1, еще не было открыто. Они указаны в таблице 1 звездочкой.
К примеру, шесть элементов в строке внизу — гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe) и радон (Rn) — не были известны в 1869 году. Об их существовании совершенно не представляли, и без них Периодическая система, казалось, имела законченный вид. Если идти последовательно сверху вниз в порядке атомных весов элементов, то изменение валентности в таблице 1 происходит (если исключить нижний ряд) по следующему порядку: 1, 1, 2, 3, 4, 3, 2, 1, 1, 2, 3, 4, 3, 2, 1, 1, 2 и так далее.
Однако, когда были открыты элементы в нижней строке, оказалось, что они не вступают в соединения с любыми другими элементами и, следовательно, имеют нулевую валентность. Таким образом, последовательность валентностей изменилась на следующую: 1, 0, 1, 2, 3, 4, 3, 2, 1, 0, 1, 2, 3, 4, 3, 2, 1, 0, 1, 2 и так далее.
Элементы нижней строки, имеющие схожие свойства и называемые инертными газами, или благородными газами, просто расширили таблицу, но не нарушили ее порядок. Наоборот, введение 0 в надлежащем месте сделало таблицу даже «элегантнее». Тот факт, что эта весьма неожиданно обнаруженная группа элементов столь превосходно вписалась в Периодическую систему, послужил дополнительным доказательством концепции Менделеева.
Для того чтобы сохранить аргон (Ar) на своем правильном месте в семействе инертных газов, его следует поставить перед калием (K), даже хотя это меняет порядок следования по молекулярным массам. И снова это повторилось в таблице с теллуром (Te) и йодом (I).
Заметим также, что в таблице 1 пять элементов с самыми большими атомными массами были неизвестны во времена Менделеева. Это полоний (Po), астат (At), радон (Rn), франций (Fr) и радий (Ra). Эти элементы были обнаружены в 1890-х и в последующие годы; они являются радиоактивными. Все эти элементы относятся к нестабильным и присутствуют в земной коре в очень малых количествах. Поскольку все они располагаются в конце таблицы, их отсутствие не влияло на все остальные.
Затем возник фтор (F), который, строго говоря, не был хорошо изучен во времена Менделеева. Это очень своеобразный элемент. Фтор был обнаружен в различных соединениях, из которых его извлечь не удавалось. Свойства фтора были известны, но на основании свойств его соединений. Его связи в соединениях оказались столь тесны, что только в 1886 году химики смогли выделить фтор из соединений, чтобы исследовать этот элемент в чистом виде. Даже малоизученный, фтор присутствовал в таблице с самого начала (это напоминает ситуацию с глобусом, северные и южные поля которого были обозначены, даже несмотря на то, что полюсов достигнуть пока не удалось).
Было еще два элемента таблицы, галлий (Ga) и германий (Ge), с особой судьбой. После их обнаружения не пришлось искать, поместить ли их в последний ряд или последнюю строку, чтобы они не нарушали общий порядок. Хотя об их существовании не подозревалось, для них оставили «вакантное место» в середине таблицы.
Если бы это место не было оставлено и будущие галлий и германий были бы проигнорированы, то при попытке перечислить элементы в порядке атомных масс пришлось бы поместить мышьяк (As) справа от алюминия (Al) и селена (Se) и справа от кремния (Si) и т. д. Это бы совершенно разрушило организацию по семействам и валентности.
Менделеев отказался от этого, и это было одним из величайших его достижений. Он поместил мышьяк (As) справа от фосфора (P), а селен (Se) справа от серы (S), где их места соответствовали их свойствам. Поскольку это оставило два свободных места справа от алюминия (Al) и кремния (Si), Менделеев решил, что они предназначены для двух элементов, которые еще только предстояло открыть. Он назвал их эка-алюминий и эка-кремний, «эка» — санскритское слово, обозначающее единицу. Другими словами, отсутствующие элементы находились на одно место справа от алюминия и кремния соответственно.
Более того, Менделеев предсказал свойства отсутствовавших элементов с большой точностью — он счел, что галлий (Ga) будет иметь свойства, промежуточные между алюминием (Al) и индием (In), а германий (Ge) — промежуточные между кремнием (Si) и цинком (Sn).
Поначалу большинство химиков мира снисходительно улыбались на «этого сумасшедшего русского», но в 1875 году был открыт галлий, а в 1886 году германий, и предсказания Менделеева сбылись во всех отношениях. Химики перестали смеяться.
Значит ли это, что описываемая нами система совершенна?
Увы, нет. Версия Периодической системы, что приведена в таблице 1, содержит лишь сорок четыре элемента, а их намного больше. Такие хорошо известные элементы, как золото, серебро, медь, железо, платина, марганец и вольфрам (все прекрасно изученные во времена Менделеева), не имели своего места в Периодической системе — в той форме, в которой она представлена в таблице 1.
Следует ли после этого отбросить систему, или же можно найти место для дополнительных элементов?
Обратите внимание, что три ячейки таблицы я пометил знаком #. Между кальцием (Ca) и галлием (Ga) разница в атомных массах составляет 29,7; между стронцием (Sr) и индием (In) 27,2; а между барием (Ba) и таллием (Tl) целых 67,1. Эти разницы немного больше, чем где-либо в Периодической системе. Если не обращать внимания на эти три интервала, то средняя разница в атомных массах от элемента к элементу во всей остальной таблице составит только 2,5.
Если мы примем 2,5 за среднюю атомную массу между соседними элементами таблицы, то останется пространство для двенадцати элементов между кальцием (Ca) и галлием (Ga), для одиннадцати элементов между стронцием (Sr) и индием (In) и для не менее чем двадцати семи между барием (Ba) и таллием (Tl).
Возможно ли это?
Да, возможно, если мы решим, что периоды в Периодической системе могут иметь не одинаковую длину (как считали некоторые поначалу), а увеличиваться по направлению к концу таблицы.
К примеру, во времена Менделеева в первом периоде имелся только один элемент, водород (H), тогда как во втором и третьем периодах было по семь элементов. Через одно поколение, когда были открыты инертные газы, оказалось, что в первом периоде находятся уже два элемента, а во втором и третьем периодах по восемь (с тех пор здесь изменений не было). Тогда почему в следующих периодах нельзя увеличить число элементов до двадцати, тридцати и даже больше?
В самом деле, во времена Менделеева было известно не менее девяти элементов с атомными массами, которые были между атомными массами кальция (Ca) и галлия (Ga); эти элементы словно заполняли большой зазор между этими массами. Аналогично девять элементов заполняли зазор между стронцием (Sr) и индием (In).
Проблема состоит в том, что валентность уже в отличие от положения с таблицей 1 не является первостепенным и определяющим фактором в этом зазоре. Элементы этого зазора расположены между элементом с валентностью 2 и элементом с валентностью 3 — от кальция (Ca) до галлия (Ga) в первом случае и от стронция (Sr) до индия (In) во втором, и, поскольку они осуществляют что-то вроде перехода от 2 до 3, их можно назвать транзитными элементами. В этой главе я буду называть элементы в таблице 1 валентными элементами.
Размещая в таблице транзитные элементы, мы можем частично руководствоваться атомными весами, частично — менее четко обозначенными валентными свойствами и частично другими химическими свойствами. Делая это, мы можем взять восемнадцать известных элементов первых двух промежутков (которые были известны к 1869 году) и выстроить их так, как показано в таблице 2.
К такому расположению трудно придраться. К примеру, ясно, что серебро (Ag) должно быть справа от меди (Cu) и что кадмий (Cd) должен быть справа от цинка (Zn), если исходить в первую очередь из основных химических свойств. Аналогично и с другими элементами. Только в указанном порядке свойства элементов соответствуют свойствам своих соседей, и у них даже атомные массы расположены по порядку, за исключением кобальта (Со) и никеля (Ni), у которых для того, чтобы сохранить последовательность химических свойств, атомные массы необходимо поменять местами. Но и в этом случае атомные массы находятся столь близко друг к другу, что подобная перестановка особенно картины не нарушает (это третий — и последний — случай перестановки в Периодической системе элементов по их атомным массам).
Таблица 2
| <<< Назад Глава 11 Умножение элементов |
Вперед >>> Переходные элементы |
