Книга: Популярная библиотека химических элементов. Книга вторая. Серебро — нильсборий
Меньше, чем лютеция
| <<< Назад Свойства обычные и необычные |
Вперед >>> Биологические функции иода |
Меньше, чем лютеция
Иод — элемент достаточно редкий. Его кларк (содержание в земной коре в весовых процентах) — всего 4?10-5%. Его меньше, чем самых труднодоступных элементов семейства лантаноидов — тулия и лютеция.
Есть у иода одна особенность, роднящая его с «редкими землями», — крайняя рассеянность в природе. Будучи далеко не самым распространенным элементом, иод присутствует буквально везде. Даже в сверхчистых, казалось бы, кристаллах горного хрусталя находят микропримеси пода. В прозрачных кальцитах содержание элемента № 53 достигает 5?10-6%. Иод есть в почве, в морской и речной воде, в растительных клетках и организмах, животных. А вот минералов, богатых иодом, очень мало. Наиболее известный из них — лаутарит Ca(IO3)2. Но промышленных месторождений лаутарита на Земле нет.
Чтобы получить иод, приходится концентрировать природные растворы, содержащие этот элемент, например воду соленых озер или попутные нефтяные воды, или перерабатывать природные концентраторы иода — морские водоросли. В тонне высушенной морской капусты (ламинарии) содержится до 5 кг иода, в то время как в тонне морской воды его всего лишь 20–30 мг.
Как и большинство жизненно важных элементов, иод в природе совершает круговорот. Поскольку многие соединения иода хорошо растворяются в воде, иод выщелачивается из магматических пород, выносится в моря и океаны. Морская вода, испаряясь, подымает в воздух массы элементного иода. Именно элементного: соединения элемента № 53 в присутствии углекислого газа легко окисляются кислородом до I2.
Ветры, переносящие воздушные массы с океана на материк, переносят и иод, который вместе с атмосферными осадками выпадает на землю, попадает в почву, грунтовые воды, в живые организмы. Последние концентрируют иод, но, отмирая, возвращают его в почву, откуда он снова вымывается природными водами, попадает в океан, испаряется, и все начинается заново. Это лишь общая схема, в которой опущены все частности и химические преобразования, неизбежные па разных этапах этого вечного коловращения.
А изучен круговорот иода очень хорошо, и это не удивительно: слишком велика роль микроколичеств этого элемента в жизни растений, животных, человека…
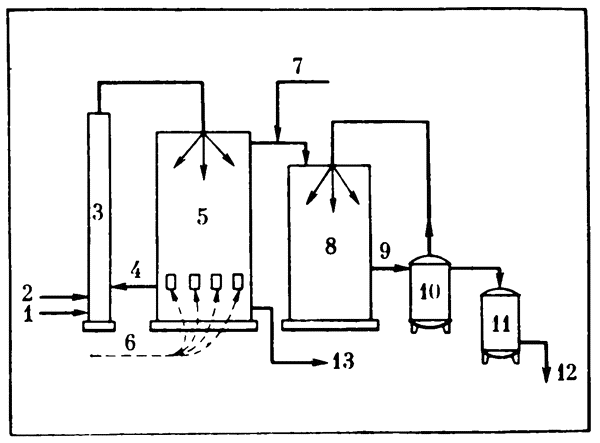
Схема одного из распространенных методов получения иода — из буровой воды воздушной десорбцией. Так же добывают и аналог иода бром.
1 — буровая вода; 2 — кислота; 3 — башня подкисления и окисления (хлоратор); 4 — хлор; 5 — башня отдувки элементного иода (десорбер); 6 — воздух; 7 — сернистый газ; 8 — уловитель иода (адсорбер); 9 — иодноватистая и серная кислоты (сорбент); 10 — сборник сорбента; 11 — кристаллизатор (здесь иод выделяется из сорбента); 12 — иод-сырец; 13 — безиодная буровая вода
| <<< Назад Свойства обычные и необычные |
Вперед >>> Биологические функции иода |
- Сохранить антибиотики: меньше значит больше
- Почему мужчины живут меньше?
- Еще о пользе секса, или Лучше меньше, да лучше
- Таблица 4.1. Кеплеровские элементы орбиты и звездные величины комет, MOID которых меньше 0,1 а.е.
- Уменьшение нормы разрешённого багажа
- Почему у людей две груди, не больше и не меньше?
- Глава 9 Все мы черные в большей или меньшей степени: физические способности и генетическое разнообразие
- В 400 тысяч раз меньше, чем радия
- Когда меньше значит больше
