Книга: Происхождение жизни. От туманности до клетки
Получение нуклеотидов
| <<< Назад Химия цианидно-формальдегидных дождей |
Вперед >>> Цианосульфидный протометаболизм |
Получение нуклеотидов
Чтобы азотистые основания приняли участие в синтезе РНК-подобных полимеров, они должны, естественно, сначала объединиться с сахаром и фосфатом. Этот этап оказался гораздо сложнее, чем получение отдельных сахаров и азотистых оснований. Во-первых, такая реакция идет с выделением воды, и поэтому в водном растворе равновесие сдвинуто в сторону отдельных сахаров и азотистых оснований. Во-вторых, стандартные способы обхода такой проблемы – нагревание сухой смеси веществ или крепкого рассола – здесь не подходят. В этих условиях азотистые основания соединяются с рибозой, но не той стороной – связь с сахаром образует боковая аминогруппа, а не атом азота из кольца. Аденин и гуанин можно соединить с рибозой правильным способом, облучая ультрафиолетом водный раствор азотистых оснований и рибозы, но выход нужного нуклеозида не превышает 1 %, а с урацилом и цитозином этот способ вообще не работает. В клетках азотистые основания соединяются с рибозой правильно с помощью сложных ферментов, но нам надо как-то обойтись без них.
Чтобы решить эту проблему, ученые пошли другим путем. Если не удается правильно соединить готовые азотистые основания с рибозой, то можно попробовать создавать эту связь до того, как рибоза и азотистые основания будут достроены. Есть три возможных пути: строить азотистые основания на готовой рибозе, строить рибозу на готовом азотистом основании и строить и то и другое одновременно. Первый путь, кстати, используется в клетках для синтеза адениновых и гуаниновых нуклеотидов из простых предшественников. В экспериментах были достигнуты успехи на всех трех направлениях.
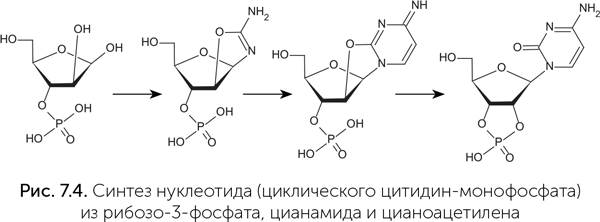
Так, если взять сухую смесь тех веществ, из которых в клетках образуется аденин (это три аминокислоты: глицин, глутамин, аспарагиновая кислота, а также соли муравьиной и фосфорной кислот и рибоза), и запекать ее при температуре 120–150 °C без доступа воздуха, то образуется нуклеотид аденозин-монофосфат с выходом 2–3 % и нуклеозид (азотистое основание с рибозой без фосфора) с выходом до 5 % (Kritsky et al., 2007). В водном растворе рибозо-3-фосфата при добавлении цианамида и цианоацетилена получается нуклеотид цитидин-монофосфат (рис. 7.4) (Ingar et al., 2003). В обоих этих случаях предшественники азотистого основания сначала реагируют с рибозой, а потом этот промежуточный продукт становится нуклеотидом.
Второй путь начинается с побочных продуктов синтеза азотистых оснований из формамида. Наряду с аденином, гуанином, цитозином и урацилом при этом получаются их формильные производные, имеющие альдегидную (CHO) группу на одном из атомов азота в кольце, чаще всего именно на том, который образует связь с сахаром в нуклеотидах. Эта группа может служить затравкой для построения сахара, если такое вещество (например, 9-формил-аденин) попадет в условия реакции Бутлерова – щелочную среду с формальдегидом. Все хитрости, которые позволяют получить в реакции Бутлерова именно рибозу, а не пригоревшую карамель, здесь тоже работают.
Наконец, возможность получения нуклеотидов по третьему пути, когда ни рибоза, ни азотистые основания не встречаются на промежуточных стадиях, была показана в 2009 году в работе Сазерленда с коллегами из Школы химии Манчестерского университета (см.: Клещенко Е. Реакция начала жизни // Химия и жизнь. 2009. № 7).
Они получили активированные пиримидиновые нуклеотиды (циклические 2',3'урацил– и цитидинмонофосфаты), смешивая в одной системе сразу и предшественники сахаров, и предшественники нуклеотидов, и фосфат. Казалось бы, это крайне расширяет круг возможных химических реакций, а значит, побочных продуктов должно быть больше. Но эксперимент опроверг это предположение.
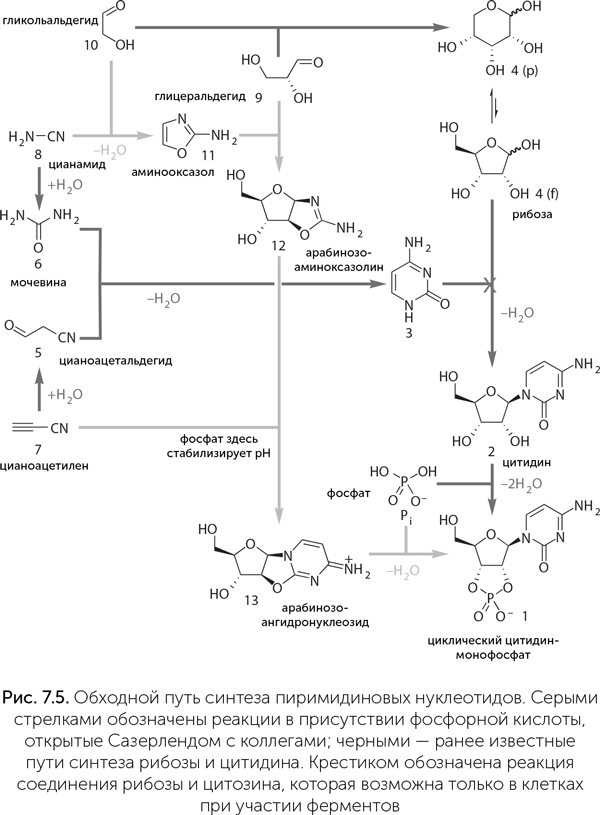
Авторы использовали цианоацетилен (на рис. 7.5 это № 7), цианамид (№ 8), глицеральдегид (№ 9) и гликольальдегид (№ 10). Фосфат облегчает реакции, приводящие в итоге к нуклеотидам, и подавляет другие, побочные. Так, он направляет реакцию цианамида с гликольальдегидом в сторону промежуточного продукта № 11 (2-аминооксазол), а затем реакцию его с глицеральдегидом с образованием продукта № 12 (арабинозо-аминооксазолин). Затем продукт № 12 реагирует с цианоацетиленом, давая вещество № 13 (арабинозо-ангидронуклеозид). В обычном водном растворе при этом повышается pH, и среда становится щелочной, что приводит к распаду промежуточных продуктов и побочным реакциям с цианоацетиленом, но фосфат и тут приходит на помощь, поддерживая среду кислой и направляя реакцию в сторону продукта № 13. Для его превращения в циклический цитидин-монофосфат достаточно подогреть реакционную смесь – все необходимое в ней уже имеется. Катализатором фосфорилирования становится мочевина, образующаяся из цианамида в ходе одной из побочных реакций. Наконец, чтобы избавиться от побочных продуктов этой реакции и превратить часть цитозина в урацил, достаточно осветить раствор ультрафиолетом.
Этот синтез поражает своим изяществом: побочные продукты одних реакций здесь становятся катализаторами последующих, фосфат направляет реакции в нужную сторону задолго до того, как войти в окончательный продукт, а ключевой промежуточный продукт (№ 11) способен к самоочищению и накоплению в высоких концентрациях благодаря своей высокой летучести – он хорошо испаряется из водных растворов при слегка повышенной температуре и конденсируется во время ночных заморозков.
Как написал редактор журнала Nature в предисловии к работе команды Сазерленда, «именно потому, что эта работа открывает так много новых направлений исследований, она на многие годы останется одним из великих достижений пребиотической химии».
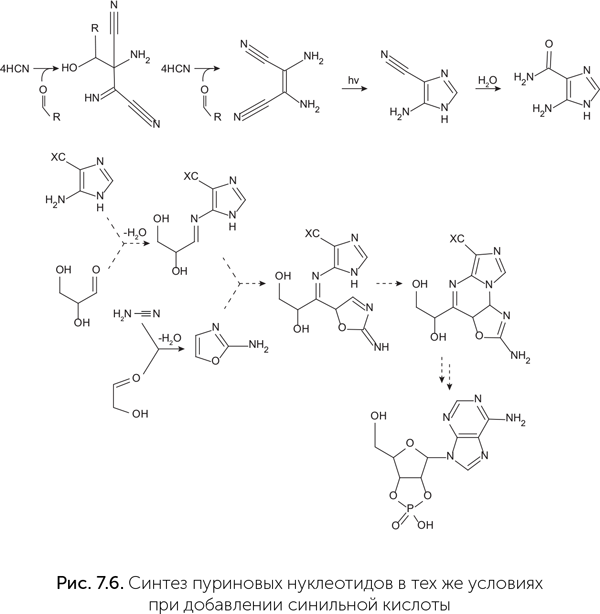
Вскоре в той же лаборатории аналогичным способом были получены и пуриновые нуклеотиды (циклические аденозин– и гуанозин-монофосфаты). Для этого оказалось достаточно добавить в систему синильную кислоту вместо цианоацетилена (рис. 7.6) (Powner et al., 2010).
| <<< Назад Химия цианидно-формальдегидных дождей |
Вперед >>> Цианосульфидный протометаболизм |
- Глава 7 Получение нуклеотидов из продуктов атмосферной фотохимии
- 8.35. ПОЛУЧЕНИЕ ФЕНОЛА — НЕЛЕГКАЯ ЗАДАЧА
- 120. Получение и применение галогенов.
- АЗОТ (NITROGENIUM)* 136. Азот в природе. Получение и свойства азота.
- Получение платины
- 126. Сера в природе. Получение серы.
- Получение крупногабаритных кристаллов
- 4. Ненормальные валерианы
- Часть II Происхождение жизни
