Книга: Основы геоэкологии
V.3. Деградация озонового слоя
| <<< Назад V.2.6. Стратегии, связанные с проблемой изменения климата |
Вперед >>> V.4. Асидификация экосферы и кислотные осадки |
V.3. Деградация озонового слоя
Максимальная концентрация озона сосредоточена в тропосфере на высотах 15–30 км, где существует так называемый озоновый слой. При нормальном, приземном давлении весь атмосферный озон образовал бы слой всего 3 мм толщиной. Для сравнения отметим, что толщина озона атмосферы при этих условиях была бы равна 8,3 км.
Озоновый слой тоньше в экваториальных районах и толще в полярных. Он отличается значительной изменчивостью во времени и по территории (до 20 %) вследствие колебаний солнечной радиации и циркуляции атмосферы, что маскирует антропогенные воздейстия.
Даже при столь малой мощности озоновый слой в стратосфере играет очень важную роль, защищая живые организмы Земли от вредного и даже губительного воздействия ультрафиолетовой радиации Солнца (UV). Озон поглощает ее жесткую часть, UVC, с длинами волн 100–280 нм (нанометров, или 10-9 м) и большую часть менее энергичной, но также опасной UVB радиации с длинами волн 280–315 нм. Менее активная часть спектра ультрафиолетовой радиации (более длинноволновая часть UVB и вся UVА с длинами волн 315–400 нм) озоном не абсорбируется и проникает в тропосферу (рис. 10).
С воздействием жесткой ультрафиолетовой радиации связаны неизлечимые формы рака кожи, болезни глаз, нарушения иммунной системы людей, неблагоприятные воздействия на жизнедеятельность планктона в океане, снижение урожая зерновых и другие экологические последствия.
Молекула озона (О3) состоит из трех атомов кислорода. Озон в стратосфере образуется в результате фотохимической диссоциации молекулярного кислорода под воздействием солнечной радиации с длиной волны менее 240 nm (hl < 240 nm). Этот процесс образует два атома кислорода, снова соединяющихся в молекулу, и две молекулы озона из трех молекул кислорода:
O2 + h? ? O + O
2 [O + O2 + M ? O3 + M],
где M – любая молекула (обычно азота или кислорода), у
носящая из реакции избыток энергии.
Поскольку кислород в атмосфере представлен почти исключительно как О2, ясно, что должны существовать процессы, реконвертирующие основную часть O3 в О2:
X + O3 ? XO + O2
03 + h? ? O + O2
O + XO ? X + O2
В итоге этой серии реакций две молекулы озона преобразуются в три молекулы кислорода. Здесь Х и ХО – это атомы или молекулы, катализирующие превращение озона в кислород. Голландский геохимик Пауль Крутцен в 1970 г. показал, что в естественных условиях наиболее важными катализаторами являются оксиды азота (NO и NO2). В свою очередь, они образуются вследствие окисления нитрита кислорода (N2O), происходящего на суше и в океанах главным образом вследствие естественных микробиологических процессов денитрификации или нитрификации. Тропические леса являются важным источником нитрита азота.
Напомним, что нитрит азота это также и газ, отличающийся заметным парниковым эффектом. В настоящее время деятельность человека (использование азотных удобрений, сжигание горючих ископаемых для производства энергии, преобразование ландшафтов, обычно сопровождающееся сжиганием биомассы и пр.) обеспечивает примерно 30–40 % от естественной эмиссии нитрита азота, и эта доля продолжает увеличиваться.
Предполагается, что жизнь на Земле возникла после образования в атмосфере Земли озонового слоя, когда сформировалась ее надежная защита. Понятно поэтому современное беспокойство за состояние озонового слоя. Основания для беспокойства имеются. Еще в 1974 г. американские геохимики Ш. Роуланд и М. Молина пришли к выводу о том, что возрастающее производство и применение хлорфторуглеродов (фреонов), ранее не существовавших в природе, неизбежно приведет к прогрессирующей деградации озонового слоя.
Семейство хлорфтор(бром)углеродов (ХФУ) насчитывает ряд сравнительно недорогих синтезируемых веществ. Более десятка из них нашли широкое применение как хладоносители (фреоны) в холодильниках и кондиционерах воздуха, а также в качестве растворителей, пенообразователей, распылителей (аэрозолей) в различных областях индустрии. ХФУ отличаются малой химической активностью и потому высокой продолжительностью существования в атмосфере. Эти свойства оказались вредными, когда стало ясно, что они играют решающую роль в разрушении озонового слоя.
Хлорфторуглероды представляют собой группу органических веществ, в которых все атомы водорода замещены на комбинацию атомов хлора, фтора и брома. Они чрезвычайно устойчивы в тропосфере, и потому по мере роста их использования происходило повышение их концентрации со скоростью до 5–6% в год. Со временем эти газообразные вещества перемещаются в стратосферу. На высоте около 25 км вследствие более высокой, чем в приземном слое, интенсивности солнечной радиации происходит их разрушение с выделением атомов хлора (Cl) и молекул моноксида хлора (ClO), которые являются более сильными катализаторами процесса разрушения молекул озона, чем оксиды азота:
Cl + O3 ? ClO + O2
ClO + O ? Cl + O2
При этом процессе каждый атом хлора может разрушить 105 молекул озона. Подобные реакции происходят и при участии атомов и соединений брома.
Приведенные выше химические реакции весьма схематично отражают процесс деградации озонового слоя. На самом деле такая деградация есть следствие нескольких сотен химических реакций в атмосфере, часть которых протекает с запаздыванием в 10–15 лет по сравнению со временем поступления данного вещества в атмосферу.
Расчеты демонстрируют весьма значительные неблагоприятные последствия деградации озонового слоя. Предположительно, потери озона достигнут 6–7% от его первоначального количества, что будет соответствовать увеличению среднего годового количества биологически вредной части УФ радиации на 6-12 %. Поэтому ожидается, например, что в США к середине XXI века будет на 100 000 больше случаев заболевания раком кожи по сравнению с 1960 г., а общее дополнительное количество заболевших достигнет трех миллионов.
Предупреждение Роуланда и Молины о грядушем разрушении озонового слоя с серьезнейшими последствиями для человечества хотя и было замечено как специалистами, так и политиками, но не вызвало солидных, согласованных действий на международном уровне. Вяло текли переговоры о подготовке международной конвенции по защите озонового слоя, которая в конце концов была заключена в Вене в 1985 г. Венская конвенция явилась фактически декларацией о необходимости международного сотрудничества в этой области, но не действенным инструментом для решения проблемы.
Однако в 1984 г. английским исследователем Д. Фарманом была обнаружена над Антарктидой область, соизмеримая со всем континентом, где содержание озона в атмосфере в октябре-ноябре было до 40 % ниже, чем в среднем (рис. 10). Это означало увеличение ультрафиолетовой радиации, достигающей земной поверхности в границах Антарктиды, приблизительно в десять раз по сравнению с обычным распределением УФР. Озоновая дыра над Антарктидой стала тревожным сигналом общепланетарного неблагополучия экосферы, требующего серьезного внимания всех стран мира.
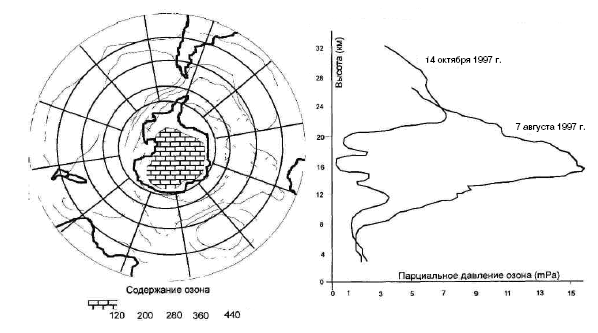
Рис. 10. Содержание озона в атмосфере над Антарктидой.
Слева – распределение суммарной концентрации озона весной Южного полушария. Справа – распределение концентрации озона в «нормальных» условиях (в августе) и при развитой «озоновой дыре» (в октябре)
Поэтому вскоре, в 1988 г., был подписан Монреальский протокол к Конвенции по защите озонового слоя, предусматривающий постепенное сокращение производства и употребления хлорфторуглеродов. Это был первый пример такого международного сотрудничества, которое направлено на решение будущей, только еще возникающей природно-антропогенной проблемы. Такое сотрудничество предполагает и значительные экономические вложения, потому что действия по защите озонового слоя означают также перестройку многих технологических процессов, при которых используются ХФУ.
В дальнейшем, после Монреаля, принимались дополнительные международные решения, связанные с еще более быстрым сокращением производства хлорфторуглеродов. Эти химические вещества отличаются, однако, продолжительным существованием в атмосфере, и поэтому, даже при соблюдении всеми странами принятых обязательств, проблема угрозы состоянию озонового слоя будет существовать по крайней мере в течение нескольких десятилетий.
Вследствие деятельности человека с конца 1960-х гг. до 1995 г. озоновый слой потерял около 5 % массы. Ожидается, что максимум потерь стратосферного озона будет достигнут к концу XX в., с последующим постепенным восстановлением в течение первой половины XXI века. Антарктическая «озоновая дыра» формируется ежегодно в сентябре-октябре. В настоящее время в октябре среднее содержание озона на 50–70 % меньше, чем в 1960-х гг. Во время развития «дыры» величина ультрафиолетовой радиации в Антарктиде на широте 64° ю. ш. больше летнего максимума в Сан-Диего (Калифорния) на широте 32° с. ш. Иными словами, антропогенное распределение озона начало превалировать над его природным распределением. Подобные, менее устойчивые «дыры» были обнаружены позднее и в других районах мира. Статистически значимые потери общего озона наблюдаются и в средних широтах обоих полушарий. В экваториальном поясе (20° с. ш. – 20° ю. ш.) значительного снижения содержания озона не отмечено.
Вследствие высокого парникового эффекта хлорфторуглеродов эти вещества вносят и будут продолжать вносить заметный вклад в изменение климата в течение значительного времени.
Вследствие антропогенной деятельности в нижних слоях атмосферы накапливается тропосферный озон, значительный загрязнитель атмосферы и активный парниковый газ. Его территориальное распределение очень изменчиво, а масса составляет не более 10 % массы стратосферного озона. Под воздействием солнечной радиации оксиды азота, выделяемые главным образом автомобильным транспортом, распадаются с выделением озона. Образуется так называемый фотохимический смог, опасный для здоровья человека и наносящий серьезный ущерб растениям, в том числе сельскохозяйственным культурам. Выражение «смог» – это комбинация двух английских слов: smoke – дым и fog – туман. Это явление проявилось уже в середине 1940-х гг. в Лос-Анджелесе, где жизнь людей была практически невозможна без личного автомобильного транспорта, а общественного транспорта не существовало.
Исследования проблемы озонового слоя получили заслуженно высокую оценку. В 1995 г. Шервуд Роуланд, Марио Молина и Пауль Крутцен за исследования химических процессов в экосфере, связанных с озоновым слоем, были удостоены Нобелевской премии по химии. Это первая Нобелевская премия за исследования проблем геоэкологии.
| <<< Назад V.2.6. Стратегии, связанные с проблемой изменения климата |
Вперед >>> V.4. Асидификация экосферы и кислотные осадки |
