Книга: Популярная библиотека химических элементов. Книга первая. Водород — палладий
Водород и практика
| <<< Назад Водород и наука |
Вперед >>> Водород и будущее |
Разделы на этой странице:
Водород и практика
Сразу же оговоримся: в отличие от «науки», как области чистых идей, «практикой» мы назовем все, что служит практической деятельности человека — пусть это даже будет деятельность ученого-экспериментатора.
Химик имеет дело с водородом прежде всего как с веществом, обладающим свойствами идеального восстановителя.
Но откуда взять водород? Конечно, проще всего из баллона. Из зеленого баллона с красной надписью «Водород» и с вентилем с «левой» резьбой (горючий газ!). Но если баллона под руками нет?
Водород можно получать взаимодействием металлов с кислотами:
Zn + H2SO4 ? ZnSO4 + Н2?.
Но этот водород не может быть идеально чистым, потому что нужны идеально чистые металл и кислота. Чистый водород получал еще Лавуазье, пропуская пары воды через раскаленный на жаровне ружейный ствол:
4Н2O + 3Fe — Fe3O4 + 4 Н2?.
Но и этот способ не слишком удобен, хотя в современной лаборатории можно обойтись кварцевой трубкой, наполненной железными стружками и нагреваемой в электропечи.
Электролиз! Дистиллированная вода, в которую для повышения электропроводности добавлено немного серной кислоты, разлагается при прохождении постоянного тока:
2Н2O ? 2Н2? + O2?.
К вашим услугам — водород почти идеальной чистоты, его нужно только освободить от мельчайших капелек воды. (В промышленности в воду добавляют щелочь, а не кислоту — чтобы не разрушалась металлическая аппаратура.)
А теперь будем медленно пропускать этот водород через воду, в которой взмучен хлористый палладий. Почти сразу начнется восстановление, и осадок почернеет — получится палладиевая чернь
PdCl2 + H2 ? Pd + 2HCl.
Палладиевая чернь — прекрасный катализатор для гидрирования разнообразных органических соединений. А катализатор тут нужен потому, что молекулярный водород весьма инертен: даже с кислородом при обычных условиях он реагирует необычайно медленно. Ведь сначала молекула водорода должна диссоциировать на атомы, а для этого на каждый моль водорода (т. е. всего на 2 г!) нужно затратить 104 ккал. А вот на поверхности катализатора этот процесс идет с гораздо меньшими затратами энергии, водород резко активизируется.
Пожалуй, не стоит много говорить о роли катализаторов в современной химической технологии: в их присутствии проводится подавляющее большинство процессов. И важнейший среди них — синтез аммиака из водорода и атмосферного азота:
3Н2 + N2 ? 2NH3.
При этом водород добывают или из воды и метана по так называемой реакции конверсии
CH4 + 2Н2O ? 4Н2 + CO2,
или расщепляя природные углеводороды по реакции, обратной реакции гидрирования:
CH3—CH3 ? CH2=CH2 + H2.
Синтетический аммиак незаменим в производстве азотных удобрений. Но водород нужен не только для получения аммиака. Превращение жидких растительных жиров в твердые заменители животного масла, преобразование твердых низкокачественных углей в жидкое топливо и многие другие процессы происходят с участием элементного водорода. Выходит, что водород — это пища и для человека, и для растений, и для машин…
Но вернемся в лабораторию. Здесь водород применяют не только в чистом виде, но и в виде его соединений с металлами — например алюмогидрида лития LiAlH4, боргидрида натрия NaBH4. Эти соединения легко и специфически восстанавливают определенные группировки атомов в органических веществах:
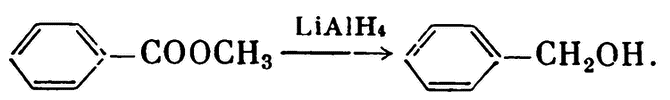
Изотопы водорода — дейтерий (2H или D) и тритий (3H или Т) — позволяют изучать тончайшие механизмы химических и биохимических процессов. Эти изотопы используют как «метки», потому что атомы дейтерия и трития сохраняют все химические свойства обычного легкого изотопа — протия — и способны подменять его в органических соединениях. Но дейтерий можно отличить от протия по массе, а тритий — и по радиоактивности. Это позволяет проследить судьбу каждого фрагмента меченой молекулы.
| <<< Назад Водород и наука |
Вперед >>> Водород и будущее |
- Водород и будущее
- 3. ВОДОРОД
- Построение структурных формул. Углеводороды.
- 669. Какое воздействие оказывает сероводород?
- 668. Почему у дна Черного моря скапливается сероводород?
- Юпитер. Жестокий, злой и водородный
- Теория и практика
- 3. Водородная гипотеза
- Вводные к водороду
- ДНК и водородная бомба
- Сложная практика дегустации вина
- Практика смирения
