Книга: Логика случая. О природе и происхождении биологической эволюции
Неклеточный компартментализированный LUCA(S): сообщество разнородных репликаторов и лаборатория ранней эволюции
| <<< Назад Сравнительно-геномная реконструкция генного репертуара LUCA |
Вперед >>> Краткий обзор и перспектива |
Неклеточный компартментализированный LUCA(S): сообщество разнородных репликаторов и лаборатория ранней эволюции
Майкл Рассел и коллеги предположили, что сети микроячеек в современных и древних гидротермальных источниках, состоящие в основном из сульфида железа, могли быть идеальной средой обитания для ранней жизни (Martin and Russell, 2003; Russell, 2007). Эти сети неорганических ячеек обеспечивают градиенты температуры и рН, способствующие первичным реакциям, и предоставляют универсальные каталитические поверхности для примитивной биохимии[117]. Подробности устройства этой среды остаются предметом исследований и споров (некоторые частности разбираются в гл. 12), но мало кто сомневается, что такие сети неорганических ячеек подходят на роль инкубаторов добиологической и доклеточной биологической эволюции, от смеси органических молекул к предполагаемому изначальному миру РНК и далее до происхождения клеток, выходящих из ячеек (см. рис. 11-2). Эти отсеки могли быть населены самой разнородной популяцией генетических элементов, вначале сегментами РНК, затем более крупными и сложными молекулами РНК, включающими один или несколько белок-кодирующих генов, а еще позже – также и сегментами ДНК постепенно увеличивающегося размера (см. рис. 11-2).
Таким образом, ранние формы жизни, возможно включая LUCA(S), рассматриваются как сложные ансамбли генетических элементов, населявшие сети неорганических ячеек. Главная особенность этой модели состоит в том, что все стратегии репликации и экспрессии, использующиеся современными вирусами (см. рис. 10-1), и, соответственно, генетические элементы, кодирующие все разнообразные механизмы репликации и экспрессии, эволюционировали одновременно и в конечном итоге сосуществовали в сети, в некоторых случаях в одной и той же ячейке. Таким образом, ранняя, несколько искусственная схема, где универсально консервативные компоненты механизма репликации ДНК были вовлечены в первичный цикл репликации ретровирусного типа (Leipe et al., 1999), становится ненужной.
Рассматриваемая модель объясняет отсутствие гомологии между мембранами, системами мембранного биогенеза и механизмами репликации ДНК архей и бактерий тем, что LUCA(S) не имел единого большого ДНК-генома и не был типичной клеткой, ограниченной мембраной. Согласно этой модели, первичные, доклеточные, «коммунальные» формы жизни рассматриваются как «лаборатории», в которых были «изобретены» и опробованы различные стратегии репликации и экспрессии генома, а также рудиментарные формы биогенной компартментализации (см. рис. 11-2 и обсуждение далее в этой главе).
Главным пунктом этого сценария ранней эволюции жизни является вирусоподобная природа предполагаемой доклеточной жизни. В соответствии с этой моделью, жизнь началась как первичный вирусный мир. Как уже упоминалось в главе 10, мысль о том, что вирусы могли быть соотнесены с первыми формами жизни, почти так же стара, как сама вирусология. Следуя умозрительным предположениям д’Эрреля, Холдейн выдвинул эту точку зрения в более определенной форме в своем классическом эссе 1928 года о происхождении жизни (Haldane, 1928). Со своей неизменной и поразительной способностью к предвидению Холдейн предположил, что первые самовоспроизводящиеся агенты были вирусами или чем-то похожим на вирусы и что вирусный этап в эволюции жизни предшествовал появлению клеток: «Жизнь, возможно, пребывала в вирусной стадии многие миллионы лет, прежде чем подходящие совокупности элементарных частей объединились в первую клетку». Впоследствии, однако, идея изначального происхождения вирусов и более смелая идея первичного вирусного этапа в эволюции жизни была фактически отброшена, когда стало ясно, что вирусы – облигатные внутриклеточные паразиты, большинство функций которых зависимы от клетки-хозяина. Ее место в концепциях о происхождении и эволюции вирусов, как обсуждалось в главе 10, заняли сценарии клеточной дегенерации и беглых клеточных генов.
Вирусологический ренессанс в первом десятилетии третьего тысячелетия привел к распространению гипотез и моделей, основанных на идее о важном вкладе вирусов в происхождение и эволюцию клеток. По сценарию «трех РНК-клеток и трех ДНК-вирусов» П. Фортера, современные, основанные на ДНК клетки возникли, когда три различных ДНК-вируса заменили первоначальный РНК-геном в трех клеточных линиях (предках бактерий, архей и эукариот соответственно; Forterre, 2006). Сами эти ДНК-вирусы, по предположению Фортера, эволюционировали как паразиты первичных РНК-клеток. Однако, как уже говорилось в этой главе, гипотеза РНК-клетки вряд ли жизнеспособна. Более правдоподобный сценарий, который, возможно, примиряет выводы сравнительной геномики и общую логику доклеточной эволюции, возрождает идею Холдейна на новом уровне и включает эволюцию различных вирусоподобных элементов и даже вирусоподобных частиц, предшествующую появлению клеток современного типа.
Проблема возникновения клеток наиболее ярко отражает те трудности, с которыми сталкиваются все объяснения эволюции сложных биологических структур (см. гл. 8). Действительно, среди современных биологических объектов мы не видим никаких промежуточных форм между макромолекулами и клетками, и представление о том, какими были и как работали такие промежуточные структуры, является огромной проблемой. Как мы уже неоднократно отмечали в настоящей книге, наименьшая клетка, не являющаяся паразитом или воспроизводящимся внутри других клеток симбионтом, должна нести по меньшей мере 400 генов, в то время как автотрофные клетки вряд ли могут существовать с геномом менее 1000 генов. Эти гены находятся на одной большой хромосоме (в большинстве прокариот) или на нескольких меньших хромосомах и (или) крупных плазмидах (в меньшем числе бактерий и архей), но никогда на сегментах ДНК размером порядка оперона или гена. Фактор отбора, направляющий эволюцию к большим, протяженным геномам прост, если мы вспомним постулат Вирхова omnis cellula e cellula: эволюционирующей клетке требуется точно раздваивать геном, что практически немыслимо с геномом, состоящим из сотен сегментов. Эта эволюционная логика подсказывает, что первые клетки на самом деле должны были иметь одну хромосому, и не только потому, что это так для большинства современных архей и бактерий, но, что более важно, из-за вероятной простоты и сравнительной неточности древнего механизма клеточного деления. Эволюционный рост сложных геномов, кодирующих наименьший комплект генов, необходимых для деятельности клетки, требует некоей разновидности первичной, абиогенной компартментализации, не требующей сложного мембранного аппарата современной клетки. Эту сложность не следует недооценивать: напомним, что все клеточные мембраны являются не только сложно организованными транспортными устройствами, но и машинами по преобразованию энергии, превращающими разность электрохимических потенциалов (протонный или натриевый градиент) в химическую энергию АТФ[118].
В настоящее время серьезно рассматриваются две формы первичной, абиогенной компартментализации: липидные везикулы и сети неорганических ячеек. Сценарий липидных везикул привлекателен тем, что в нем абиогенные мембраны являются прямыми предками современных биологических мембран. Эта возможность в настоящее время широко изучается экспериментально, в первую очередь в лаборатории Джека Шостака, и были получены интересные результаты в области транспорта полярных соединений, в том числе нуклеотидов, через липидные мембраны (Mansy et al., 2008). Однако трудности, с которыми сталкивается эта модель, остаются очень большими. Эти проблемы достаточно очевидны и включают в себя не только транспорт мономеров со скоростями, достаточными для поддержания репликации и трансляции генетических элементов до появления белковых транспортеров, но и создание и поддержание мембранного потенциала для производства энергии. Кроме того, везикулярная модель, по-видимому, не способствует интенсивному ГПГ, важному аспекту всей микробной эволюции, но особенно необходимому на доклеточной стадии.
Не отказывая модели липидных везикул в потенциальной важности, рассмотрим модель происхождения клеток из вирусного мира как начального состояния, эволюционирующего в сетях неорганических ячеек. Эта модель, возможно, встречает меньше проблем, чем модель липидных везикул, и содержит ряд привлекательных черт, в том числе возможный ключ к разгадке происхождения биологических мембран и биоэнергетики. Как и биологическая эволюция в целом, доклеточная эволюция, несомненно, обусловливалась сочетанием случайного дрейфа и естественного отбора. Возможности для дрейфа изобилуют в рамках этой модели; пожалуй, самым простым и очевидным примером будет «засев» пустой ячейки случайным генетическим элементом. Отбор сразу же выходит на сцену с появлением репликаторов (см. гл. 2) – первоначально, как сейчас предполагается, молекул РНК, реплицируемых рибозимами, а впоследствии, после появления трансляции, молекул РНК, реплицирующихся с помощью белков (см. гл. 12). Одним из центральных аспектов модели вирусоподобной компартментализированной доклеточной стадии эволюции является постепенный переход от отбора на уровне отдельных генетических элементов к отбору ансамблей таких элементов[119], кодирующих ферменты, непосредственно участвующие в репликации, а также белки, отвечающие за вспомогательные функции, такие как трансляция и синтез предшественников нуклеиновых кислот. Отбор на уровне ансамблей генетических элементов, очевидно, является одной из форм группового отбора, который сам по себе является предметом давних споров среди биологов-эволюционистов и иногда отбрасывается как выдумка. Не вдаваясь глубоко в теоретические построения, отметим, что начальная эволюция, от малых генетических элементов к большим геномам, сравнимым с геномами современных клеточных форм жизни, не представляется возможной без группового отбора в той или иной форме (Koonin and Martin, 2005). Исследуя математические модели, Э. Сатмари с коллегами продемонстрировали возможность группового отбора в ансамблях репликаторов, самовоспроизводящихся в разделенной на ячейки среде (Fontanari et al., 2006; Szathmary and Demeter, 1987). Некоторые из решений, возможно доступных ансамблям «эгоистичных кооператоров», известны из теории группового отбора. Наиболее очевидным и важным представляется взаимный альтруизм, когда члены группы реализуют взаимодополнительные функции, стимулирующие репродукцию друг друга[120]. Так, в первичном ансамбле генетический элемент, кодирующий репликазу, катализировал бы репликацию элементов, кодирующих, например, компоненты систем трансляции и синтеза предшественников, – то есть функции, способствующие его собственной репликации.
Ансамбли эгоистичных кооператоров могли возникать двумя (отнюдь не взаимоисключающими) путями: (1) физическим соединением генетических элементов и (2) компартментализацией. Первый путь представляет собой начало эволюции оперонов, включая супероперон, включающий гены рибосомых белков и субъединиц РНК-полимеразы, единственный массив генов, в значительной степени сохраненный между археями и бактериями (см. гл. 5). Путь компартментализации включает эволюцию вирусоподобных частиц, которые могли содержать достаточно стабильные наборы сегментов генома, напоминающие ныне существующие сегментированные РНК-вирусы. В отличие от клеток, вирусоподобные частицы с малыми геномами, в особенности широко распространенные икосаэдрические (сферические) капсиды, являются простыми симметричными структурами, которые во многих случаях формируются путем самосборки единственного белка капсида. Таким образом, весьма привлекательна идея о том, что простые вирусоподобные частицы были первой формой настоящей, биологической компартментализации и играли большую роль на доклеточной стадии эволюции. В дополнение к преимуществам компартментализации, вирусоподобные частицы могут защитить генетические элементы (особенно РНК) от деградации и могут служить транспортом для перемещения генов между ячейками и сетями.
Большая часть сферических вирусов с относительно сложными геномами обладает молекулярными механизмами для упаковки ДНК и РНК внутри капсида; по крайней мере в некоторых случаях эти молекулярные механизмы работают и в обратном направлении, обеспечивая экспорт вирусных транскриптов из капсидов (Rao and Feiss, 2008). Вирусные механизмы упаковки и экспорта используют моторные АТФазы как минимум трех известных семейств, которые, по-видимому, имеют общую архитектуру, формируя гексамерные каналы, по которым активно (то есть за счет энергии гидролиза АТФ) перемещаются молекулы ДНК или РНК. Примечательно, что одна из групп вирусных упаковочных АТФаз является ветвью суперсемейства FtsK-HerA, которое также включает в себя прокариотические АТФазы, ответственные за транспорт ДНК в дочерние клетки во время клеточного деления, в то время как другое семейство сходно с двигательными АТФазами бактериальных нитей (pili) (Iyer et al., 2004b). В имеющих мембраны вирионах многих вирусов аппарат упаковки перемещает ДНК и РНК как сквозь капсид, так и сквозь липидную мембрану вириона. Заманчиво предположить, что вирусные механизмы упаковки были эволюционными предшественниками клеточных насосов и двигательных АТФаз. H+(Na+) – АТФазы/АТФ-синтазы, важнейшие, универсальные мембранные ферменты, краеугольный камень современной клеточной энергетики, также образуют подобные гексамерные каналы и, возможно, появились как часть механизма упаковки и экспорта в некоем, до сих пор не описанном (возможно, вымершем) классе вирусоподобных агентов.
Мембраны ионных градиентно-зависимых АТФ-синтаз представляют собой удивительный молекулярный «электродвигатель», роторный мотор, который переводит ионный градиент в механическую энергию вращения, а затем в химическую энергию ?-?-фосфодиэфирной связи АТФ. Анализ методами сравнительной геномики заставляет предположить, что предки двух основных ветвей мембранных АТФаз/синтаз, так называемые F-АТФазы, как правило обнаруживаемые в бактериях (и в эндосимбиотических органеллах эукариот), и V-АТФазы, характерные для архей и эндомембранных систем эукариот, произошли от общего предка, который функционировал как транслоказа белков или РНК (Mulkidjanian et al., 2007).
В предложенном эволюционном сценарии стадия транслоказы предваряет расхождение ветвей бактерий и архей, но мембранные АТФ-синтазы как таковые существенно различаются у архей и бактерий и, возможно, возникли дважды, независимо в разных ветвях клеточной жизни. Эти аналогии позволяют устремиться еще дальше в доклеточное эволюционное прошлое и предположить происхождение этой древней транслоказы от РНК-геликазы и мембранной поры или канала (см. рис. 11-3). Реконструкция эволюции мембранной АТФ-синтазы является основой для определения последовательности доклеточной эволюции: широкая диверсификация ферментов, содержащих петлю связывания фосфата (P-loop; см. гл. 12), которая породила, кроме множества АТФаз, еще и отдельное семейство РНК-геликаз (включающих бактериальный фактор терминации транскрипции Rho), произошла еще до развития мембранной энергетики, по крайней мере в той ее форме, которая наблюдается в современных клетках.
Весьма привлекательной кажется мысль о том, что, возможно, древнейшие вирусные мембраны могли быть промежуточными шагами в эволюции биологической компартментализации, что относит вглубь по исторической шкале время появления полноценных клеточных мембран. Действительно, в эволюции современных сложных мембран есть парадокс. Мембраны всех современных клеток являются исключительно изощренными устройствами: двойной липидный слой непроницаем даже для небольших молекул, а перенос молекул между внутриклеточным пространством клетки и внешним миром происходит при помощи мембранных белковых комплексов, таких как каналы, поры, транслоказы и вышеупомянутые градиент-зависимые АТФазы, ответственные за клеточную энергетику. Мембрана – это еще одна сложнейшая система, понимание происхождения которой сталкивается с классической дарвиновской проблемой: жизнеспособные промежуточные стадии сложно себе представить. «Дырявая» мембрана не может обеспечить целостность клеточного содержимого, в то время как непроницаемая мембрана будет бесполезна, поскольку не позволит импортировать строительные блоки для репликации. Вирусоподобные частицы могут разрешить этот парадокс, поскольку они получают выгоду от непроницаемой мембраны, если вирион снабжен транслоказой нуклеиновой кислоты[121]. Подобно тому как репликацию генома вирусоподобных объектов можно рассматривать как изначальный полигон для отработки репликационных стратегий, две из которых впоследствии были вовлечены в две основных линии клеточной жизни, вирусные частицы могли быть «лабораторией» для отработки молекулярных устройств, которые в дальнейшем встроились в мембраны развивающихся клеток.
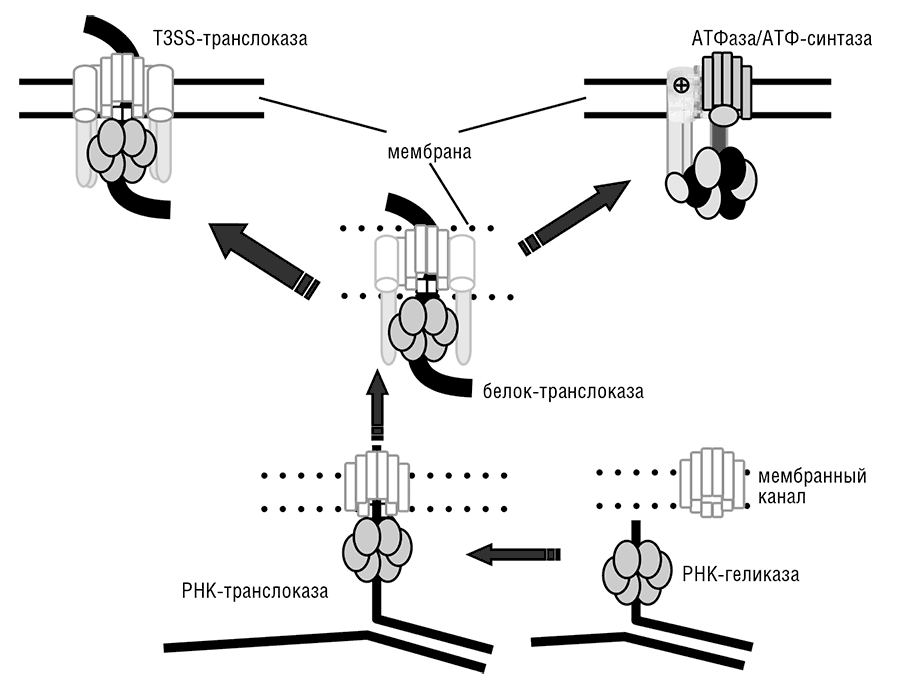
Рис. 11-3. Модель эволюции молекулярных моторов и мембранной биоэнергетики: от РНК-геликазы и мембранного канала к РНК-белковой транслоказе, и далее к ионно-градиентной АТФ-синтазе. Сплошные линии показывают современные непроницаемые для ионов мембраны, прерывистые линии показывают гипотетические «протекающие» древние мембраны. Изогнутая стрелка показывает утечку катионов из клетки. T3SS – система секреции типа 3, белковая транслоказа, распространенная у современных бактерий. В белковых транслоказах центральную позицию временно занимает перемещаемый белок, в то время как в мембранных АТФазах эту позицию занимают соответствующие белковые субъединицы. Сценарий эволюции взят из Mulkidjanian et al., 2007.
От отбора генных ансамблей прямая дорога к отбору содержимого ячеек, когда ячейки, поддерживающие быструю репликацию, «заражают» смежные ячейки и фактически распространяют свои коллективные «геномы»; первичные вирусоподобные частицы могли содействовать этому процессу (Koonin and Martin, 2005). Доклеточный эквивалент ГПГ – перенос генетического содержимого между ячейками – тоже часть этой модели, в согласии с идеей о том, что массовый ГПГ был неотъемлемой частью ранней стадии эволюции жизни. После того как в ходе эволюции эгоистичных кооператоров в сети неорганических ячеек был достигнут определенный уровень сложности, стал возможен «побег» протоклеточных организмов, имеющих сравнительно большие ДНК-геномы и мембраны, содержащие механизмы транспорта и транслокации (изначально развившиеся, согласно модели, в вирусоподобных агентах). Нельзя сказать, как много подобных попыток провалилось моментально и сколько продержалось дольше, но только археи и бактерии (согласно симбиотическому сценарию более позднего возникновения эукариот, как описано в гл. 7) дожили до сегодняшнего дня. Первый успешный «побег» клеточной жизни из гипотетического доклеточного «супа» соответствует дарвиновскому порогу клеточной эволюции, описанному Вёзе, – порогу, за которым ГПГ должен был существенно сократиться и начаться эволюция отдельных линий (видов) клеточных организмов (Woese, 2002).
Как и в других моделях ранних стадий эволюции биологической сложности и, возможно, даже более явно, сценарий «первобытного вирусного мира», описанный здесь, сталкивается с проблемой победы эгоистичных элементов. В главе 10 мы говорили о том, что появление паразитов – черта, присущая любой эволюционирующей системе репликаторов. Если бы первобытные паразиты стали слишком агрессивными, они могли бы уничтожать своих хозяев внутри ячейки и далее выживать, только инфицируя следующую ячейку (где они снова представляли бы опасность). Можно вообразить разрушительную «пандемию», прокатившуюся по всей сети и уничтожившую все ее содержимое, и, скорее всего, именно такой была судьба многих, если не большинства, первобытных «организмов». Примечательно, что математическое моделирование репликаторов заставляет предполагать, что важной движущей силой, определившей появление ДНК, которая привела к разделению роли матрицы и катализаторов на доклеточной стадии эволюции, могла быть повышенная сопротивляемость паразитов в системах со специализированными, выделенными матрицами (Takeuchi et al., 2011). Условием для выживания доклеточных форм жизни было, во-первых, появление умеренных паразитов, которые не убивали хозяина, и, во-вторых, эволюция защитных механизмов, вероятнее всего основанных на РНК-интерференции. Повсеместное распространение умеренно эгоистичных элементов и защитных систем, основанных на РНК-ин терференции, во всех ветвях клеточной жизни наводит на мысль, что эти явления появились на очень ранней, даже, возможно, доклеточной стадии эволюции.
Согласно этому сценарию, в первобытном генетическом резервуаре не существовало четко очерченных границ между эгоистичными генными элементами, которые позже стали вирусами, и большими генными ансамблями, которые в дальнейшем дали начало геномам клеточных форм жизни, хотя расхождение этих двух форм началось, когда паразиты начали «кормиться» на ансамблях «эгоистичных кооператоров». Появление клеток стало и настоящим началом мира вирусов, каким мы представляем его сегодня.
Модель доклеточной эволюции в первобытном вирусном мире, обрисованная здесь, предлагает, по-видимому, правдоподобные, хотя и весьма умозрительные решения многих загадок, связанных с происхождением клеток. Сравнительная геномика вирусов и других эгоистичных элементов дает, как мне кажется, серьезную эмпирическую поддержку этой модели. Учитывая, что, согласно такому сценарию, первые клетки произошли из неклеточного предкового состояния в ходе множественных независимых случаев возникновения протоклеток, кажется осмысленным говорить не о едином предке всех живых форм (LUCA), а о предковом состоянии (LUCAS), описывающем первобытный резервуар вирусоподобных генетических элементов.
| <<< Назад Сравнительно-геномная реконструкция генного репертуара LUCA |
Вперед >>> Краткий обзор и перспектива |
- Сравнительно-геномная реконструкция генного репертуара LUCA
- Какие мембраны были у LUCA?
- Глава 1. Теории прогрессивной эволюции
- ГЛАВА 6. ЖЕРТВЫ ЭВОЛЮЦИИ
- Семейные отношения — ключ к пониманию нашей эволюции
- Глава V ПОНЯТИЕ ОБ ЭВОЛЮЦИИ. ПАЛЕОНТОЛОГИЧЕСКАЯ ЛЕТОПИСЬ
- Глава 3. Факторы микроэволюции
- Y-хромосома – двигатель эволюции
- Глава 6. Направленность эволюции
- Пути эволюции предопределены на молекулярном уровне
- Сообщество превращается в организм
- В начале было сообщество?
