Книга: Популярная библиотека химических элементов. Книга вторая. Серебро — нильсборий
Распространенность цезия в природе и его производство
| <<< Назад ЦЕЗИЙ |
Вперед >>> Свойства цезия |
Разделы на этой странице:
Распространенность цезия в природе и его производство
В литературе нет точных данных о том, сколько цезия имеется на земном шаре. Известно лишь, что он относится к числу редких химических элементов. Полагают, что его содержание в земной коре во всяком случае в несколько сот раз меньше, чем рубидия, и не превышает 3,7?10-4%.
Цезий встречается в крайне рассеянном состоянии (порядка тысячных долей процента) во многих горных породах; ничтожные количества этого металла были обнаружены и в морской воде. В большей концентрации (до нескольких десятых процента) он содержится в некоторых калиевых и литиевых минералах, главным образом в лепидолите. Но особенно существенно то, что, в отличие от рубидия и большинства других редких элементов, цезий образует собственные минералы — поллуцит, авогадрит и родицит. Родицит крайне редок, притом некоторые авторы причисляют его к литиевым минералам, так как в его состав (R2O?2Al2O3?3B2O3, где R2O — сумма окисей щелочных металлов) входит обычно больше лития, чем цезия. Авогадрит (К, Cs)[BF4] тоже редок, да и поллуциты встречаются нечасто; их залежи маломощны, зато цезия они содержат не менее 20, а иногда и до 35%. Наибольшее практическое значение имеют поллуциты США (Южная Дакота и Мэн), Юго-Западной Африки, Швеции и Советского Союза (Казахстан и др.).
Поллуциты — это алюмосиликаты, сложные и весьма прочные соединения. Их состав определяют формулой (Cs, Na)[AlSi2O6]?AlH2O, и хотя цезия в них много, извлечь его не так просто. Чтобы «вскрыть» минерал и перевести в растворимую форму ценные компоненты, его обрабатывают при нагревании концентрированными минеральными кислотами — плавиковой или соляной и серной. Затем освобождают раствор от всех тяжелых и легких металлов и, что особенно трудно, от постоянных спутников цезия — щелочных металлов: калия, натрия и рубидия.
Современные методы извлечения цезия из поллуцитов основаны на предварительном сплавлении концентратов с избытком извести и небольшим количеством плавикового шпата. Если вести процесс при 1200°C, то почти весь цезий возгоняется в виде окиси Cs2O. Этот возгон, конечно, загрязнен примесью других щелочных металлов, но он растворим в минеральных кислотах, что упрощает дальнейшие операции.
Из лепидолитов цезий извлекается вместе с рубидием попутно, как побочный продукт производства лития. Лепидолиты предварительно сплавляют (или спекают) при температуре около 1000°C с гипсом или сульфатом калия и карбонатом бария. В этих условиях все щелочные металлы превращаются в легкорастворимые соединения — их можно выщелачивать горячей водой. После выделения лития остается переработать полученные фильтраты, и здесь самая трудная операция — отделение цезия от рубидия и громадного избытка калия. В результате ее получают какую-либо соль цезия — хлорид, сульфат или карбонат. Но это еще только часть дела, так как цезиевую соль надо превратить в металлический цезий. Чтобы понять всю сложность последнего этапа, достаточно указать, что первооткрывателю цезия — крупнейшему немецкому химику Бунзену — так и не удалось получить элемент № 55 в свободном состоянии. Все способы, пригодные для восстановления других металлов, не давали желаемых результатов. Металлический цезий был впервые получен только через 20 лет, в 1882 г., шведским химиком Сеттербергом в процессе электролиза расплавленной смеси цианидов цезия и бария, взятых в отношении 4: I. Цианид бария добавляли для снижения температуры плавления. Однако барий загрязнял конечный продукт, а работать с цианидами было трудно ввиду их крайней токсичности, да и выход цезия был весьма мал. Более рациональный способ найден в 1890 г. известным русским химиком Н.Н. Бекетовым, предложившим восстанавливать гидроокись цезия металлическим магнием в токе водорода при повышенной температуре. Водород заполняет прибор и препятствует окислению цезия, который отгоняется в специальный приемник. Однако и в этом случае выход цезия не превышает 50% теоретического.
Наилучшее решение трудной задачи получения металлического цезия было найдено в 1911 г. французским химиком Акспилем. При методе Акспиля, до сих пор остающемся наиболее распространенным, хлорид цезия восстанавливают металлическим кальцием в вакууме, причем реакция
2CsCl + Ca ? CaCl2 + 2Cs
идет практически до конца. Процесс ведут в специальном приборе (в лабораторных условиях — из кварца или тугоплавкого стекла), снабженном отростком. Если давление в приборе не больше 0,001 мм рт. ст., температура процесса может не превышать 675°C. Выделяющийся цезий испаряется и отгоняется в отросток, а хлористый кальций полностью остается в реакторе, так как в этих условиях летучесть соли ничтожна (температура плавления CaCl2 равна 773°C, т. е. на 100°C выше температуры процесса). В результате повторной дистилляции в вакууме получается абсолютно чистый металлический цезий.
В литературе описаны еще многие другие способы получения металлического цезия из его соединений, но, как правило, они не сулят особых преимуществ. Так, при замене металлического кальция его карбидом температуру реакции приходится повышать до 800°C, и конечный продукт загрязняется дополнительными примесями. Можно разлагать азид цезия или восстанавливать цирконием его бихромат, но эти реакции взрывоопасны. Впрочем, при замене бихромата хроматом цезия процесс восстановления протекает спокойно, и, хотя выход не превышает 50%, отгоняется очень чистый металлический цезий. Этот способ применим для получения небольших количеств активнейшего металла в специальном вакуумном приборе.
Мировое производство цезия сравнительно невелико, но в последнее время оно постоянно растет. О масштабах этого роста можно только догадываться — цифры не публикуются.
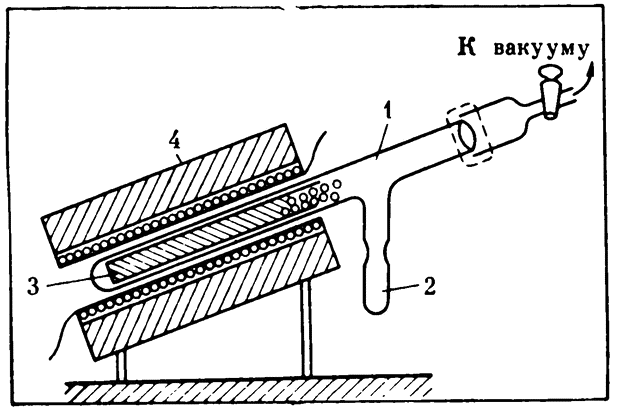
Схема прибора Акспиля для получения металлического цезия восстановлением его хлорида
1 — стеклянная трубка длиной 30–35 см; 2 — патрубок для сбора металлического цезия (по окончании процесса отпаивается); 3 — железная пробирка с исходными компонентами (смесь хлорида цезия и металлического кальция); 4 — электрическая печь
| <<< Назад ЦЕЗИЙ |
Вперед >>> Свойства цезия |
- Производство спирта
- Глава 12 Распространенность микроорганизмов
- Численность и воспроизводство населения
- Производство на душу населения Беларусь и Российская Федерация (2009)
- Производство Беларуси и Российской Федерации (2009)
- Глава 6. Охрана и воспроизводство рыбных запасов Московской области
- 2.3.2. Производство
- Производство народа
- 1.20. ПРОИЗВОДСТВО СОДЫ ПО СОЛЬВЕ
- 239. Производство чугуна и стали.
- Свойства цезия
