Книга: Удивительный мир органической химии
13.1. «Частокол» на воде
| <<< Назад Глава 13 ПАВ — что это такое? |
Вперед >>> 13.2. Какими бывают ПАВ? |
13.1. «Частокол» на воде
Стиркой и мытьем занимались еще в глубокой древности. Более чем за две тысячи лет до нашей эры в городах Римской империи существовали превосходно оборудованные бани с бассейнами для плавания. В этих банях для мытья тела использовали отруби, соки растений и некоторые сорта моющих глин.
Впервые о получении мыла из жира и золы упоминается в трудах римского врача Галена (ок. 130-200 н. э.). Промышленное производство мыла в отдельных европейских странах возникло, по-видимому, в XIX в. В это время мыло уже варили в Германии и во Франции. Позже мыловарение стало развиваться в Англии. В 1400 г. исключительной славой пользовалось «венецкое» мыло (из Венеции).
В XIII в. мыловарение на Руси уже существовало как вполне развитый промысел (например, в Поволжье). Более того, мыло стало даже предметом вывоза в другие страны.
Мы знаем, что мыла — это соли высших карбоновых кислот. Обычное мыло, которым мы умываемся, представляет собой смесь натриевых солей пальмитиновой и стеариновой кислот:
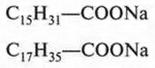
Эти мыла — твердые вещества. Но бывают и жидкие мыла — калиевые («зеленое» мыло).
Известно, что мыла обладают поверхностной активностью — они снижают поверхностное натяжение воды. Мы уже говорили об этом раньше. Теперь подробнее расскажем об этом интересном явлении, с которым знакомы, наверное, многие. Например, если стакан осторожно наполнить водой полностью, то ее уровень может подняться выше края стакана, образуя выпуклость, заметную глазом. Этот избыток воды удерживается особой водяной пленкой, не позволяющей жидкости стечь вниз. Кстати, эта пленка позволяет некоторым насекомым свободно передвигаться по спокойной поверхности озера. Как же возникает такая пленка?
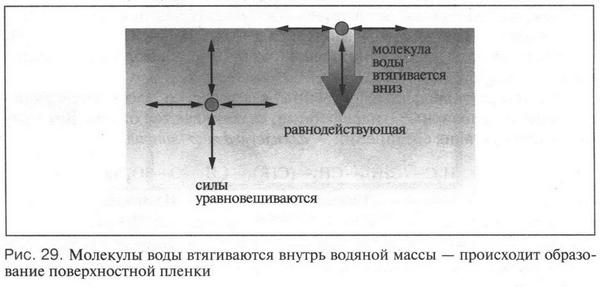
Представим молекулу воды, окруженную другими молекулами. Находясь в тесном контакте с ними, молекула испытывает на себе их воздействие. Поскольку такое воздействие одинаково со всех сторон, то все силы, действующие на «нашу» молекулу, взаимно уравновешиваются. Но вот молекула оказалась на поверхности воды (на границе раздела вода — воздух). Теперь она испытывает воздействие только с трех сторон: с боков и снизу, а сверху — нет. При этом силы, которые действуют на молекулу из глубины, будут преобладать. Эти силы тянут молекулу в одном направлении — вниз (рис. 29). Вот почему молекула притягивается к воде — происходит образование поверхностной пленки. Что же касается сил «влево-вправо», то они взаимно компенсируются. Эта пленка обладает относительной прочностью. Помните стакан, наполненный выше краев водой? С помощью двух ниток осторожно положите швейную иглу на поверхность воды. Если с первой попытки это не удастся, то попробуйте еще раз. И вы убедитесь, что иголка будет плавать на поверхности благодаря водяной пленке.
Итак, мыло снижает поверхностное натяжение воды. Однако у обычных мыл имеются существенные недостатки. Они плохо моют, как вы знаете, в жесткой воде. Соли кальция и магния, которые присутствуют в этой воде, за счет обменной реакции образуют нерастворимые в воде кальциевые и магниевые мыла. Кроме того, мыла в воде гидролизуются (омыляются) с образованием щелочи:

Эта щелочь оказывает вредное действие на некоторые ткани (шерсть, шелк и др.).
Есть еще один существенный недостаток. Он связан с расходом огромного количества ценных пищевых жиров (животных и растительных). Правда, сейчас для получения мыла используют высшие карбоновые кислоты, которые получают окислением алканов. Кислоты нейтрализуют щелочью, и полученную соль используют для производства туалетного и хозяйственного мыла (цифры «60» и «72» на кусках мыла означают процент содержания в нем натриевых солей высших кислот).
В последние десятилетия использование мыла для стирки тканей, очистки стеклянных, керамических, деревянных, металлических и полимерных изделий резко сократилось в связи с появлением синтетических моющих средств (СМС), которые называют также детергентами. Эти вещества известны еще с 1907 г. (но с биологическими добавками они появились в 1967 г.).
Основу всех синтетических моющих средств составляют поверхностно-активные вещества (ПАВ), которые, как и мыло, снижают поверхностное натяжение воды. ПАВ — это органические соединения, в молекулах которых содержатся одновременно две противоположные по свойствам группы. Одна из них — полярная (—СООН, —COONa, —SO3H, —SO3Na и др.), другая — неполярная (различные углеводородные радикалы С12—С18).
Полярные (гидрофильные) группы, как известно, легко растворяются в воде, а неполярные (гидрофобные) отталкиваются от нее. Вот пример одного из таких соединений — алкилсульфата натрия.

Поэтому молекулы ПАВ на пограничной поверхности (на границе вода — воздух, вода — масло, вода — уголь и т. д.) располагаются в определенном порядке: гидрофильные группы направлены в воду, а гидрофобные выталкиваются из нее (см. рис. 24). В результате вся поверхность воды покрыта своеобразным «частоколом» из молекул ПАВ. Такой «частокол» очень тонкий (всего 0,1 нм). Но благодаря ему водная поверхность обладает более низкой энергией, чем поверхность чистой воды. Помните о плавающей швейной игле на поверхности воды? Стальная игла удерживается на водяной пленке и не тонет благодаря поверхностному натяжению. Но стоит осторожно добавить к воде какое-нибудь поверхностно-активное вещество (например, мыльный раствор), как игла сразу же упадет на дно стакана. Следовательно, понижение поверхностного натяжения способствует быстрому и полному смачиванию различных предметов. Поскольку поверхностное натяжение воды сильно затрудняет процесс мытья и стирки, то главная задача всех ПАВ — понизить это натяжение.
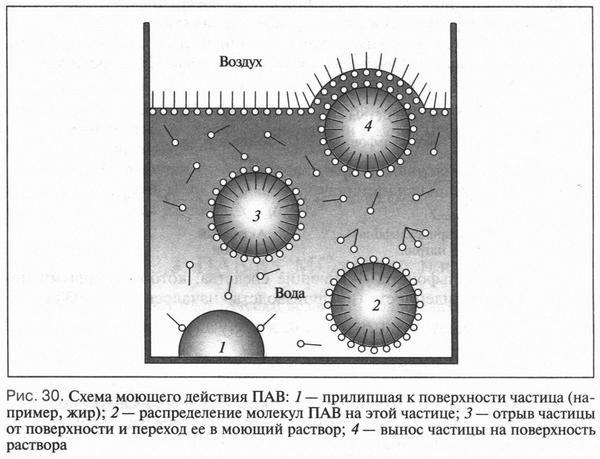
Процесс удаления загрязнений с поверхности предмета (например, ткани) происходит, как это показано на рисунке 30. Молекулы ПАВ адсорбируются на поверхности ткани и на загрязняющих ее частицах (жировые пятна, сажа и др.) и проникают в зазоры между ними. Полностью покрытая такими молекулами частица отделяется от поверхности ткани и в виде эмульсии или суспензии уходит в раствор. ПАВ — хорошие пенообразователи и стабилизаторы эмульсии. Пене также принадлежит важная роль: загрязняющие частицы, прилипшие к ее пузырькам, удаляются вместе с ней из моющего раствора.
| <<< Назад Глава 13 ПАВ — что это такое? |
Вперед >>> 13.2. Какими бывают ПАВ? |
- ГЛАВА 16 Для чего служат брови и ресницы?
- Что видно с воздуха?
- 9.2. Области применения инженерно-биологических технологий и их основные типы
- Десятый отряд Хоботные
- Миф заключительный (вместо послесловия) Если человек произошел от обезьяны, то все дозволено!
- Краски и рисунки одежд
- Вайтань-Бунд и Наньцзинлу
- Не все кукушки бывают «кукушками»
- Глава 13 ПАВ — что это такое?
- 13.2. Какими бывают ПАВ?
- Красная зима, черная осень
- 28. Камералка
