Книга: Онтогенез. От клетки до человека
Глава 9 Прокладка труб
| <<< Назад Глава 8 Внутренние путешествия |
Вперед >>> Глава 10 Организация органов |
Глава 9
Прокладка труб
Человек – ходячий шедевр водопроводных работ.
Клетки – объекты очень малого размера: как правило, около сотой доли миллиметра. Белки, которые участвуют во внутриклеточных реакциях, еще меньше: их радиус – примерно десятимиллионная доля миллиметра, а молекулы воды, в которой растворены белки, намного меньше их самих. На молекулярном уровне содержимое клетки находится в постоянном движении. Это не имеет никакого отношения к тому факту, что клетки живые. Движение, о котором я говорю, с тем же успехом продолжится и в мертвой клетке, впрочем, как и в теплом супе. Оно вытекает из основных законов физики. При любой температуре выше абсолютного нуля молекулы совершают случайные колебания и движения (температура – просто мера этой энергии движения, усредненная по популяции молекул). Движущиеся молекулы иногда сталкиваются, а затем отскакивают друг от друга. Если крупные молекулы, например белки, растворены в воде, молекулы воды сталкиваются и с ними, сообщая им часть своего импульса, поэтому молекулы белков тоже находятся в постоянном хаотичном движении.
Этот эффект можно наблюдать и на более крупных и тяжелых объектах, чем белки, например на пылинках. Римский поэт и ученый Лукреций еще в 60 г. до н. э. предположил, что хаотический «танец» частиц дыма в воздухе может быть связан с быстрым движением «атомов» (именно так он их назвал) – невидимые простым глазом, они случайно сталкиваются с частицами.[137] В жидкостях этот эффект впервые наблюдал Ян Ингенхауз в 1785 г., а 42 года спустя его вновь описал шотландский ботаник Роберт Броун. В его честь движение растворенных или взвешенных в жидкости частиц называют «броуновским» (что несколько несправедливо по отношению к Ингенхаузу), а открытие того, что это движение возникает из-за столкновения с невидимыми атомами или молекулами, обычно приписывают Эйнштейну (что несколько несправедливо по отношению к Лукрецию).
Броуновское движение имеет большое значение для развивающегося эмбриона, потому что хаотичное движение молекул является автоматическим механизмом транспортировки растворенных веществ (пищи, кислорода и «стройматериалов») туда, где они нужны. Ферменту, которому требуется конкретное вещество, остается только ждать, когда хаотическое движение приведет это вещество в контакт с ним. Этот механизм хорошо работает на небольших расстояниях, но, учитывая, что хаотично движущиеся молекулы часто меняют направление движения, при увеличении расстояния эффективность транспортировки падает. Для растущего эмбриона это очень существенно: поскольку пища и кислород поступают через стенки матки, клетки, находящиеся глубоко внутри развивающегося организма, рискуют остаться без необходимых веществ и погибнуть голодной смертью. Максимальное расстояние, на котором обычная клетка млекопитающего в плотной ткани может получать питательные вещества за счет случайной тепловой диффузии, в несколько десятков раз превышает диаметр клетки (некоторые специализированные клетки, в частности клетки скелета и связанных с ним тканей, могут находиться дальше от источника питательных веществ). Эмбриону бо?льшего размера – а центр туловища взрослого человека лежит на расстоянии примерно в тридцать тысяч клеточных диаметров от кожи – необходимо разработать систему эффективного транспорта питательных вещества в глубоко лежащие ткани. Такая система должна подводить питательные вещества достаточно близко к каждой клетке, чтобы они могли преодолеть оставшееся расстояние за счет хаотической тепловой диффузии. В организме человека и других позвоночных проблема решается за счет циркуляции жидкости-носителя – крови – по тончайшим трубочкам, расходящимся по всем уголкам тела.
Для работы кровеносной системы нужны четыре основных компонента: жидкая составляющая крови, переносящая основную часть питательных веществ и токсинов; свободно плавающие в ней клетки крови, отвечающие за перенос кислорода (транспортировать кислород в растворенном виде проблематично); замкнутая система труб для подведения крови к тканям; и насос для поддержания циркуляции крови между тканями, в которых кровь обогащается полезными веществами, и тканями, которые расходуют их. Все ткани развивающегося эмбриона потребляют питательные вещества и выделяют продукты обмена. В плаценте кровь эмбриона подходит очень близко к крови матери, которая обновляется и очищается с помощью легких, кишечника, печени и почек. Так как молекулы могут довольно свободно циркулировать между кровеносными системами матери и эмбриона, их концентрация, как правило, стремится к равновесию, поэтому в плаценте истощенная кровь эмбриона обогащается кислородом и питательными веществами и избавляется от отходов. Поэтому кровь эмбриона должна циркулировать по кругу от плаценты к телу эмбриона и обратно. Для этого должна появиться система кровеносных сосудов и «насос».
Сосудистая система эмбриона человека возникает в виде двух основных частей. Одна из них находится за пределами эмбриона, в желточном мешке, а другая – внутри эмбриона. Обе части важны и вместе формируют единую систему, но, чтобы немного упростить тему, в этой главе мы сосредоточимся главным образом на той части кровеносной системы, которая располагается в организме эмбриона.
Клетки, которые дадут начало первым кровеносным сосудам эмбриона, можно впервые различить в мезодерме[138] на самом краю тела эмбриона примерно в то время, когда формируется нервная трубка[139] (глава 5; рис. 38). Их формирование и размножение запускается сигнальным белком, VEGF, который секретируется другими областями мезодермы, а также эндодермой.[140],[141] В ответ на сигналы эти клетки – гемангиобласты[142] – начинают размножаться и производить белки, характерные для кровеносных сосудов. Это мигрирующие клетки; они чувствительны к сигнальным белкам, которые синтезируются сомитами, и мигрируют в направлении источника этих белков. Итак, гемангиобласты перемещаются от края эмбриона к средней линии его тела[143],[144] (рис. 38, б).
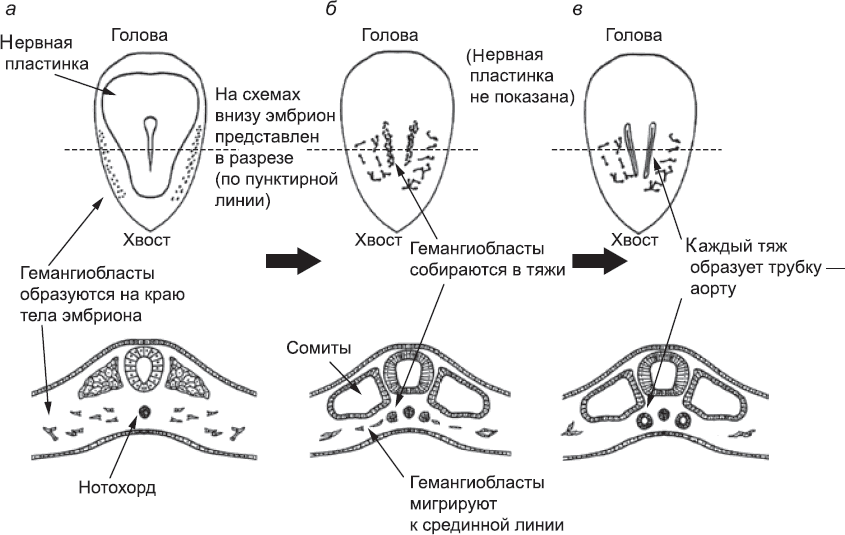
Рис. 38. Закладка аорт – первых артерий эмбриона: (а) эмбрион (вид сверху и в разрезе) на ранних стадиях формирования сомитов; гемангиобласты образуются в наружных частях мезодермы. На схеме (б) эти клетки начали мигрировать и формировать тяжи по бокам нотохорда, а на схеме (в) тяжи уже приобрели просвет. Они дадут начало разным частям аорты, которые пока что изолированы друг от друга
Если бы сигналов больше не поступало, развитие гемангиобластов остановилось бы. Продолжение развития, как и многие другие события в районе средней линии раннего эмбриона, зависит от сигналов белка Sonic Hedgehog, который вырабатывается нотохордом.[145] В присутствии этого белка гемангиобласты «прилипают» друг к другу, образуя сеть связанных клеток. Клетки, которые сошлись под сомитами, формируют такую плотную сеть, что с обеих сторон эмбриона она принимает вид плотных тяжей, проходящих под сомитами (см. рис. 38, б). Эти тяжи затем становятся полыми трубками (рис. 38, в). Механизм этого преобразования напоминает то, что происходило в первые дни жизни эмбриона, когда трофэктодерма отделялась от внутренней клеточной массы (глава 3). Клетки на наружной стороне тяжа находятся в контакте не только с другими гемангиобластами, но и с обычной мезодермой; благодаря этой асимметрии они выживают и образуют эпителиальный пласт цилиндрической формы. Клетки внутренней части стержня, наоборот, окружены только другими гемангиобластами. Отсутствие асимметрии заставляет их активировать программу «клеточного самоубийства» – они погибают, и образуется пустое пространство (роль клеточного самоубийства в развитии будет подробнее рассмотрена в главе 14). В результате сплошной тяж превращается в полую трубку со стенками, состоящими из поляризованных эпителиальных клеток (рис. 39). Так формируются две аорты – слева и справа от центральной линии.
Важность поступления белка Sonic Hedgehog из эндодермы была показана в экспериментах двух типов, выполненных одной и той же исследовательской группой.[146] В первом эксперименте удаляли эндодерму, ликвидируя таким образом основной источник этой молекулы, и аорта не формировалась. Во втором эксперименте чистый белок Sonic Hedgehog добавили искусственным путем в эмбрион, лишенный эндодермы, и образование кровеносных сосудов налаживалось. Роль белка Sonic Hedgehog подтверждается тем фактом, что даже в простых чашках Петри можно заставить гемангиобласты создавать цепь сосудистых трубок, просто добавив этот белок.
Учитывая, что под влиянием сигнальных белков гемангиобласты слипаются друг с другом, есть риск того, что они образуют только один тяж, идущий вдоль средней линии тела. Чтобы этого не произошло, в действие вступают сигнальные белки малого радиуса действия, такие как Noggin. Их источником является нотохорд. Поскольку пространство под нотохордом (между ним и эндодермой) ограничено, эти белки эффективно блокируют формирование кровеносных сосудов вдоль средней линии. В результате образуются две отдельные аорты – по одной на каждой стороне тела[147] (рис. 40). Такое расположение сосудов нормально для раннего эмбриона, но в дальнейшем меняется по мере созревания плода.[148]
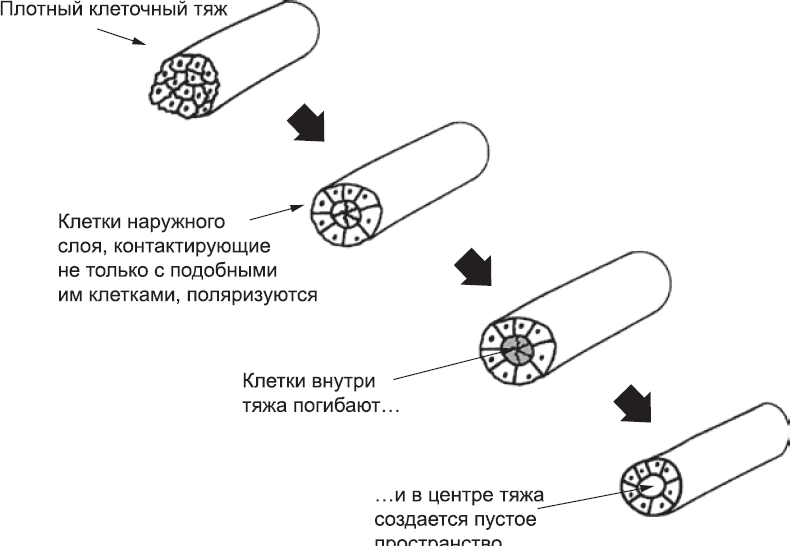
Рис. 39. Предполагаемая схема того, как плотный тяж гемангиобластов превращается в полый сосуд. (Происходит ли это именно так у человека, непонятно, но для других животных эта схема справедлива.) Внешний клеточный слой (его клетки асимметричны, так как контактируют не только с другими гемангиобластами) поляризуется, образуя герметичную трубку. Внутренние клетки, со всех сторон окруженные себе подобными клетками и лишенные контакта с тканью снаружи, погибают, и образуется полость, по которой в один прекрасный день потечет кровь
Кровеносные сосуды тела бывают двух типов – артерии и вены. Артерии – это сосуды с относительно маленьким просветом и толстыми стенками, по которым кровь идет под высоким давлением из сердца к мелким кровеносным сосудам в тканях. Вены – это сосуды большего диаметра и с более тонкими стенками, по которым кровь возвращается к сердцу под более низким давлением. Выяснилось, что судьба гемангиобластов предопределена еще до начала их миграции к средней линии тела. В клетках, которые дадут начало артериям, экспрессируется немного другой набор белков, чем в клетках, которые дадут начало венам (особенно это относится к белкам, которые принимают участие в межклеточных взаимодействиях). По крайней мере, у рыб, которые хорошо изучены в этом отношении, дифференцировка гемангиобластов на венозные и артериальные контролируется, опять же, белками семейства Hedgehog. Если клетка получает эти сигнальные белки в высоких концентрациях, она рано развивается, рано начинает миграцию и берет на себя функции артериального гемангиобласта. Если же клетка получает эти белки в низких концентрациях, то она развивается и мигрирует позже, становясь венозным гемангиобластом.[149] Разные наборы белков, выделяемые клетками с разной судьбой, позволяют им распознавать себе подобных и держаться вместе с ними. Клетки, запрограммированные на формирование вен, мигрируют по несколько иным маршрутам, но образуют кровеносные сосуды по той же основной схеме. Две крупные вены образуются параллельно аортам по всей длине эмбриона, но дальше от срединной линии (что вполне естественно, потому что концентрация белков семейства Hedgehog там ниже, и среда более благоприятна для образования вен).
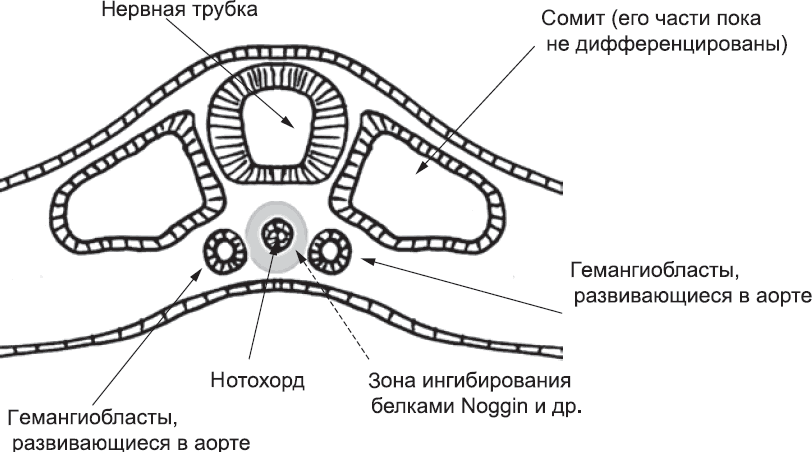
Рис. 40. Нотохорд выделяет белки Noggin, которые не дают тяжам гемангиобластов слиться по срединной линии. Поэтому формируются два отдельных тяжа, по одному с каждой стороны тела. В дальнейшем тяжи превращаются в полые трубки – правую и левую аорты
В ткани артериальная и венозная системы образуют тонкие ответвления, которые соединяются, формируя сеть мелких кровеносных сосудов. Стенки этих сосудов достаточно тонкие, так что кислород и питательные вещества могут свободно проникать через них.
Однако от кровеносных сосудов мало прока, если нет сердца, которое гонит по ним кровь. Поэтому этот орган одним из первых появляется у эмбриона и первым начинает функционировать. Сердце начинает формироваться примерно через девятнадцать дней после зачатия и примерно через два дня после начала образования крупных сосудов. Подобно тому как гемангиобласты собираются вместе и образуют трубки по обеим сторонам от средней линии, клетки, которые создадут сердце, сходятся и образуют новую пару трубок. Эти кардиогенные клетки также приходят из мезодермы с внешних краев эмбриона, но в данном случае с внешних краев головной части эмбриона, а не его туловища (рис. 41, а). Их образование ограничено этой областью за счет взаимодействия секретируемых белков из трех семейств.[150] Во-первых, сигналы, исходящие из эндодермы по краям эмбриона, стимулируют образование кардиогенных клеток. Во-вторых, белки семейства WNT, секретируемые нервной трубкой (см. главу 7), действуют противоположным образом, ингибируя образование кардиогенных клеток. В-третьих, белки, синтезируемые эндодермой головной части зародыша, позволяют клеткам сопротивляться сигналам белков WNT (по крайней мере, кардиогенным клеткам). Таким образом, голова – единственное место, где действие белков WNT подавляется в достаточной степени, чтобы могли образоваться кардиогенные клетки.[151] То, что область положительных сигналов ограничена самым краем эмбриона, означает, что кардиогенные клетки могут формироваться только в области, имеющей форму полумесяца, залегающей у внешнего края головы эмбриона.
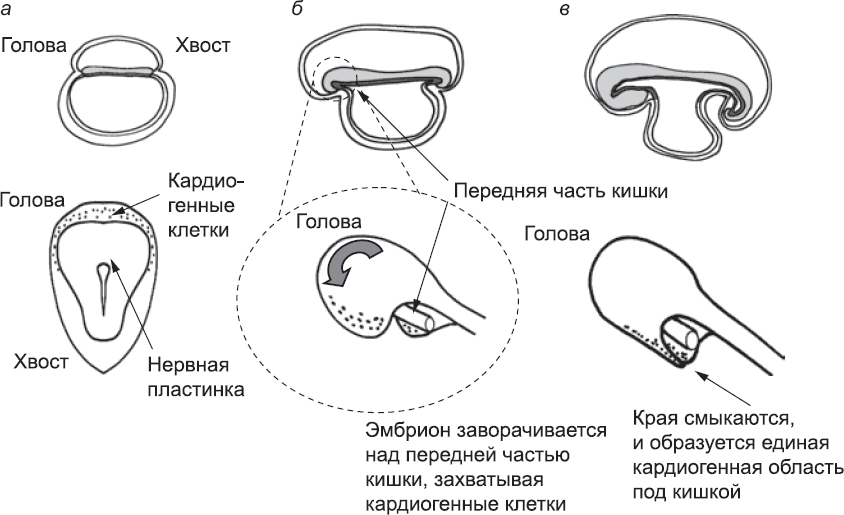
Рис. 41. Три стадии формирования сердца. Схемы в верхнем ряду, на которых эмбрион показан сбоку, уже встречались нам в главе 5; на схемах в нижнем ряду показан вид сверху (а) или вид сверху и сбоку (б и в). На первой стадии (а), когда эмбрион еще плоский и его удлинение незначительно, кардиогенные клетки находятся в мезодерме за нервной пластинкой в области головы. Позднее (б), по мере удлинения эмбриона, которое способствует формированию из концов эндодермы кишечной трубки, эмбрион изгибается. Когда его края смыкаются под кишечником (в), все кардиогенные клетки оказываются в одной области ниже кишечника (с вентральной стороны); там и будет формироваться сердце
Как и гемангиобласты, которые формируют артерии и вены, кардиогенные клетки приобретают способность к миграции, распознают себе подобные клетки, объединяются с ними и образуют трубки. Концы этих трубок, обращенные к туловищу эмбриона, соединяются с аортами, образуя непрерывный слой клеток. На этом этапе тело эмбриона довольно быстро удлиняется, и геометрия его концов меняется. В конце главы 5 я упоминал, что концы тела эмбриона подворачиваются вниз и за счет этого из эндодермы образуется кишечная трубка. Другим результатом этого подворачивания является то, что полумесяц ткани на краю головной части, где располагаются кардиогенные клетки, продвигается вниз по передней поверхности эмбриона приблизительно до уровня будущей груди; таким образом, он оказывается ниже кишечника (рис. 41, б, в). Здесь кардиогенные клетки, которые находятся в процессе создания двух отдельных параллельных трубок, сходятся вместе. При образовании параллельных дорсальных аорт им не давали сливаться ингибирующие сигналы нотохорда. На параллельные трубки сердца с вентральной стороны нотохорд не действует, и ингибирующих сигналов нет. Поэтому они могут беспрепятственно встретиться и соединиться, что они и делают. Так образуется одна трубка большого диаметра – первичное сердце.
Заворачивание тела эмбриона над концом кишки захватывает и концы аорт, к которым уже присоединились трубки сердца. Конец левой аорты направлен вниз слева от кишечника, а конец правой – соответственно справа, так что в результате кишечник оказывается окружен артериальным кольцом (рис. 42).[152] Позже нотохорд перестает продуцировать сигнальные белки, препятствующие слиянию проходящих над кишечником дорсальных аорт, и они объединяются в один сосуд.
На ранних стадиях сердечная трубка состоит из одного типа клеток, образующих выстилку кровеносных сосудов. В ней нет ни мышц, ни каких-либо специализированных тканей, обеспечивающих управление и контроль, а без таких тканей работа органа, который должен биться и/или играть роль насоса, невозможна. Однако уже через несколько дней сердечная трубка «притягивает» клетки, которые образуют сердечную мышцу и другие необходимые ткани.
Клетки сердечной мышцы обладают интересным свойством: они могут сокращаться сами по себе, не будучи связанными с нервной системой. Объединяясь, они взаимодействуют при помощи электрических сигналов, что позволяет синхронизировать сокращения разных клеток. Исследователи, работающие со стволовыми клетками эмбриона, имеют возможность непосредственно наблюдать за этим процессом. Когда стволовые клетки эмбриона выращиваются в условиях, при которых они могут «начать сначала» и приступить к созданию тканей тела, некоторые из них становятся сердечными мышечными клетками. В течение нескольких дней на дне чашки Петри в море разнообразных клеток появляются многочисленные пульсирующие островки регулярно сокращающихся клеток сердечной мышцы.[153] Это удивительное зрелище, от которого невозможно оторваться даже тем счастливцам, которые имеют возможность наблюдать такое каждый день.
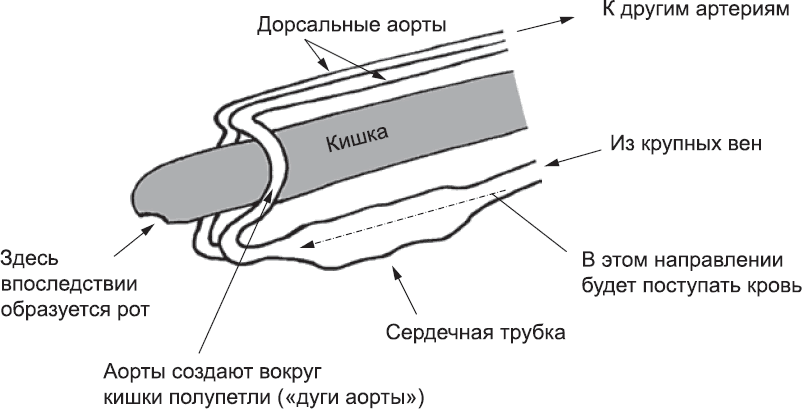
Рис. 42. За счет того же процесса изгибания эмбриона, благодаря которому кардиогенные клетки оказываются в его нижней части, оказываются внизу и места их соединения с головным концом аорты. Это приводит к образованию артериальной петли вокруг кишечника – дуги аорты. На схеме эмбрион «спрямлен», чтобы этот процесс был виден более четко
Хотя простая мышечная трубка очень далека от анатомически сложного развитого человеческого сердца, она вполне справляется с перегонкой небольших объемов крови по организму эмбриона на ранних стадиях развития. Наблюдать за работой сердца человеческого эмбриона по понятным причинам затруднительно, но сердечные трубки эмбрионов рыб, очень похожие на человеческие, являются благодатным объектом для исследования, потому что большинство рыб развивается в икринках вне тела матери и их эмбрионы прозрачны. Кроме того, некоторые виды рыб можно генетически модифицировать так, что их сердечные трубки будут флуоресцировать ярко-зеленым цветом, и следить за их развитием будет еще проще. Скоростная съемка этих эмбрионов показала, что механизм, с помощью которого работает сердечная трубка, удивительно сложен. Раньше предполагалось, что сердечные трубки перемещают кровь с помощью простой перистальтики: мышцы волнообразно сокращаются, трубка сужается и толкает жидкость вперед. Однако тщательное изучение[154] видео, снятых на большой скорости, показало, что работа сердечного «насоса» гораздо более эффективна и полагается на механизм отражения волн давления от конца трубки.
Отражение волн давления на концах труб или в местах, где меняется диаметр или эластичность стенок, – обычное явление. На нем основано, например, отражение звуковых волн в трубах органа. Часть волны, отраженная в нисходящем направлении, взаимодействует с восходящей частью; если длина волны такова, что эти части совпадают по фазе, возникает громкий звук (длина волны зависит от длины трубы, поэтому для получения нот разного тона используются трубы разной длины). Отраженные волны жидкости могут быть весьма мощными. Хороший пример мы находим в книге «Утро стрелочника» – автобиографии отставного железнодорожника Адриана Вохана.[155] В ней есть эпизод, когда инженер проверяет клапан в большом водоводе, открывая и быстро закрывая его несколько раз. Когда волна отраженного давления жидкости, вызванная первым открытием клапана, встретилась со следующей волной, возникло такое высокое давление, что трубы лопнули и на главной железнодорожной линии между Лондоном и Бристолем на несколько часов воцарился полный хаос.
В кровеносной системе эмбриона нет ни клапанов, ни открытых концов, но в местах, где большие вены присоединяются к сердцу, диаметр и эластичность стенок сосудов резко меняются. Этого достаточно для возникновения волн отраженного давления, и на ранних этапах развития эмбрион очень умело пользуется этой особенностью. Сердечный цикл начинается с сокращения небольшого участка заднего отдела сердца и локального сужения трубки (рис. 43). Сокращение распространяется от этой точки в обоих направлениях. Зачем сокращение должно распространяться к голове, интуитивно понятно (для продвижения крови вперед), а вот сокращения, направленные к хвосту, кажутся нелогичными. Однако возникающая в результате волна давления, распространяясь к хвосту, сильно отражается от места соединения с большими венами. При этом задняя часть сердца расслабляется, благодаря чему трубка открывается и начинает засасывать кровь. Таким образом, кровь движется вперед и за счет засасывания, и за счет волны отраженного давления, которая теперь движется к голове, заполняя пространство, открывающееся за волной сокращения, которая все это время распространялась в этом направлении.
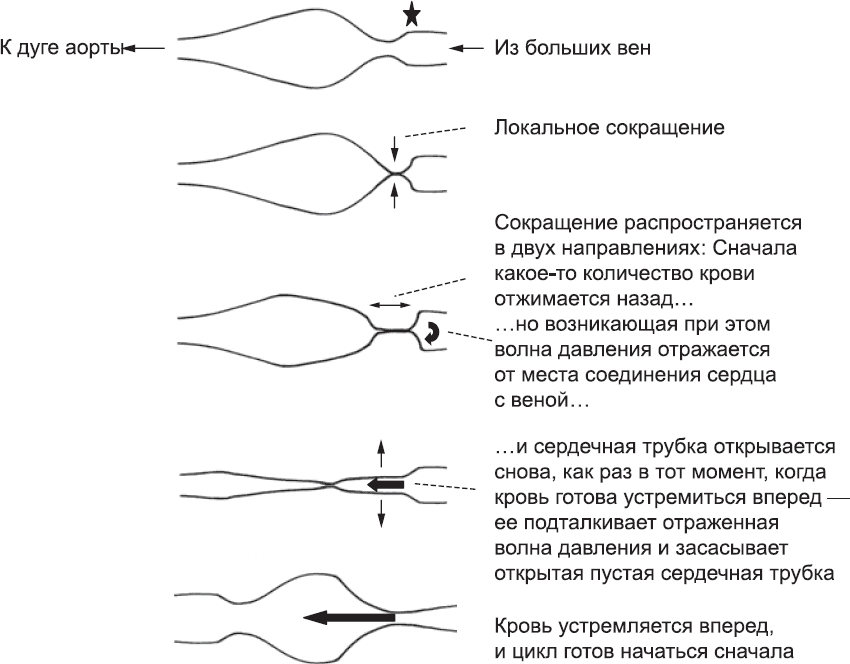
Рис. 43. На ранних этапах развития сердце устроено очень просто; у него нет ни клапанов, ни сложных систем контроля. Тем не менее оно эффективно гонит кровь благодаря отражению направленной к хвосту волны давления от места соединения сердца и вен (отмечено звездочкой на первой схеме)
Этого простейшего сердца достаточно для того, чтобы перегонять кровь по телу эмбриона, а также подводить ее к плаценте и желточному мешку. На более поздних этапах развития оно претерпевает множество сложнейших изменений, и простая трубка, перегонявшая кровь к голове, превращается в четырехкамерный орган, снабженный многочисленными клапанами. Они нужны для того, чтобы обслуживать два круга кровообращения, подводя кровь сначала к легким, а затем ко всем остальным частям организма.
После образования аорт, больших вен и сердца эмбрион переходит к созданию других кровеносных сосудов, используя для этого два новых метода. Первый метод – это ветвление уже существующих артерий и вен. Ответвления прорастают в ткани и, соединяясь друг с другом, формируют новые сосуды, по которым и будет течь кровь. От аорты, например, отходят сосуды, которые проходят между сомитами, ветвятся в нервной трубке и мышцах спины, а затем присоединяются к ответвлениям больших вен. От аорты также отходят сосуды к близлежащим органам, например к почкам (глава 10) и половым железам (глава 11). В некоторых отделах тела, например в шейном, артериальные сосуды, проходящие между сомитами, формируют боковые ответвления и таким образом соединяются друг с другом. Это означает, что ряд параллельных артерий в области шеи вблизи средней линии теперь соединяется, по сути дела, новой артерией, проходящей в направлении от головы к хвосту (рис. 44). После этого большинство поперечных артерий исчезает, и остается только новая, позвоночная артерия. Такая перепланировка системы кровообращения происходит многократно, еще раз указывая на то, что наше тело возникло – за счет целого ряда сложнейших модификаций – на основе плана строения эмбриона рыбы. Если бы человеческий эмбрион создавался с нуля, он был бы сразу похож на взрослую особь. Скорее всего, мутации, которые радикально меняли бы рыбообразный эмбрион и при этом не приводили к его немедленной гибели, были настолько маловероятны, что единственно возможным механизмом эволюции оставались мелкие постепенные изменения.
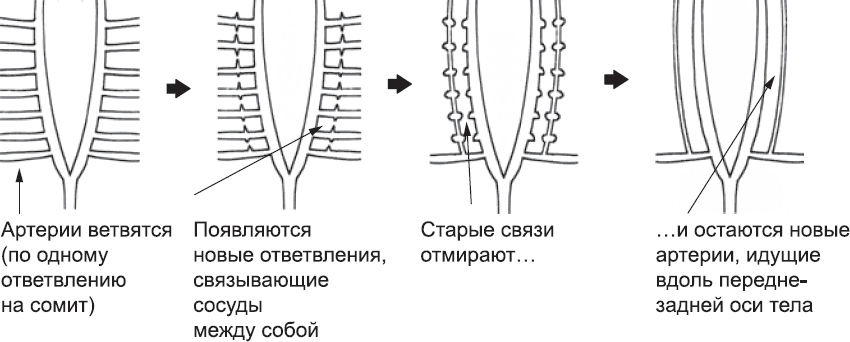
Рис. 44. Пример масштабной перепланировки системы кровеносных сосудов во время развития эмбриона. В области шеи, как и в туловище, от артерии отходят ответвления, проходящие между сомитами. От них, в свою очередь, отходят сосуды, проходящие в направлении голова – хвост. Когда они встречаются, образуется сеть артерий. Новые артерии развиваются, а поперечные сосуды дегенерируют. Таким образом, образуются две новые (позвоночные) артерии, идущие от головы к хвосту. Сохранившиеся поперечные артерии, показанные на схеме внизу, преобразуются в подключичные артерии взрослых особей. В нашем организме есть множество подобных примеров, как скажет вам любой отчаявшийся запомнить их студент медицинского института
Второй «новый» метод создания новых кровеносных сосудов прекрасно подходит для того, чтобы добавлять элементы к уже функционирующей системе, не нарушая при этом ее работу (как мы говорили в главе 1, это серьезная проблема). При интуссусцептивном (= вставочном) ангиогенезе новые ответвления возникают в системе, по которой уже циркулирует кровь.[156] В этом процессе задействованы участок стенки сосуда в верхней части и участок в нижней части; эти участки впячиваются в просвет сосуда навстречу друг другу, пока не встретятся. После этого клетки перенастраивают свои адгезионные контакты и присоединяются друг к другу, образуя своего рода опорный столбик. Затем этот столбик разрастается вдоль оси кровеносного сосуда, образуя стенку, разделяющую его на два параллельных сосуда (рис. 45). Эта стенка постепенно утолщается за счет присоединения новых клеток, и в конце концов два новых сосуда разделяются. С каждым из них теперь может произойти то же самое, и тогда получится в общей сложности четыре сосуда, и так далее. При помощи этого метода один кровеносный сосуд может преобразоваться в целую сеть без нарушения тока крови. Интуссусцептивный ангиогенез также может использоваться для смещения точки ветвления сосудов, чтобы они расходились под менее острым углом. Это очень важно для выравнивания потока крови, и вскоре мы вернемся к этой теме.
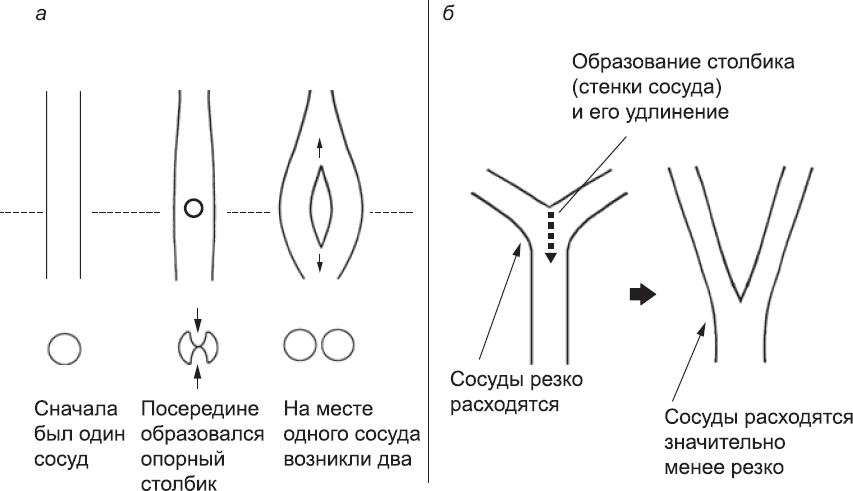
Рис. 45. Интуссусцептивное ветвление: (а) три стадии интуссусцептивного ангиогенеза. Верхний ряд – сосуд, вид сверху; нижний ряд – сосуд, вид в разрезе (по пунктирной линии). Впячивания верхней и нижней стенок сосуда приводят к образованию опорного столбика, который разрастается вдоль оси сосуда, пока тот не делится на два; (б) аналогичный процесс позволяет изменить угол расхождения сосудов (даже если один из них возник как ответвление основного сосуда) и выровнять кровоток
Однако, помимо кровеносных сосудов и сердца, у эмбриона должны образоваться также и собственно клетки крови. Здесь возникает проблема топологического характера: клетки крови должны находиться внутри кровеносных сосудов, а они образуют замкнутую систему, не имеющую прямой связи с остальными частями организма. Как же заполнить кровеносную систему клетками крови? Очень просто: первые кровяные тельца возникают из клеток, которые когда-то были клетками стенки аорты, и, следовательно, имеют доступ к просвету сосуда с момента его образования.[157],[158]
Формирование клеток крови из стенки аорты решает топологическую проблему, но ставит проблему иного характера: приступить к созданию клеток крови должны лишь некоторые клетки стенки аорты. Если это попытаются сделать все клетки, будет кровь, но не будет сосуда. Нужно, чтобы популяция идентичных клеток поделилась на две группы и у каждой был свой путь развития. И в этом случае тоже процессом дифференцировки управляют сигналы, поступающие из близлежащих тканей. Ткани органов, залегающих ниже аорты, например ткани кишечника, подают сигналы, подталкивающие клетки стенок сосуда к образованию клеток крови, а ткани органов, лежащих выше аорты, например ткани нервной трубки, этот процесс подавляют. Были найдены несколько сигнальных белков, вовлеченных в этот процесс, и оказалось, что среди них есть белки семейства Hedgehog, которые ранее контролировали образование аорты.[159]
Сигналы, поступающие от окружающих тканей, примерно определяют участок стенки аорты, клетки которого превратятся в клетки крови, но, чтобы ограничить число клеток, вовлеченных в этот процесс, используются другие механизмы. Клетки участка, предрасположенного к образованию клеток крови, начинают «переговариваться» между собой. Эти «разговоры», осуществляющиеся при помощи молекул на наружной поверхности клеток, похожи не на массовое оповещение, как при распространении сигнала с образованием градиента, а на негромкий обмен репликами между соседями. Нам известны далеко не все подробности, но некоторые из этих молекул уже выявлены; к ним относятся, например, белки Notch, Jagged и Mind-bomb.[160] Такие «разговоры по-соседски» приводят к тому, что не все клетки этой области становятся клетками крови.
Клетки, покидающие стенку аорты, – это еще не клетки крови, а скорее, стволовые клетки кровяной линии. Я уже говорил о стволовых клетках в главе 1, имея в виду клетки эмбриона на ранней стадии развития, которые могут дать начало любым клеткам организма. Сейчас речь идет о другом типе стволовых клеток. Клетки, покидающие стенку аорты, могут дать начало только разным типам клеток крови. Покинув аорту, они мигрируют и сначала поселяются в печени, которая только начинает развиваться (глава 10). Там они создают всю кровь для раннего плода. Гораздо позже, после образования костей, стволовые клетки кровяной линии снова отправляются в путь и окончательно обосновываются в костном мозге. Мы вернемся к их судьбе в главе 18.
Большие сосуды организма имеют стандартное расположение, не слишком отличающееся у разных людей. Напротив, расположение малых сосудов и тонких капилляров, доставляющих кровь вглубь тканей, сильно варьирует, поскольку они развиваются в соответствии с локальными потребностями конкретной ткани. У такой системы есть одно большое преимущество: она может адаптироваться к ошибкам и изменениям в расположении и площади ткани, которые должна обслуживать. Если клетки ткани «поймут», что находятся слишком далеко от ближайшего кровеносного сосуда, они подадут биохимический сигнал о помощи, и помощь – в виде новых сосудов и капилляров – не замедлит прийти.
Самое серьезное последствие расположения клетки вдали от циркулирующей крови – это нехватка кислорода (гипоксия). На этом основано действие по крайней мере одной из систем, контролирующих развитие кровеносных сосудов. Большинство клеток содержит белок, который называется Hypoxia Inducible Factor Alpha[161] (Hif1?). При нормальных концентрациях кислорода Hif1? быстро переходит в состояние, в котором он сразу разрушается клеточной системой переработки белка.[162],[163] При недостатке кислорода Hif1? остается в стабильном состоянии, не разрушается и не перерабатывается. Он успевает войти в ядро клетки и активировать несколько конкретных генов. Белки, кодируемые некоторыми из этих генов, приостанавливают клеточные процессы, для которых требуется кислород, за исключением процессов, необходимых для выживания. В частности, они прекращают размножение клеток, чтобы не добавлять новые клетки к области, и без того бедной кислородом, и не усугублять проблему. Однако еще один ген, активируемый Hif1?, делает нечто совершенно противоположное: он отвечает за производство VEGF[164] – белка, способствующего размножению и миграции клеток кровеносных сосудов. Этот белок и служит тем самым биохимическим «криком о помощи».
Обнаружив VEGF, клетки стенок кровеносных сосудов – как артерий, так и вен – начинают размножаться и двигаться в направлении наибольшей концентрации VEGF, то есть непосредственно к ткани, которой не хватает кислорода. Ветви мелких сосудов прорастают в ткани и там соединяются, создавая сеть мелких трубочек. В результате образуются тонкие сосуды – капилляры, – соединяющие артерии и вены и доставляющие свежую кровь тканям, которым раньше не хватало кислорода.
Когда кровь доставляет кислород к клеткам, которым его не хватает, Hif1? в них тут же разрушается. Когда концентрация Hif1? достигнет минимума, гены, экспрессию которых запускал этот белок, перестают экспрессироваться. Следовательно, клетки больше не подают сигналы о помощи и могут свободно размножаться. В результате размножения рано или поздно клеток будет так много, что клеткам, расположенным далеко от капилляра, снова будет не хватать кислорода, и процесс повторится сначала.
Подобные системы гарантируют то, что кровоснабжение будет поспевать за увеличением количества клеток и ростом ткани. Развивающимся сосудам не нужна точная «карта» роста тканей. Они просто должны уловить сигналы о помощи от тканей, испытывающих нехватку кислорода, и направиться к ним. Этот способ весьма экономичен в плане объема информации, которой должны обладать клетки (если бы клетки «ориентировались» по некоей гипотетической «карте», информации потребовалось бы гораздо больше), и при этом практически бесконечно адаптивен, так как позволяет обеспечить кислородом любую ткань, которая в нем нуждается.
Образование новых ветвей кровеносных сосудов зависит не только от сигналов тканей, в которых проходят сосуды, но и от самого кровотока. При движении жидкости вниз по трубке возникает слабая сила сопротивления, действующая и на движущуюся жидкость, и на стенки трубки. Течение жидкости замедляется, а вдоль стенок трубки действует сила, известная как напряжение сдвига. Ровное, спокойное течение жидкости (специалисты называют это «ламинарным потоком») вызывает лишь незначительное напряжение сдвига, и клетки стенки сосуда реагируют на такое воздействие, не изменяя своей стабильной формы. С другой стороны, турбулентный поток, который возник бы в том случае, если бы слишком много крови сразу хлынуло в узкий сосуд или изгиб сосуда был бы слишком резким, вызывает сильное напряжение сдвига в стенке сосуда. Клетки, оказавшиеся под таким воздействием, начинают создавать новые отростки, разветвлять уже существующие за счет интуссусцептивного ангиогенеза или делать и то и другое. Эффект не заставляет себя ждать: если пережать ветвь артерии, проходящей по поверхности желтка в курином яйце, напор крови в других местах увеличится и интуссусцептивная перестройка артериальной системы начнется в течение пятнадцати минут. Она будет продолжаться до тех пор, пока давление крови и скорость потока не придут в норму, а ткань не будет должным образом обеспечена кровеносными сосудами.[165] Постоянная и автоматическая перестройка кровеносной системы, направленная на избегание «горячих точек» турбулентности, приводит к появлению кровеносной системы с ровным кровотоком, силы, воздействующие на стенки сосудов, минимальны, сердце практически не тратит энергию на сопротивление турбулентности. И, как уже было сказано, это адаптивная и автоматическая система.
Адаптивность развития кровеносных сосудов очень важна для способности нашего организма к самоподдержанию и самокоррекции (см. главу 18), но и плата за это высока. Опухоли, как и обычные ткани, состоят из клеток, которые лучше всего чувствуют себя при высоком содержании кислорода. Когда клетки в середине растущей опухоли начинают чувствовать нехватку кислорода, они, как правило, тоже посылают сигнал о помощи, как это сделали бы нормальные клетки организма. Не понимая, что сигнал идет от потенциально опасной опухоли, а не от нормальных клеток, попавших в беду, близлежащие кровеносные сосуды услужливо направляют свои ветви в опухоль, обеспечивая ее кислородом и пищей и, таким образом, помогая ей расти. Один из подходов к разработке противоопухолевых лекарств основан на блокировании способности кровеносных сосудов отвечать на сигналы опухоли. Проблема осложняется тем, что клетки могут «звать на помощь» по-разному, но некоторый прогресс в этом направлении есть. Может быть, разработанные таким образом лекарства и не станут панацеей, но не исключено, что в сочетании с другими методами лечения они позволят продлить жизнь многим раковым больным.
| <<< Назад Глава 8 Внутренние путешествия |
Вперед >>> Глава 10 Организация органов |
- Глава 9 Прокладка труб
- Расчеты с микротрубочками?
- Глава 7 Туловище
- Насиживание яиц и вывод молодняка
- Физиология человека. Общая. Спортивная. Возрастная
- Цветущие камни
- Общая характеристика папоротниковидных
- Антибиотики с выключателем
- 1.8. Изомер означает «равный»
- Глава 3
- Глава 2 ОСВОЕНИЕ ТРАССЫ ЗЕМЛЯ-ЛУНА
- Китоглавы, или абу-маркубы.
