Книга: Происхождение жизни. От туманности до клетки
РНК и витамины
| <<< Назад Рибозимы осваивают обмен веществ |
Вперед >>> РНК и свет |
РНК и витамины
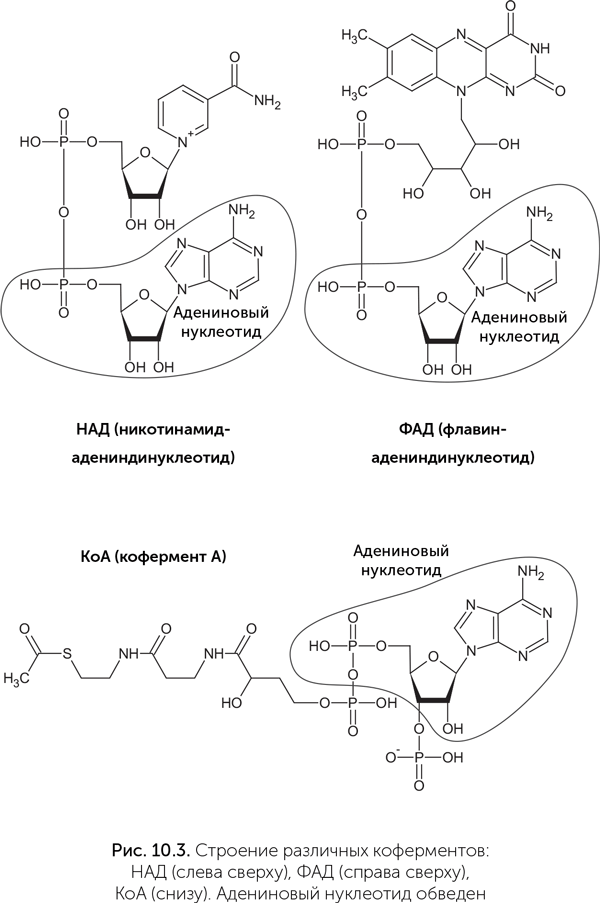
Коферменты – это разнородная группа веществ, которые выполняют особые функции в биохимии и не относятся ни к одному из основных классов веществ живых организмов (белки, нуклеиновые кислоты, сахара, липиды). Организм человека не способен производить большинство коферментов из простых предшественников, поэтому мы должны получать их «заготовки» с пищей, в виде витаминов. Коферменты НАД и ФАД переносят атомы водорода и участвуют в окислительно-восстановительных реакциях. Кофермент А (КoA) работает в реакциях, связанных с переносом ацетильных групп (-CO-CH3) и других кислотных остатков. Тиаминпирофосфат принимает участие в реакциях карбоксилирования и декарбоксилирования (присоединения и отщепления углекислого газа). Цианкобаламин служит для переноса метильных (CH3) групп.
Многие важнейшие коферменты имеют в своем составе адениновый нуклеотид: у кофермента А (КoA) к нему присоединена молекула витамина В5, у НАД – витамин РР, у ФАД – витамин B2 (рис. 10.3). Адениновый нуклеотид также входит в состав аденозил-кобаламина – активной формы витамина В12. Более того, у коферментов НАД и ФАД молекула в целом выглядит как два соединенных нуклеотида, где одно азотистое основание – обычный аденин, а в роли второго выступает никотинамид или флавин. Аденин в составе коферментов никак не участвует в их работе и служит только для узнавания коферментов белками. Скорее всего, это наследие РНК-мира, в котором витамины были пришиты к рибозимам для расширения их каталитических возможностей.
В опытах по искусственному отбору рибозимов были получены рибозимы, катализирующие часть этапов синтеза коферментов, а именно присоединение пантетеина, никотинамид-мононуклеотида и флавин-мононуклеотида к АТФ с образованием КoA, НАД и ФАД соответственно (Jadhav, Jarus, 2002). Также известны рибозимы, которые специфически пришивают НАД, ФАД или КoA к концу своей собственной молекулы или к другой РНК.
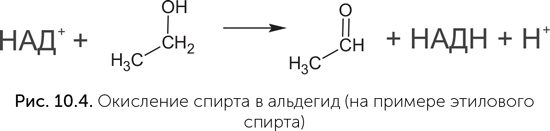
Коферменты НАД и ФАД переносят атомы водорода от одной молекулы к другой и необходимы в клетке для проведения окислительно-восстановительных реакций. Хотя в клетках они работают совместно с белками, в экспериментах были получены рибозимы, которые прочно и избирательно связывали НАД и с его помощью окисляли спирт в альдегид (рис. 10.4), – в клетках эту реакцию проводит НАД-содержащий белковый фермент алкоголь-дегидрогеназа (Tsukiji et al., 2004). Для никотинамида, ключевого компонента НАД, обнаружен простой путь синтеза, не требующий никаких ферментов и вполне реальный в условиях древней Земли. В нем простой сахар (диоксиацетон-фосфат) реагирует с аспарагиновой кислотой (одна из обычных аминокислот в составе белков) в водном растворе при температуре 60–100 °C (Cleaves, Miller, 2001). РНК, в которых на 5' конце находится НАД вместо обычного нуклеотида, обнаружены и в современных клетках: у кишечной палочки такой модификации подвергается до 15 % малых регуляторных РНК (sRNA) (Cahova et al., 2014), хотя функция НАД в составе этих РНК пока неизвестна.
Кофермент А тоже прекрасно ладит с рибозимами. Очень впечатляет работа Вазанта Ядхава и Михаэля Яруса (Jadhav и Yarus, 2002). Они создали набор рибозимов, проводящих в одном опыте три последовательные химические реакции: пришивание КoA к концу РНК, активацию органической кислоты при помощи АТФ (при этом получается ацил-аденилат) и перенос кислотного остатка ацил-аденилата на КoA в составе рибозима. Затем другая команда химиков получила рибозим, который использует ацетил-КоА и малонил-КоА для реакции конденсации Клайзена (Ryu et al., 2006). В этой реакции – а она является ключевым шагом в построении длинных молекул жирных кислот – соединяются два остатка органических кислот.
Еще один кофермент, который удалось заставить работать вместе с рибозимом, – это тиаминпирофосфат, активная форма витамина В1. Он используется в обмене веществ там, где надо присоединить или отщепить молекулу углекислого газа. Канадские химики Пол Чернак и Дипанкар Сен получили рибозим, который прочно связывает тиаминпирофосфат и с его помощью отщепляет СО2 от пировиноградной кислоты и ее аналогов (Cernak, Sen, 2013). Эта реакция очень важна в обмене веществ, через нее проходит «сгорание» всех потребляемых нами сахаров (подробнее в главе 11). Воспроизведение ее при помощи рибозима, а не белкового фермента – существенное доказательство возможности сложного обмена веществ до появления белков.
В той же лаборатории под руководством Дипанкара Сена рибозимы «подружились» и с гемом. Этот кофермент входит в состав гемоглобина крови, придавая ей красный цвет и способность переносить кислород. Кроме того, гем входит в состав цитохромов – большой группы белков, участвующих в самых разных окислительно-восстановительных реакциях.
РНК, отобранные на прочное связывание гема, заодно проводили две химические реакции: окисление разных веществ перекисью водорода при помощи гема и вставку цинка и меди в протопорфирин IX (подобная реакция происходит на последней стадии сборки гема) (Sen and Poon, 2011).
| <<< Назад Рибозимы осваивают обмен веществ |
Вперед >>> РНК и свет |
- Микробы и витамины
- 5.3. Внутренняя среда организма человека. Группы крови. Переливание крови. Иммунитет. Обмен веществ и превращение энерги...
- Глава 10 Витамины, аминокислоты и пептиды в РНК-мире
- Противоречивые витамины
- Запахи, издаваемые микроорганизмами
- Самая маленькая химическая фабрика
- Микробы и гниение
- Дружба с животными
- 5. Микробы в действии
- 12. Молекулы наследственности и микробы
