Книга: Происхождение жизни. От туманности до клетки
Термодинамика жизни
| <<< Назад Катализ |
Вперед >>> Глава 6 Место происхождения жизни, «первичный бульон», пицца и майонез |
Термодинамика жизни
Теория РНК-мира никак не рассматривает потоки и превращения энергии в живых системах. Поэтому биофизики, изучающие эти процессы, были в ней особенно разочарованы и стали создавать свои теории для объяснения энергетической стороны возникновения жизни (дальнейшее изложение во многом основано на книге К. Еськова «История Земли и жизни на ней», это лучшее известное автору изложение термодинамических основ жизни на русском языке).
Нам придется начать издалека. От людей, поверхностно знакомых с физикой, можно услышать утверждения вроде «жизнь нарушает второй закон термодинамики». Что это значит и почему это неверно?
Важнейшим достижением человечества стало создание машин для превращения тепла в механическую работу. Первой такой машиной был паровой двигатель. Он производит работу при передаче тепла от горячего котла с паром к холодильнику с водой. Поэтому наука о взаимных превращениях работы и энергии стала называться термодинамикой, а паровой двигатель – ее основной моделью.
Первый закон термодинамики, или закон сохранения энергии, гласит, что из любой системы нельзя получить больше работы, чем в ней содержится энергии. Воображаемое устройство, которое нарушает этот закон, получило название «вечный двигатель первого рода». Во всех реальных ситуациях, конечно, работы будет получаться меньше, чем допускает закон сохранения энергии, из-за всевозможных потерь, например, на трение. Но эти потери можно уменьшить. Например, если мы рассматриваем электрический двигатель, то можно использовать в нем сверхпроводящие обмотки, магнитно-левитационные подшипники и поместить двигатель в вакуум, чтобы исключить трение о воздух, и тогда реально получить коэффициент полезного действия (отношение произведенной работы к затраченной энергии) выше 99 %.
С тепловым двигателем, однако, такая оптимизация невозможна. Как доказал в 1824 году Сади Карно, эффективность теплового двигателя ограничена разностью температур горячего и холодного резервуаров (котла и холодильника в случае паровой машины):
I = (T2 – T1)/T2
(T1 – температура холодильника, Т2 – температура нагревателя, по шкале Кельвина, которая начинается от абсолютного нуля, – 273,13 °С).
Иными словами, если холодильник у нас имеет комнатную температуру (27 °C = 300 К), а нагреватель – 127 °C = 400 К, как у первых паровых машин, то мы можем превратить в работу не более 25 % тепловой энергии. Если у нас есть только одно, сколь угодно горячее тело и нет холодильника, мы вообще не можем превратить его тепловую энергию в работу. Это и есть одна из формулировок второго закона термодинамики: «Ни одно устройство не способно извлечь работу из системы, находящейся на одном потенциальном уровне». Она относится и к другим видам энергии: чтобы получить работу из потенциальной энергии тела, поднятого над Землей, ему должно быть куда падать. Из камня, лежащего посреди высокогорного плато, работы не получить. Чтобы пошел электрический ток, должна быть разность электрических потенциалов между разными телами. Иначе говоря, если в системе есть разные уровни энергии, то она будет перетекать с высокого уровня на низкий: тепло будет передаваться от горячего тела к холодному, камень покатится вниз по склону, а электрический ток пойдет от высокого потенциала к низкому.
Если паровой двигатель представляет собой замкнутую систему, т. е. не обменивается ни веществом, ни энергией с внешней средой, то горячий резервуар будет постепенно остывать, а холодный – нагреваться. В соответствии с формулой Карно получается, что чем дальше, тем меньшая доля тепловой энергии в такой системе может быть превращена в работу, а доля «недоступной» тепловой энергии будет расти. В 1865 году Р. Клаузиус, рассматривая эту недоступную тепловую энергию, ввел новую физическую величину – энтропию (S). Она отражает отношение тепловой энергии к температуре и имеет размерность джоуль на градус. В любом процессе, где происходит превращение энергии, энтропия растет либо в идеальном случае не убывает. Поэтому второй закон термодинамики называют еще «законом неубывания энтропии».
Пусть у нас в системе есть отдельные холодный и горячий резервуары, между которыми затем идет передача тепла, и их температура выравнивается. Можно сказать, что система вначале была упорядочена – поделена на горячую и холодную части, а потом перешла в беспорядочное, или хаотическое состояние. Мы видим, что, когда температура в системе выравнивается, уровень беспорядка (хаоса) в системе возрастает. Поскольку энтропия при этом тоже возрастает, возникает вопрос: нет ли связи между хаосом и энтропией? Действительно, связь между ними есть. Как доказал в 1872 году Л. Больцман, энтропия является мерой неупорядоченности системы:
S = klnP,
где k – универсальная постоянная Больцмана (3,29 ? 10–24 кал/град), а P – мера неупорядоченности системы.
Мера неупорядоченности P определяется как «количество микросостояний, которыми реализуется данное макросостояние». Что это значит? Попробуем объяснить на простейшем примере. Пусть у нас есть сосуд, в котором находятся четыре одинаковые молекулы газа. Каждая молекула может находиться с равной вероятностью в левой или в правой половине сосуда. Почему маловероятно, что все четыре молекулы окажутся в одной половине? Потому что движутся они независимо друг от друга, и по правилам комбинаторики в такой системе есть 16 вариантов расположения молекул. Это будут микросостояния. Макросостояния – это обезличенные описания ситуации в сосуде, когда мы не отличаем молекулы друг от друга. Макросостояний возможно пять: все молекулы слева; три слева, одна справа; две слева, две справа; одна слева, три справа; и все молекулы справа. Понятно, что макросостояние «все слева» реализуется только одним микросостоянием (каждая из четырех молекул должна быть слева). Макросостояние «два слева, два справа» можно получить шестью разными способами: слева могут быть молекулы 1 и 2; 1 и 3; 1 и 4; 2 и 3; 2 и 4; 3 и 4. Иначе говоря, для более упорядоченного состояния «все слева» Р = 1, а для неупорядоченного состояния «два слева, два справа» Р = 6. Если мы рассматриваем не четыре молекулы в сосуде, а, скажем, 1022 (10 000 миллиардов миллиардов) – примерно столько молекул воздуха находится в объеме обычного стакана, то состояние, когда молекулы поровну распределены между половинами стакана, реализуется примерно 1044 микросостояниями, а состояние, когда весь воздух собрался в одной половине стакана, – только одним. Отсюда понятно, почему заполнение воздухом половины стакана – крайне маловероятное событие, которое никто никогда не видел.
Соотношение Больцмана показывает, что в замкнутой системе все процессы в конечном итоге ведут к увеличению хаоса. Поскольку наша Вселенная по определению является замкнутой системой, то в отдаленном будущем ее неизбежно ждет «тепловая смерть» – полное исчезновение всякой структуры. Это, казалось бы, налагает запрет на возникновение более организованных (а значит, менее вероятных) структур из менее организованных, т. е. на прогрессивную эволюцию. Это очень беспокоило самого Больцмана: горячо восприняв дарвиновскую теорию эволюции, он потратил много сил, чтобы дать ей строгое физическое обоснование, но не смог. Однако живые организмы, создавая свои копии из слабо организованной неживой материи и усложняясь в ходе эволюции, очевидно, могут уменьшать свою энтропию. Как им это удается?
Вообще-то, этот трюк умеют делать не только живые организмы. Как работает обычный холодильник? Он понижает температуру внутри холодильной камеры и повышает температуру снаружи, т. е. понижает энтропию системы «холодильник – комната». Но эту систему нельзя считать замкнутой: она получает энергию извне, по электросети, в которую включен наш холодильник. Если мы рассматриваем систему «холодильник – комната-электростанция», то ее энтропия со временем только растет. Точно так же любой живой организм нуждается во внешних источниках энергии. Растения получают ее в виде солнечного света, а животные – в виде пищи. В конечном счете почти вся биосфера питается энергией Солнца. Она выделятся в ходе термоядерных реакций, связанных с огромным повышением энтропии, поэтому энтропия системы «Земля – Солнце» со временем растет, несмотря на возникновение и эволюцию земной жизни.
Здесь надо подчеркнуть, что термодинамика (связанная родством с химией) в одном отношении отличается от всех остальных разделов физики, так или иначе выросших из классической механики. В классической механике все процессы обратимы (т. е. могут точно так же происходить в обратную сторону), а картина мира – детерминистическая. Это значит, что если знать все параметры всех тел во Вселенной на какой-то момент времени, то можно точно предсказать ее будущее на любой срок, а также до мельчайших деталей восстановить ее прошлое. А если все процессы обратимы, то объективного времени вообще не существует, а есть только субъективное время, вводимое для нашего удобства, в виде нумерации порядка событий. Даже теория относительности и квантовая механика, перевернувшие физику в XX веке, в этом отношении сохраняют верность классической механике: в уравнении Шрёдингера, лежащем в основе квантовой механики, время остается однозначно обратимым.
В термодинамике все не так: ее модель Вселенной – не вечное вращение планет вокруг Солнца, а паровая машина, в топке которой безвозвратно сгорает топливо. Согласно второму закону термодинамики эта машина постепенно сбавляет обороты, приближаясь к тепловой смерти. Поэтому ни один момент времени не равен предыдущему, события невоспроизводимы, а время объективно существует и имеет однозначное направление. Термодинамика разграничивает обратимые процессы, в которых энтропия не изменяется, и необратимые, в результате которых происходит возрастание энтропии.
Как показал Илья Пригожин, необратимость появляется, только если в системе возможно случайное поведение. Случайность создает различие между прошлым и будущим системы и, следовательно, необратимость. Движение молекул в газе можно считать случайным, и первые необратимые процессы, которые изучала термодинамика, были связаны с поведением газов в тепловых двигателях. В термодинамике картина мира становится стохастической, и предсказать будущее уже невозможно, даже зная все про настоящий момент.
Классическая термодинамика XIX века имела два ограничения. Во-первых, она рассматривала в основном замкнутые системы. Во-вторых, она изучала достаточно медленные процессы, в которых в каждый момент времени система находится близко к равновесию. В XX веке ситуация изменилась. Появились новые виды тепловых двигателей, и при их разработке инженеры столкнулись с явлениями, которые в классической равновесной термодинамике принципиально невозможны. Например, при создании жидкостных ракетных двигателей инженеры столкнулись с серьезной проблемой высокочастотных пульсаций горения. Внезапно в работающем двигателе начинались быстрые – сотни раз в секунду – колебания давления, которые нарастали до тех пор, пока двигатель не взрывался. Чем мощнее двигатель и чем выше давление в нем, тем чаще возникали эти пульсации. Найти причину этих колебаний и устранить их долго не удавалось. Среди людей, которые знали об этой проблеме и не могли ее решить, был и великий математик, президент Академии наук СССР Мстислав Келдыш. И вот в декабре 1964 года в его кабинет пришел молодой биофизик Анатолий Жаботинский, поставил на стол стакан, смешал в нем несколько реактивов, и жидкость в стакане стала менять цвет с красного на синий и обратно. Это была первая признанная колебательная химическая реакция, ныне известная как «реакция Белоусова – Жаботинского» (BZ-reaction). В тонком слое раствора, например, на тарелке, в ней получаются сложные узоры из движущихся колец и спиралей (рис. 5.3). Келдыш сразу понял, что жидкость, меняющая цвет туда-обратно, имеет прямое отношение к неустойчивости горения в ракетном двигателе.
Реакция Белоусова – Жаботинского стала важной моделью новой, неравновесной термодинамики, за создание которой Илья Пригожин получил Нобелевскую премию в 1977 году. В неравновесной термодинамике доказывается, что в открытых системах, далеких от равновесия, возможна самоорганизация: местное уменьшение энтропии, которое может проявляться как появление новых структур. Это могут быть и коллективные, упорядоченные движения многих молекул. Пригожин назвал такие структуры диссипативными, чтобы подчеркнуть парадокс: процесс диссипации (безвозвратной потери энергии) играет в их возникновении ключевую конструктивную роль.

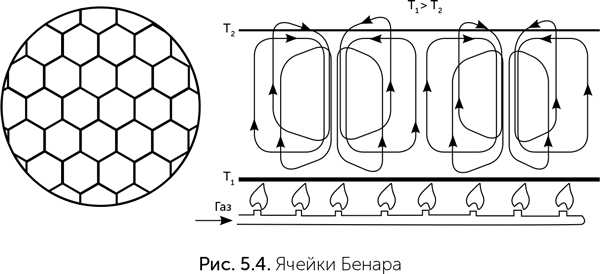
Одним из простейших случаев такой самоорганизации являются ячейки Бенара. Если равномерно нагревать снизу тонкий слой вязкой жидкости, на поверхности станут видны структуры правильной, в классическом варианте шестиугольной формы (рис. 5.4). Это и есть ячейки Бенара. Их появление связано с особенностями перераспределения тепла в слое жидкости высокой плотности. Поначалу тепло будет проходить через жидкость только за счет теплопроводности. Но если греть достаточно сильно, то в какой-то момент в жидкости начнется конвекция: молекулы начнут движение, организуясь в упорядоченные структуры. Это противоречит классической термодинамике, где тепловой поток – это источник потерь (диссипации), разупорядочивания, а не порядка. Если в классической термодинамике тепловой поток считается источником потерь, то в ячейках Бенара он становится источником порядка. Пригожин характеризует возникшую ситуацию как гигантскую флуктуацию, стабилизируемую путем обмена энергией с внешним миром. Похожим образом возникают циклоны – самоорганизующиеся структуры в атмосфере Земли.
Самоорганизация в реакции Белоусова – Жаботинского имеет другое происхождение. Для появления самоорганизации в химических системах необходимо, чтобы в них происходили автокаталитические реакции, т. е. такие, где продукт реакции ускоряет синтез самого себя. Реакция Белоусова – Жаботинского (окисление малоновой кислоты броматом калия в присутствии солей церия) оказалась очень сложна, в ней насчитывается свыше 30 промежуточных продуктов, и помимо автокаталитических шагов в ней есть также подавление отдельными веществами синтеза друг друга.
В ракетных двигателях такой сложной химии нет. Столь опасная самоорганизация в них имеет смешанное физико-химическое происхождение. Движение газов в ракетном двигателе происходит очень быстро, сравнимо со скоростью химических реакций в них, поэтому газы в камере сгорания далеки от равновесия. На съемках старта ракет на керосиновом топливе («Союз», «Зенит», «Фалькон») хорошо видно, что ярко-желтое пламя тянется на десятки метров за ракетой. Желтый свет испускают частички сажи, которые являются промежуточными продуктами горения керосина. Конечные продукты сгорания керосина – вода, угарный и углекислый газы – прозрачны. Вместо автокатализа в камере сгорания срабатывает ускорение химических реакций в газе. Поскольку горение керосина в ограниченном объеме приводит к повышению температуры и давления, возникает обратная связь: случайное ускорение горения в одном месте повышает давление, а давление ускоряет горение дальше. Повышенное давление не может оставаться в одном месте. Волна повышенного давления распространяется по газу и отражается от стенок камеры, и в какой-то ее точке отраженные волны сходятся. Там горение резко ускоряется и волна повышенного давления (фактически звуковая волна) расходится из этой точки, усилившись. Так в камере сгорания возникают устойчивые, нарастающие колебания давления. Благодаря реакции Белоусова – Жаботинского, которая гораздо безопаснее в изучении, чем ракетный двигатель, удалось разобраться в этих неустойчивостях, разработать форму камеры сгорания, в которой эффективно поглощаются звуковые волны, и создать надежные и мощные ракетные двигатели.
Любой живой организм является неравновесной системой. Равновесное состояние живого существа в обиходе называется трупом. Как и диссипативные структуры неживой природы, любая форма жизни существует благодаря какому-нибудь внешнему градиенту. Например, для человека и животных это химический окислительно-восстановительный градиент между кислородом атмосферы и органическими веществами пищи. Но этот градиент создан другими формами жизни, которые используются в пищу, т. е. в конечном итоге в подавляющем большинстве растениями.
Бывает, что живые существа используют и другие градиенты. Например, альбатрос для своего полета использует разницу в скорости ветра на разной высоте над водой. Он чередует планирование с медленной потерей высоты и короткие взлеты выше, в слой быстрого ветра, чтобы в нем набрать скорость для следующего планирования. В дальних перелетах 80 % энергии, нужной для полета, альбатрос получает из разных скоростей ветра, и только 20 % – из пищи. С точки зрения Земли альбатрос – это прежде всего мешалка для воздуха, и лишь во вторую очередь потребитель рыбы и кальмаров.
Биосфера в целом эксплуатирует энергию Солнца, т. е. градиент температуры между Солнцем и холодным космосом; этот градиент используется путем поглощения солнечного света в ходе фотосинтеза и излучения тепла в космос с поверхности планеты. На космических снимках хорошо видно, что богатые жизнью области планеты – леса и прибрежные воды – темнее, чем остальная суша или океан. Отдельные организмы могут так же использовать химический окислительно-восстановительный градиент между атмосферой и мантией Земли. Мантия содержит много железа в восстановленной (двухвалентной) форме, которое может окисляться при контакте с веществами поверхности Земли – кислородом, водой, углекислым газом. Этот градиент используют микробы, получающие энергию (читай – питающиеся) путем хемосинтеза.
Хотя жизнь имеет общие черты с неживыми диссипативными структурами, живые организмы обладают важным отличием от циклонов и ячеек Бенара. Диссипативные структуры возникают всякий раз, когда есть условия для их появления, и исчезают вместе с ними. Форма диссипативных структур определяется этими условиями. Любой современный живой организм, в отличие от них, обладает эволюционной историей, уходящей на четыре миллиарда лет в прошлое – это более четверти возраста Вселенной! Устройство живых организмов гораздо больше зависит от путей эволюции в прошлом, чем от современных условий их жизни. Такая историческая память обеспечивается молекулами ДНК, хранящими информацию об устройстве клеточных белков, эта информация копируется из поколения в поколение с высокой точностью. В следующих главах мы попытаемся понять, как из химических диссипативных структур возникла жизнь, основанная на наследственной информации.
| <<< Назад Катализ |
Вперед >>> Глава 6 Место происхождения жизни, «первичный бульон», пицца и майонез |
