Книга: Происхождение жизни. От туманности до клетки
Роль вирусов в происхождении эукариот
| <<< Назад Гипотезы о происхождении ядра |
Вперед >>> Вирусная теория происхождения ядра и полового размножения |
Роль вирусов в происхождении эукариот
Мы рассмотрели происхождение эукариот путем симбиоза между археей и бактерией в условиях перехода микробного сообщества к кислородной среде. Однако этот сценарий не объясняет многие особенности эукариотических клеток. Непонятно, как переход археи к фагоцитозу и обзаведение симбионтами могли способствовать появлению, например, полового размножения и мейоза. А если обратить внимание на более частные вопросы, то совершенно несуразной выглядит такая деталь эукариотической системы трансляции (считывания), как кэпы матричных РНК. Кэп – это остаток 7-метилгуанозина, пришитый к 5'-концу мРНК специальным 5' – 5'-трифосфатным мостиком (рис. 18.11). Он требуется для начала трансляции на эукариотической рибосоме – без него рибосома не может связаться с мРНК.
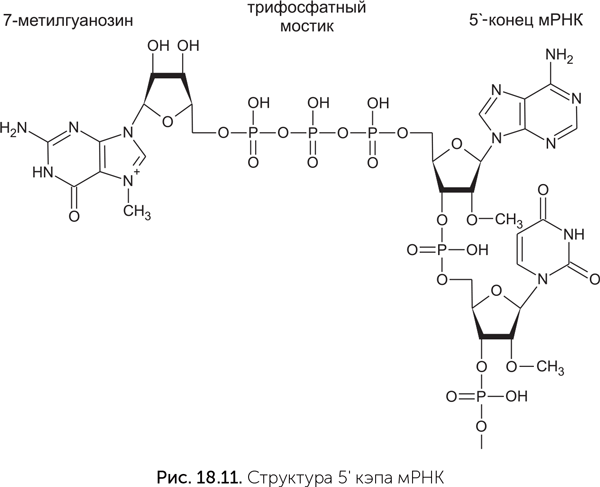
Для узнавания кэпа рибосомой есть специальный белок – фактор инициации eIF4E, не имеющий аналогов у прокариот. Важно, что из-за наличия кэпа и eIF4E эукариоты не могут иметь оперонов – групп генов, которые транскрибируются в одну длинную мРНК, кодирующую несколько белков последовательно, один за другим. Опероны позволяют бактериям и археям экономить на регуляции активности генов: достаточно одного регуляторного участка в начале оперона, чтобы одновременно управлять активностью всех его генов. (Обычно белки, которые кодируются генами одного оперона, функционально связаны, а значит, требуются в равных количествах.) Переход к кэпированным мРНК на заре эволюции эукариот потребовал бы массированной перестройки генома, распада всех оперонов и появления тысяч новых регуляторных участков для отдельных генов. Сложно представить себе причину, по которой это было бы выгодно для клетки, и еще сложнее найти причину, по которой система пришивания и узнавания кэпа вообще возникла.
Эти особенности эукариот находят объяснение, если допустить, что в их появлении участвовали помимо архейного и бактериального партнеров еще и вирусы. Вирусное происхождение отдельных компонентов эукариотической клетки не вызывает сомнения. Так, фермент теломераза, достраивающий защитные концевые структуры хромосомной ДНК (теломеры), происходит от обратной транскриптазы ретровирусов. Часть генетического аппарата митохондрий – ДНК-полимераза, РНК-полимераза и праймаза – унаследована от хвостатого бактериофага, похожего на современный фаг Т4 и встроенного в геном бактериального предка митохондрий. Однако есть и более радикальное мнение о роли вирусов в появлении эукариотической клетки – вирусная теория происхождения ядра.
Эту теорию в современном виде выдвинули вирусологи Филипп Джон Белл и Масахара Такемура (Bell, 2001; Takemura, 2001; Bell, 2009). Они утверждают, что ядро эукариотической клетки происходит от крупного ДНК-вируса, заразившего древнюю архею. Этот вирус мог перейти к умеренной эксплуатации хозяина: он не убивал его сразу (это явление называется лизисом), а сосуществовал, медленно размножая свою ДНК в его клетках (лизогения). Постепенно такой вирус мог взять клетку хозяина под полный контроль. Поначалу другие ученые практически не рассматривали эту теорию всерьез, но в последнее время она стала набирать популярность – так, к ее обсуждению подключился крупнейший французский вирусолог Патрик Фортерр.
Ключевую стадию пришивания кэпа проводит фермент гуанилил-трансфераза. Поскольку эукариотические рибосомы не связываются с мРНК без кэпа, вирусы эукариот для синтеза своих белков должны как-то решать эту проблему. Мелкие ДНК-вирусы, умеющие проникать в ядро сквозь ядерные поры, обычно используют гуанилил-трансферазу хозяина. РНК-вирусы создают на 5' концах своих мРНК сложные конструкции из шпилек (они называются IRES), которые имитируют форму белка eIF4E и позволяют РНК связаться с рибосомой без участия кэпа и eIF4E. Крупные ДНК-вирусы обычно имеют свою собственную гуанилилтрансферазу и производят матричные РНК с кэпами. В ходе эволюции эти ферменты могли передаваться между хозяевами и вирусами в обоих направлениях, но где они появились исходно?
Белл провел филогенетический анализ ферментов пришивания кэпа, который показывает, что ферменты эукариот образуют на дереве единую самостоятельную ветвь (рис. 18.12). Случай переноса фермента из клетки вирусу отразился бы на этом дереве вирусной веткой среди эукариот, но ничего такого мы не видим. А значит, следов переноса гуанилилтрансферазы от клеток вирусам нет.
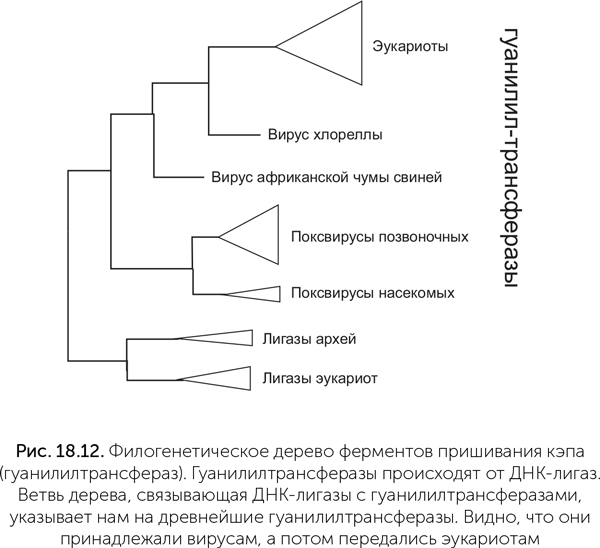
Чтобы понять, какой из узлов дерева гуанилилтрансфераз самый древний и соответствует предковому ферменту, к ним добавлены родственные ферменты – АТФ-зависимые ДНК-лигазы. Это более древние белки, предковые по отношению к гуанилилтрансферазам. Соответственно, та часть дерева гуанилилтрансфераз, которая выходит из лигазной части дерева, укажет нам древнейшую гуанилилтрансферазу. Оказывается, она принадлежала вирусам: первая ветвь ее потомков содержит ферменты поксвирусов (вирус оспы и его родственники), вторая – ферменты вируса ASF (африканской чумы свиней – African swine fever) и третья – вируса хлореллы. Гуанилилтрансферазы эукариот происходят от фермента вирусной линии, давшей начало вирусам ASF и хлореллы. Это доказывает, что кэпирование мРНК, как и другие инновации в генетических системах, появилось сначала среди вирусов и лишь затем было заимствовано эукариотами.
Для вирусов, в отличие от клеток, есть очевидная выгода в создании такой системы. Это средство перехвата управления клеткой хозяина. Вирус вносит в клетку фермент, который разрушает клеточные матричные РНК без кэпа и не трогает вирусные мРНК с кэпом. Белок eIF4E тоже мог сначала появиться у вирусов как средство захвата рибосом хозяина. Он присоединяется к рибосомам, после чего они узнают только вирусные мРНК с кэпом, останавливая синтез белков клетки. Современные клеточные eIF4E обычно связаны с рибосомами. У мимивируса[21] обнаружен собственный белок-аналог eIF4E, роль его пока непонятна.
Такемура обратил внимание на систему репликации ДНК эукариот. По сравнению с машинами репликации бактерий и архей эукариотическая версия сложна и медлительна. Если у бактерий и архей скорость репликации составляет около 1000 нуклеотидов в секунду, то у эукариот обычно около 50. Там, где многие бактерии и археи обходятся одной ДНК-полимеразой (см. главу 14), эукариоты используют три родственные. Дельта-полимераза копирует отстающую цепь, эпсилон-полимераза – лидирующую, а альфа-полимераза имеет неожиданную функцию. Она удлиняет РНК-затравки на 15–20 нуклеотидов уже из ДНК, после чего уступает место полимеразам дельта и эпсилон. Альфа-полимераза часто делает ошибки, поэтому созданные ею фрагменты ДНК потом удаляются одновременно с РНК-затравками, и дельта-полимераза строит на их месте точные копии ДНК-матрицы. Кроме этих трех ДНК-полимераз у большинства эукариот есть четвертая – дзета-полимераза. Она заменяет другие полимеразы, когда нужно срочно скопировать поврежденную ДНК и нет времени на ее починку.
Все четыре эукариотические полимеразы принадлежат к семейству PolB (глава 14), но достаточно сильно различаются между собой. На родословном дереве ДНК-полимераз эукариот, архей и вирусов (рис. 18.13) хорошо видно, что полимераза эпсилон унаследована эукариотами от архей, полимераза дельта – от вирусов, а полимеразы альфа и дзета образуют отдельные ветви, начинающиеся ближе к корню дерева, чем ?. Об их происхождении нельзя судить точно, но они тоже могли попасть в клетки эукариот от каких-то вымерших или еще не открытых вирусов.
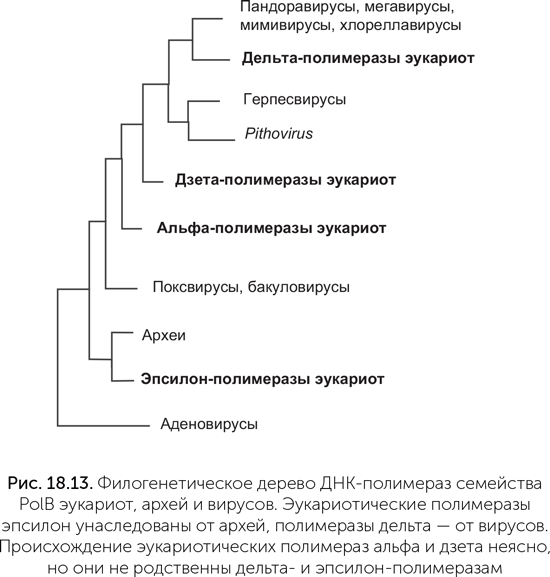
Наконец, Патрик Фортерр связал с вирусами происхождение огромного количества эукариотических белков, которые не похожи ни на какие белки бактерий и архей (Forterre, 2011). По последним оценкам, общий предок современных линий эукариот уже имел более 1400 таких белков. Среди них преобладают вспомогательные белки цитоскелета и ДНК-связывающие белки, в структуре которых присутствуют многочисленные короткие повторы. Вирусы, особенно крупные, содержат много генов, не похожих ни на какие гены клеточных организмов, а часто и на гены других вирусов. Кодируемые ими белки тоже часто имеют множественные короткие повторы. Низкая точность вирусных полимераз, интенсивная рекомбинация и «гонка вооружений» с хозяевами приводят к очень быстрой эволюции вирусных белков по сравнению с клеточными, поэтому вирусы – обильный источник принципиально новых белков.
| <<< Назад Гипотезы о происхождении ядра |
Вперед >>> Вирусная теория происхождения ядра и полового размножения |
- Клетки с ядром – новый уровень сложности жизни
- Химерное происхождение эукариот
- Другие возможные источники генов эукариот
- Архейный предок эукариот
- Причины и механизмы появления эукариот
- Гипотезы о происхождении ядра
- Роль вирусов в происхождении эукариот
- Вирусная теория происхождения ядра и полового размножения
- Дальнейшая эволюция эукариот
- Глава 7. Происхождение эукариот: эндосимбиоз, удивительная история интронов и исключительная важность единичных событий ...
- Эволюция в мире микробов и вирусов и трехдоменное древо жизни
- Эукариотическая клетка, ее внутренняя архитектура и пропасть между прокариотической и эукариотической клеточной организа...
- Сложный, «растущий» LECA и темные века эволюции эукариот
- Генная архитектура эукариот: наглядная демонстрация неадаптивной теории эволюции генома
- Корни эукариот среди архей и бактерий
- Поиск архейного и бактериального «родителей» эукариот
- Роль языка в происхождении сознания
- 10. Эукариотическая клетка. Цитоплазма. Органоиды
- Логика случая. О природе и происхождении биологической эволюции
