Книга: Самая главная молекула. От структуры ДНК к биомедицине XXI века
Иммунотерапия рака
| <<< Назад Команда «Умри!» |
Вперед >>> ДНК и сердце |
Иммунотерапия рака
Идея напустить иммунную систему пациента на его же собственную злокачественную опухоль впервые возникла на рубеже XIX и XX веков. Нью-йоркский врач Уильям Коли нарочно заражал раковых пациентов стрептококком, чтобы вызвать острую иммунную реакцию. В 10 % случаев пациенты вылечивались от рака. Однако такой подход не получил широкого распространения из-за низкой эффективности терапии. В середине 1980-х годов за разработку иммунотерапии рака взялся Стивен Розенберг из Национального института исследования рака (США). Он решил использовать для этой цели определенный класс Т-лимфоцитов, точнее, Т-киллеров. Они способны распознать и обезвредить, а попросту убить раковые клетки.
Розенберг обрабатывал Т-киллеры, взятые из крови больного, специальным белком, ростовым фактором Т-лимфоцитов. Этот белок называют интерлейкин-2, его нарабатывают в больших количествах стандартными методами генной инженерии. Затем размноженные Т-киллеры вводились в кровь пациента. Розенбергу удалось таким способом полностью исцелить больную меланомой – считавшейся неизлечимой формой рака кожи. У ряда других больных наблюдалось резкое уменьшение размера опухолей. Исследования Розенберга первоначально вызвали огромный интерес у специалистов и широкой публики. Но и этот подход не получил распространения, видимо, тоже из-за малого процента успешного вылечивания. Скорее всего, низкий процент успеха был связан с тем, что раковые клетки научались защищаться от Т-киллеров, как уже обсуждалось в предыдущем разделе. Потребовалось еще 30 лет упорной работы, чтобы методы иммунотерапии рака наконец стали широко внедряться.
Наиболее продвинутым в медицинскую практику является метод блокады контрольных точек иммунитета, разработанный, главным образом, Джеймсом Эллисоном из Ракового центра им. М. Д. Андерсона Техасского университета. Исследователям удалось разобраться, как раковые клетки избегают того, чтобы быть уничтоженными Т-киллерами. В арсенале раковых клеток таких способов несколько, мы остановимся на одном из них (рис. 48). Т-клетки несут на своей поверхности рецептор, белок PD-1. Коварная раковая клетка выставляет на своей поверхности другой белок, лиганд PD-1, или PD—L1. Когда Т-киллер приближается к раковой клетке, чтобы ее убить, PD—L1 вступает в контакт с рецептором PD-1, и в результате внутрь Т-клетки, к ее ДНК, идет команда «Умри!», и включается механизм апоптоза. Ведь акроним PD означает «запрограммированная смерть» (programmed death). На самом деле все оказалось не так драматично, как первоначально думали. Т-клетка не совершает самоубийство, она получает сигнал «Отставить!», т. е. отказывается убивать раковую клетку. Ну так давайте, решили исследователи, наработаем специальные антитела, которые будут связываться с рецептором PD-1 или с его лигандом, PD—L1, или и с тем и с другим, тем самым блокируя взаимодействие между рецептором и лигандом! Тогда команда «Отставить!» не пройдет, и Т-киллер благополучно слопает раковую клетку (рис. 48). Это и была та «Эврика!», которая привела к революции в терапии рака.
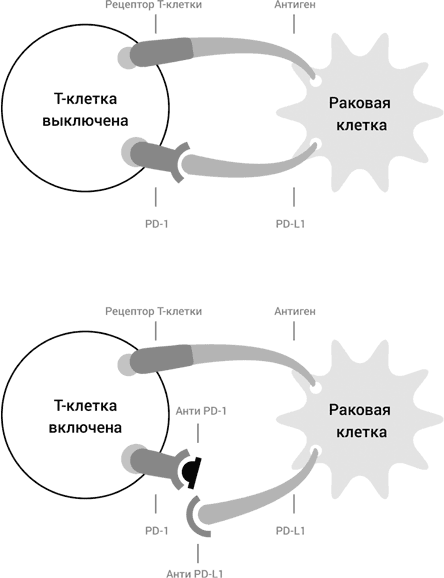
Рис. 48. Иммунотерапия рака, основанная на блокировке контрольных точек иммунитета. Сверху: раковая клетка выставляет лиганд рецептора PD-1, PD-L1 и тем самым выключает Т-клетку. Внизу: антитела к рецептору PD-1 и к лиганду PD-L1 препятствуют связыванию рецептора и лиганда и тем самым не позволяют раковой клетке командовать: Т-клетка узнает антиген на поверхности раковой клетки и уничтожает ее
Блокаторами контрольных точек иммунитета являются антитела. Их вводят пациенту, и происходит настоящее чудо: зловреднейшая меланома скукоживается и исчезает. Антитела против PD-1 и PD—L1 особенно эффективны именно против меланомы IV стадии, в ситуации, считавшейся безнадежной до наступления эры иммунотерапии. Но иммунотерапия работает и в случае некоторых других форм рака. Конечно, не все пациенты вылечиваются, но уже здравствуют тысячи людей, которым первоначально был вынесен смертный приговор.
Хорошо помню, как в августе 2015 года в телевизоре неожиданно появился бывший президент США Джимми Картер и объявил, что у него диагностирована меланома IV стадии, причем метастазы уже обнаружены в мозгу. Ему тогда было 90 лет. Ситуация казалась безнадежной, но Картер держался очень мужественно, шутил, все время улыбался. Ему прописали лечение антителами блокирующими контрольные точки иммунитета. В марте 2016 года Картер опять появился в ящике и объявил, что он признан врачами полностью чистым от рака. Именно благодаря успехам в лечении считавшихся ранее безнадежными случаев рака при помощи антител президент Обама объявил в конце 2015 года о государственной программе борьбы с раком, аналогичной космической программе «Аполлон» 1960-х годов. Эту программу возглавил вице-президент Джо Байден, сын которого умер от рака в расцвете лет.
Почему блокировка контрольных точек иммунитета помогает далеко не всегда и вообще работает не для всех видов рака? Почему опухоль одних пациентов прекрасно реагирует на терапию и случается прямо-таки чудо, как в случае с Картером, а в других случаях такого не происходит? Попробуем разобраться, в чем может быть причина. Ведь блокировка при помощи антител лишь нейтрализует защиту раковой клетки против иммунной системы. В основе иммунотерапии лежит способность Т-клеток распознать в раковой клетке чужака. Такое распознавание происходит потому, что раковые клетки несут соматические мутации, и в результате на поверхности раковой клетки презентуются мутантные белки, которые распознаются иммунной системой как антигены. Поскольку это новые для организма антигены, их называют неоантигенами.
Основная причина разного ответа на терапию в разных случаях, наверное, в том, что у каждого пациента имеется свой конкретный неоантиген на поверхности раковых клеток и одни неоантигены способны сильно стимулировать иммунный ответ, а другие не способны. Если это так, то следует помочь иммунной системе адекватно ответить на появление неоантигена. Как мы помогаем иммунной системе адекватно реагировать на вирусную инфекцию? Правильно, при помощи вакцин. Так возникла идея антираковой вакцины. В отличие от антивирусных вакцин, антираковая не предотвращает болезнь, но лечит ее, т. е. это терапевтическая вакцина.
Пока еще такие вакцины не используются в клинической практике, хотя уже идут клинические испытания после того, как опыты на мышах дали очень обнадеживающие результаты. Когда такие вакцины начнут применяться в больницах, это будет началом персональной терапии. Потому что цель антираковой вакцины состоит в максимальном стимулировании Т-клеток на атаку раковых клеток конкретной опухоли у конкретного пациента.
Здесь необходимо пояснить, что, в отличие от рецепторов В-клеток, рецепторы Т-клеток (РТК) распознают не сам белок-антиген как таковой. РТК распознает отдельные пептиды, содержащие примерно по 10 аминокислотных остатков, нарезанные из белка-антигена. Именно такие пептиды презентуются на поверхности клетки, в которой экспрессируется белок-антиген, специальным белковым устройством, составляющим важнейшую часть иммунной системы, которым оборудована каждая клетка. Это устройство носит название «главный комплекс гистосовместимости», сокращенно: ГКГС. Вот такой презентуемый с помощью ГКГС пептид и распознает рецептор конкретной Т-клетки. В зависимости от типа Т-клетки такое распознавание приводит либо к наработке Т-киллеров, способных убивать клетки, презентующие этот конкретный пептид, либо, если распознавшая пептид клетка сама есть Т-киллер, – к непосредственному убийству клетки. Как же будет работать персонифицированная антираковая вакцина?
Выделенная из клеток опухоли пациента ДНК секвенируется, и ее последовательность сравнивается с последовательностью ДНК из нормальной клетки пациента. Таким образом идентифицируется множество неоантигенов. Как было только что объяснено, такими неоантигенами служат не полные белки, а короткие пептиды, состоящие из примерно 10 аминокислотных остатков. Все пептиды, имеющие последовательности, содержащие аминокислотные замены, по сравнению с пептидами, которые соответствуют ДНК нормальных, нераковых клеток пациента, входят в лонг-лист кандидатов на вакцину. С помощью специальной компьютерной программы из этого лонг-листа выбирают шорт-лист пептидов, обладающих наибольшим сродством к ГКГС. Так получают 5–10 пептидов, которые должны в наибольшей степени стимулировать иммунную систему пациента на то, чтобы она атаковала клетки опухоли. Затем отобранные пептиды синтезируют, и смесь их всех или только нескольких из них и представляет собой антираковую вакцину, которую вводят пациенту. Весь это путь уже пройден в опытах на мышах, и уже начаты клинические испытания на больных. Довольно скоро должно стать ясно, оправдывает ли эта радикально новая иммунотерапия рака возложенные на нее ожидания.
И метод блокады контрольных точек иммунитета, и метод антираковых вакцин основан на использовании в полной мере собственного потенциала иммунной системы пациента. Упорно разрабатывается еще более радикальный подход, восходящий к ранним попыткам иммунотерапии, которые делал Розенберг и о которых мы упоминали выше. Идея состоит в том, чтобы извлечь Т-киллеры из крови пациента и как-то с ними проманипулировать. Розенберг просто размножал Т-киллеры и потом вводил их обратно пациенту. А что, если провести манипуляции с геномом Т-клеток, заменив имеющийся у них ТКР на ТРК, узнающий с большой эффективностью антиген, присущий данной опухоли пациента и к тому же посылающий мощный сигнал внутрь Т-клетки, к ее ДНК, сигнал об усиленном размножении? Такая технология, разработанная в Институте им. Вейцмана в Израиле, представляет собой высший пилотаж использования генетически модифицированных клеток для терапии рака. Она получила название «Технология химерного антигенного рецептора Т-клеток» или, сокращенно, ХАР-Т.
Хотя громадный потенциал технологии уже был продемонстрирован на пациентах, пока что это слишком грозное оружие в борьбе с раком, чтобы его можно было внедрять в практику. Если генетически модифицированные Т-киллеры обнаруживают даже ничтожное присутствие антигена на поверхности здоровой клетки, они набрасываются на нее и расправляются с ней. В результате несколько пациентов умерло в ходе клинических испытаний. Но в то же время имеется замечательный случай успешного применения этой технологии, информация о котором облетела в свое время все мировые СМИ.
Это произошло в Лондоне в 2015 году. В возрасте трех месяцев девочка Лайла заболела чрезвычайно острой формой лейкемии. Никакие стандартные методы лечения болезни не помогали, и казалось, что ребенок обречен. Даже иммунотерапия не работала, поскольку у ребенка почти не вырабатывались свои собственные Т-клетки. Тогда доктора, заручившись согласием родителей девочки и контролирующих органов, пошли на отчаянный шаг. Они связались с исследователями, незадолго до того разработавшими новый вариант технологии ХАР-Т, направленной как раз на лечение лейкемии, в котором не требовалось использовать Т-клетки пациента. Как такое может быть? Ведь введение в организм Т-клеток донора вместо собственных Т-клеток пациента должно вызывать сильнейшую реакцию отторжения! Чтобы избежать этого, исследователи, используя технологию редактирования генома (только использовалась не новейшая технология КРИСПР-кас, о которой мы подробно говорили в главе 10, а одна из более ранних технологий), так изменили геном Т-клеток донора, несущих химерный рецептор, что на этих Т-клетках не презентовались белки-антигены донора. Иными словами, исследователям удалось сделать Т-клетки-невидимки, не распознаваемые иммунной системой пациента.
Результат превзошел самые смелые ожидания. Лайла выздоровела и уже больше года развивается совершенно нормально. Совсем недавно в той же больнице удалось проделать то же самое еще с одним ребенком. Следует еще раз подчеркнуть, что подобные случаи пока единичны и метод ХАР-Т пока далек от внедрения в медицинскую практику. Но, безусловно, у этого метода огромный потенциал.
| <<< Назад Команда «Умри!» |
Вперед >>> ДНК и сердце |
- 27. Иммунопрофилактика, иммунотерапия, иммунокоррекция
- 3. Иммунотерапия
- Иммунотерапия
- Глава 41 Иммунопрофилактика и иммунотерапия
- Микробиология
- 25. Аутоиммунные процессы
- 26. Методы иммунодиагностики
- 41. Туберкулез. Диагностика. Профилактика. Лечение
- 3. Диагностика. Профилактика. Лечение
- 2. Иммунопрофилактика
