Книга: Биология. Общая биология. Базовый уровень. Учебник для 10–11 класс
2.5. Органические вещества. Углеводы. Белки
| <<< Назад 2.4. Органические вещества. Общая характеристика. Липиды |
Вперед >>> 2.6. Органические вещества. Нуклеиновые кислоты |
2.5. Органические вещества. Углеводы. Белки
Вспомните!
Какие вещества называют биологическими полимерами?
Каково значение углеводов в природе?
Назовите известные вам белки. Какие функции они выполняют?
Углеводы (сахара). Это обширная группа природных органических соединений. В животных клетках углеводы составляют не более 5 % сухой массы, а в некоторых растительных (например, клубни картофеля) их содержание достигает 90 % сухого остатка. Углеводы подразделяют на три основных класса: моносахариды, дисахариды и полисахариды.
Моносахариды рибоза и дезоксирибоза входят в состав нуклеиновых кислот (рис. 11). Глюкоза присутствует в клетках всех организмов и является одним из основных источников энергии для животных. Широко распространена в природе фруктоза – фруктовый сахар, который значительно слаще других Сахаров. Этот моносахарид придает сладкий вкус плодам растений и меду.
Если в одной молекуле объединяются два моносахарида, такое соединение называют дисахаридом. Самый распространенный в природе дисахарид – сахароза, или тростниковый сахар, – состоит из глюкозы и фруктозы (рис. 12). Ее получают из сахарного тростника или сахарной свеклы. Именно она и есть тот самый «сахар», который мы покупаем в магазине.
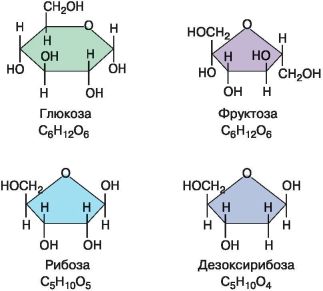
Рис. 11. Структурные формулы моносахаридов
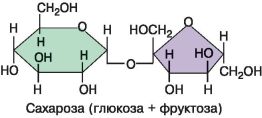
Рис. 12. Структурная формула сахарозы (дисахарида)
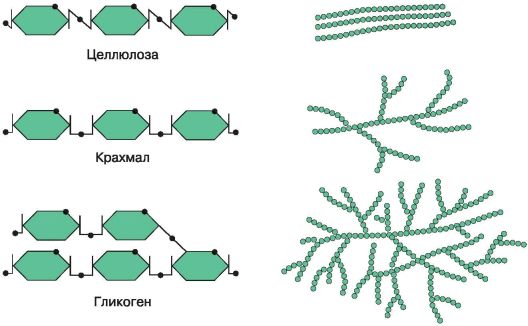
Рис. 13. Строение полисахаридов
Сложные углеводы – полисахариды, состоящие из простых Сахаров, выполняют в организме несколько важных функций (рис. 13). Крахмал для растений и гликоген для животных и грибов являются резервом питательных веществ и энергии.
Крахмал запасается в растительных клетках в виде так называемых крахмальных зерен. Больше всего его откладывается в клубнях картофеля и в семенах бобовых и злаков. Гликоген у позвоночных содержится главным образом в клетках печени и мышцах. Крахмал, гликоген и целлюлоза построены из молекул глюкозы.
Целлюлоза и хитин выполняют в живых организмах структурную и защитную функции. Целлюлоза, или клетчатка, образует стенки растительных клеток. По общей массе она занимает первое место на Земле среди всех органических соединений. По своему строению очень близок к целлюлозе хитин, который составляет основу наружного скелета членистоногих и входит в состав клеточной стенки грибов.
Белки (полипептиды). Одними из наиболее важных органических соединений в живой природе являются белки. В каждой живой клетке присутствует одновременно более тысячи видов белковых молекул. И у каждого белка своя особая, только ему свойственная функция. О первостепенной роли этих сложных веществ догадывались еще в начале XX в., именно поэтому им дали название протеины (от греч. protos – первый). В различных клетках на долю белков приходится от 50 до 80 % сухой массы.

Рис. 14. Общая структурная формула аминокислот, входящих в состав белков
Строение белков. Длинные белковые цепи построены всего из 20 различных типов аминокислот, имеющих общий план строения, но отличающихся друг от друга по строению радикала (R) (рис. 14). Соединяясь, молекулы аминокислот образуют так называемые пептидные связи (рис. 15).
Две полипептидные цепи, из которых состоит гормон поджелудочной железы – инсулин, содержат 21 и 30 аминокислотных остатков. Это одни из самых коротких «слов» в белковом «языке». Миоглобин – белок, связывающий кислород в мышечной ткани, состоит из 153 аминокислот. Белок коллаген, составляющий основу коллагеновых волокон соединительной ткани и обеспечивающий ее прочность, состоит из трех полипептидных цепей, каждая из которых содержит около 1000 аминокислотных остатков.
Последовательное расположение аминокислотных остатков, соединенных пептидными связями, является первичной структурой белка и представляет собой линейную молекулу (рис. 16). Закручиваясь в виде спирали, белковая нить приобретает более высокий уровень организации – вторичную структуру. И наконец, спираль полипептида сворачивается, образуя клубок (глобулу) или фибриллу. Именно такая третичная структура белка и является его биологически активной формой, обладающей индивидуальной специфичностью. Однако для ряда белков третичная структура не является окончательной.
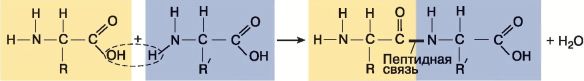
Рис. 15. Образование пептидной связи между двумя аминокислотами
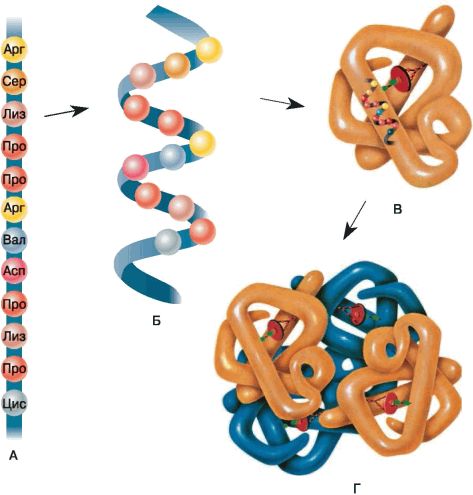
Рис. 16. Строение белковой молекулы: А – первичная; Б – вторичная; В – третичная; Г – четвертичная структуры
Может существовать четвертичная структура – объединение нескольких белковых глобул или фибрилл в единый рабочий комплекс. Так, например, сложная молекула гемоглобина состоит из четырех полипептидов, и только в таком виде она может выполнять свою функцию.
Функции белков. Огромное разнообразие белковых молекул подразумевает столь же широкое разнообразие их функций (рис. 17, 18). Около 10 тыс. белков-ферментов служат катализаторами химических реакций. Они обеспечивают слаженную работу биохимического ансамбля клеток живых организмов, ускоряя во много раз скорость химических реакций.
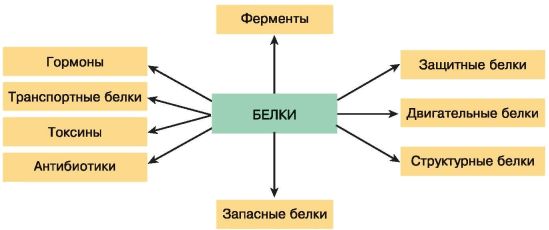
Рис. 17. Основные группы белков
Вторая по величине группа белков выполняет структурную и двигательную функции. Белки участвуют в образовании всех мембран и органоидов клетки. Коллаген входит в состав межклеточного вещества соединительной и костной ткани, а основным компонентом волос, рогов и перьев, ногтей и копыт является белок кератин. Сократительную функцию мышц обеспечивают актин и миозин.
Транспортные белки связывают и переносят различные вещества и внутри клетки, и по всему организму.
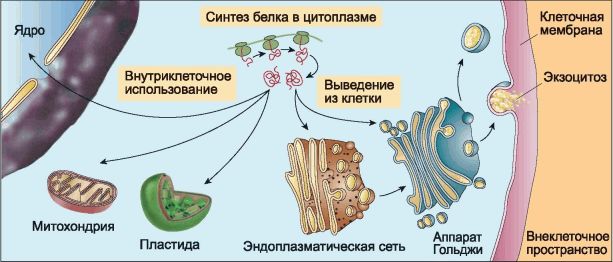
Рис. 18. Синтезированные белки или остаются в клетке для внутриклеточного применения, или выводятся наружу для использования на уровне организма
Белки-гормоны обеспечивают регуляторную функцию.
Например, соматотропный гормон, вырабатываемый гипофизом, регулирует общий обмен веществ и влияет на рост. Недостаток или избыток этого гормона в детском возрасте приводит, соответственно, к развитию карликовости или гигантизма.
Чрезвычайно важна защитная функция белков. При попадании в организм человека чужеродных белков, вирусов или бактерий на защиту встают иммуноглобулины – защитные белки. Фибриноген и протромбин обеспечивают свертываемость крови, предохраняя организм от кровопотери. Есть у белков и защитная функция несколько иного рода. Многие членистоногие, рыбы, змеи и другие животные выделяют токсины – сильные яды белковой природы. Белками являются и самые сильные микробные токсины, например ботулиновый, дифтерийный, холерный.
При нехватке пищи в организме животных начинается активный распад белков до конечных продуктов, и тем самым реализуется энергетическая функция этих полимеров. При полном расщеплении 1 г белка выделяется 17,6 кДж энергии.
Денатурация и ренатурация белков. Денатурация – это утрата белковой молекулой своей структурной организации: четвертичной, третичной, вторичной, а при более жестких условиях – и первичной структуры (рис. 19). В результате денатурации белок теряет способность выполнять свою функцию. Причинами денатурации могут быть высокая температура, ультрафиолетовое излучение, действие сильных кислот и щелочей, тяжелых металлов и органических растворителей.
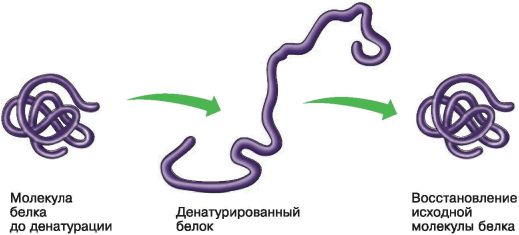
Рис. 19. Денатурация белка
Дезинфицирующее свойство этилового спирта основано на его способности вызывать денатурацию бактериальных белков, что приводит к гибели микроорганизмов.
Денатурация может быть обратимой и необратимой, частичной и полной. Иногда, если воздействие денатурирующих факторов оказалось не слишком сильным и разрушение первичной структуры молекулы не произошло, при наступлении благоприятных условий денатурированный белок может вновь восстановить свою трехмерную форму. Этот процесс называется ренатурацией, и он убедительно доказывает зависимость третичной структуры белка от последовательности аминокислотных остатков, т. е. от его первичной структуры.
Вопросы для повторения и задания
1. Какие химические соединения называют углеводами?
2. Что такое моно– и дисахариды? Приведите примеры.
3. Какой простой углевод служит мономером крахмала, гликогена, целлюлозы?
4. Из каких органических соединений состоят белки?
5. Как образуются вторичная и третичная структуры белка?
6. Назовите известные вам функции белков.
7. Что такое денатурация белка? Что может явиться причиной денатурации?
| <<< Назад 2.4. Органические вещества. Общая характеристика. Липиды |
Вперед >>> 2.6. Органические вещества. Нуклеиновые кислоты |
- 2.1. История изучения клетки. Клеточная теория
- 2.2. Химический состав клетки
- 2.3. Неорганические вещества клетки
- 2.4. Органические вещества. Общая характеристика. Липиды
- 2.5. Органические вещества. Углеводы. Белки
- 2.6. Органические вещества. Нуклеиновые кислоты
- 2.7. Эукариотическая клетка. Цитоплазма. Органоиды
- 2.8. Клеточное ядро. Хромосомы
- 2.9. Прокариотическая клетка
- 2.10. Реализация наследственной информации в клетке
- 2.11. Неклеточная форма жизни: вирусы
