Книга: Происхождение жизни. От туманности до клетки
Фосфорная проблема и пути ее решения
| <<< Назад Как сделать выбор между «цинковым» и «железосерным» мирами? |
Вперед >>> Наземные геотермальные поля – колыбель жизни? |
Фосфорная проблема и пути ее решения
Живые клетки содержат большое количество фосфора. Он входит в состав ДНК, РНК, энергетической «валюты» – АТФ и многих других жизненно важных молекул. Сахара присутствуют в клетках в основном в фосфорилированной форме. Однако в неживой природе фосфор существует практически только в виде фосфатных минералов, таких как апатит Ca5(PO4)3OH, которые нерастворимы в воде и химически инертны. Более того, высокая концентрация растворенного фосфата несовместима с клеточными концентрациями магния и кальция – их фосфаты плохо растворимы и должны выпадать в осадок. В клетке этого не происходит, потому что почти весь внутриклеточный фосфор находится в составе различных фосфорилированных органических молекул, соли которых с магнием и кальцием растворимы.
Как же собрать в колыбели жизни достаточно фосфора, причем в форме, пригодной для получения сахарофосфатов и нуклеотидов? В принципе, возможно несколько решений (рис. 6.6). Например, пирофосфат (P2O74?) растворим в воде в присутствии кальция и магния и, более того, способен служить источником энергии для биохимических реакций, подобно АТФ. Некоторые микроорганизмы и сейчас используют пирофосфат для тех реакций, которые у других организмов требуют затрат АТФ. Другая растворимая и химически активная форма фосфора – фосфит (HPO32?). Это соединение может окисляться до фосфата с выделением большого количества энергии и давно используется химиками для синтеза искусственной ДНК (Lestinger et al., 1975). Кроме того, многие бактерии обладают ферментами для окисления фосфита и могут использовать его как единственный источник фосфора. Некоторые бактерии даже способны получать энергию из процесса окисления фосфита.
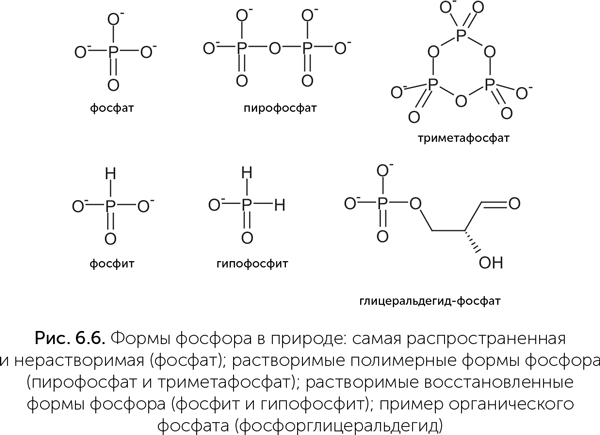
Где и как могли накопиться пирофосфаты или фосфиты в высоких концентрациях? Хорошим источником могут быть метеориты. В двух типах метеоритов (состоящие из железа и силикатов энстатитовые хондриты и железные метеориты) содержится до 0,1–0,5 % минерала шрайберзита (фосфид железа Fe3P). При попадании в воду шрайберзит постепенно разлагается, выделяя фосфиты, фосфаты, пирофосфаты, оксид железа и водород. До 50 % фосфора из шрайберзита переходит в фосфиты и до 5 % – в пирофосфаты. Фосфит устойчив к ультрафиолетовому излучению, не окисляется в отсутствии катализаторов и может сохраняться в морской воде сотни миллионов лет (Pasek et al., 2008).
Другой источник фосфитов и пирофосфатов – вулканы и связанные с ними наземные геотермальные источники. Измерения японских геохимиков на вулкане Усу (остров Хоккайдо) показали, что в выходящих из фумарол вулканических газах с температурой 540–700 °C содержится заметное количество летучих оксидов фосфора: P4O10, PO2 и P4O6. При лабораторном моделировании поведения жидкой лавы при температуре 1300 °C оказалось, что до 40 % фосфора из нее улетучивается в виде оксидов (Yamagata et al., 1991). Последующее растворение этих оксидов в воде дает фосфиты и пирофосфаты.
Вода многих наземных геотермальных источников обогащена соединениями фосфора: например, в грязевых котлах Мутновской сопки на Камчатке его концентрация достигает 0,01 % (Bortnikova et al., 2009). В большинстве геохимических анализов геотермальной воды измерялся общий уровень фосфора во всех формах, не различая фосфат, пирофосфат и фосфит, но для горячих источников Мамонтовых озер в Калифорнии показано, что до половины фосфора в их воде содержится в виде фосфита (Pech et al., 2009). В древних вулканических газах и геотермальных водах, скорее всего, содержание всех форм фосфора было еще в несколько раз выше, потому что древнейшие материки, как мы помним из главы 4, были сложены богатыми фосфором KREEP-базальтами.
Еще один механизм накопления фосфора связан с уже упомянутыми кристаллами сульфида цинка. Как мы помним, на свету эти кристаллы постепенно разрушаются. В качестве подходящего восстановителя для предохранения ZnS от фотокоррозии, как оказалось, идеально подходят восстановленные формы фосфора – фосфиты и гипофосфиты (H2PO2?). В присутствии фосфитов ZnS проводит восстановление CO2, сопряженное с окислением фосфита до фосфата. Более того, значительная часть этого фосфата соединяется с прилипшими к кристаллу органическими молекулами, образуя фосфорилированные сахара и кислоты, как в клетках. Это один из возможных путей накопления фосфорилированной органики в местах зарождения жизни.
| <<< Назад Как сделать выбор между «цинковым» и «железосерным» мирами? |
Вперед >>> Наземные геотермальные поля – колыбель жизни? |
- Проблема отходов
- Проблема измерения времени.
- Глава 1 Введение в проблематику биосферы
- 921. В каком месте побережья США проблема сброса канализационного отстоя в океан наиболее серьезна?
- Глобальное потепление — не единственная проблема
- 641. Почему проблема обрастания супертанкеров особенно сложна?
- Глава 11 Проблема АКО: перспективы кооперации
- 10.1. Проблема противодействия — общие аспекты
- Проблема гравитации в пяти измерениях
- Проблема НЛО
- ЧАСТЬ II. ЭКОЛОГИЯ, КАК ПОЛИТИЧЕСКАЯ ПРОБЛЕМА
- Проблема рубежа
