Книга: Естествознание. Базовый уровень. 10 класс
Схемы и уравнения реакций.
| <<< Назад § 50 Химические реакции |
Вперед >>> Типы химических реакций. |
Схемы и уравнения реакций.
Химические реакции обычно описывают с помощью уравнений. Химическим уравнением называют условную запись химической реакции посредством химических знаков и формул.
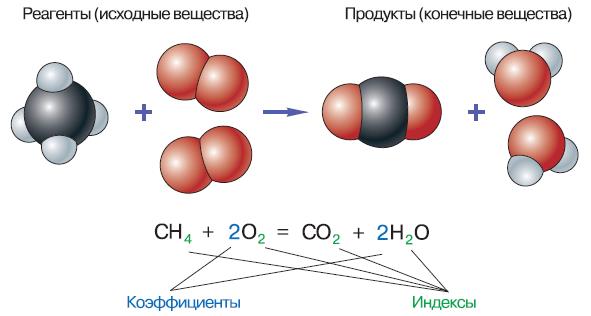
Рис. 130. Уравнение реакции и его изображение с помощью моделей
В левой части уравнения реакции записывают формулы веществ, которые вступают в реакцию (реагентов), а в правой – формулы конечных продуктов реакции (рис. 130).
Рассмотрим реакцию образования воды из кислорода и водорода. Химическая формула газообразного кислорода О2, а водорода – Н2. Составим схему реакции: Н2 + О2? Н2О. Для того чтобы она превратилась в уравнение, надо расставить коэффициенты: 2Н2 + O2 = 2H2O.
Коэффициенты в уравнении реакции показывают, в каком количественном соотношении находятся реагирующие вещества и продукты. Из полученного нами уравнения следует, что число вступающих в данную реакцию молекул водорода в два раза больше числа молекул кислорода. Смесь водорода и кислорода в соотношении 2: 1 называют гремучим газом, так как достаточно небольшого воздействия, например в виде искры, для того чтобы произошёл взрыв и образовалась вода.
Теперь разберём более сложный случай. Одним из важнейших процессов, обеспечивающих существование жизни на Земле, является осуществляемый растениями фотосинтез. В результате фотосинтеза из воды и углекислого газа образуются глюкоза и кислород. Рассмотрим схему и составим уравнение этой реакции. Формула глюкозы С6Н12О6. Следовательно, схема процесса выглядит так:
Н2О + СО2 ? С6Н12О6 + О2.
Расставив коэффициенты, получаем уравнение реакции:
6H2O + 6CO2 = C6H12O6 + 6O2.
По химическим уравнениям производят различные количественные расчёты в производственной и лабораторной практике. Например, попробуем определить, сколько граммов воды и углекислого газа потребуется для синтеза 1 г глюкозы. Для этого вспомним понятие моля. Моль – это такое количество вещества, масса которого, выраженная в граммах, численно равна его атомной или молекулярной массе. Молекулярная масса глюкозы равна сумме атомных масс входящих в её молекулу элементов, т. е. 6 12 + 12 • 1 + 6 • 16 = 180. Следовательно, масса одного моля глюкозы составляет 180 г. То же самое относится к воде, масса одного моля которой равна 18 г, и к углекислому газу, масса моля которого составляет 44 г. Значит, для получения 180 г глюкозы потребуется 108 г воды и 264 г углекислого газа. Итого 372 г. Но всем известно, что материя не исчезает. Куда же делись остальные 192 г? Очевидно, что это масса выделившегося кислорода. Проверим. В реакции образовалось 6 моль О2, каждый из которых имеет массу 32 г. Итого ровно 192 г. Как видите, закон сохранения массы и в этом случае оказался справедлив. Если вы хотите теперь узнать, сколько воды и углекислого газа потребуется для образования 1 г глюкозы и сколько при этом выделится кислорода, разделите все полученные числа на 180.
| <<< Назад § 50 Химические реакции |
Вперед >>> Типы химических реакций. |
- 95. Составление уравнений окислительно-восстановительных реакций.
- Практическое значение смещенных реакций
- 2.6. Биосинтез белка и нуклеиновых кислот. Матричный характер реакций биосинтеза. Генетическая информация в клетке. Гены...
- Типы химических реакций.
- Скорость и энергия химических реакций
- § 51 Скорость и энергия химических реакций
- Порядок возникновения реакций обмена веществ
- 6.2. Роль различных отделов цнс в регуляции лозно-тонических реакций
- 3.6.3. Особенности энергетики мышечной деятельности и реакций вегетативных систем на физические нагрузки
- 12.3.1. Принципиальные особенности реакций организма спортсменов на стандартные и предельные нагрузки
- Варианты ускоренных реакций агглютинации. Реакция пассивной гемагглютинации и ее варианты
- Запуск реакций.
