Книга: Естествознание. Базовый уровень. 10 класс
Изотопы
| <<< Назад Строение ядра. |
Вперед >>> Сильное и слабое взаимодействие. |
Изотопы
Может показаться, что каждый химический элемент должен всегда иметь определённое зарядовое число и определённую атомную массу. Однако это утверждение верно только в отношении зарядового числа. Ещё в начале XX в. было обнаружено, что некоторые элементы, проявляющие одинаковые свойства в химических реакциях, состоят из атомов, имеющих различную атомную массу. Атомы одного и того же элемента, имеющие различную массу, были названы изотопами. Встречающиеся в природе элементы чаще всего являются смесью нескольких изотопов, один из которых является преобладающим. Атомы всех изотопов одного элемента имеют одинаковый заряд ядра и, соответственно, занимают одно и то же место в периодической системе химических элементов. Различие между ними заключается в числе содержащихся в ядре нейтронов.
Ядро атома гелия чаще всего содержит два нейтрона, но встречаются изотопы, число нейтронов в ядре которых равно одному или трём. Кислород в природе может существовать в виде трёх изотопов с восемью, девятью или десятью нейтронами. При этом число протонов в ядре атома кислорода и, следовательно, его зарядовое число и атомный номер всегда равны восьми. Водород является первым элементом периодической системы элементов. Ядро его атома содержит всего один протон и чаще всего вообще не содержит нейтронов. Такой изотоп водорода называют протий. Однако в природном водороде содержится почти 0,02 % изотопа, называемого дейтерием и содержащего один нейтрон (рис. 115, А). Соответственно, атомная масса дейтерия равна двум.
Рассмотренные изотопы гелия, кислорода и водорода называют стабильными, так как они устойчивы и не подвергаются самопроизвольному распаду. К настоящему времени в природе обнаружено 270 стабильных изотопов. Кроме них существуют и нестабильные изотопы, ядро которых неустойчиво и подвержено постоянному распаду. Эти изотопы чаще всего встречаются у тяжёлых элементов, т. е. элементов с большой атомной массой. Нестабильные изотопы часто получают искусственно при помощи ядерных реакций. Таким способом можно получить, например, нестабильный изотоп водорода, в ядре которого находятся два нейтрона. Этот изотоп водорода называется тритием из-за того, что его атомная масса равна трём (один протон плюс два нейтрона) (см. рис. 115, А).
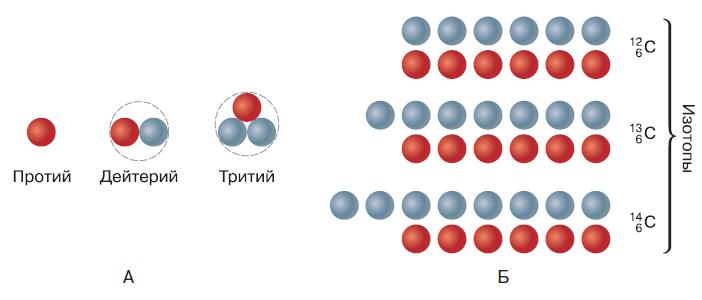
Рис. 115. Состав атомных ядер: А – водорода; Б – углерода (красные шарики – протоны, голубые – нейтроны)
Большинство природных химических элементов существуют в виде нескольких устойчивых изотопов (рис. 115, Б). Например, железо имеет четыре стабильных изотопа, ртуть – семь, а олово – десять. Поэтому атомная масса элементов выражается дробным числом. Так, хлор, встречающийся в природе, на 76,5 % состоит из изотопа с атомной массой, равной 35, и на 24,5 % – из изотопа с массой 37. Поэтому средняя атомная масса хлора равна приблизительно 35,5.
Как следует из самого названия, нестабильные изотопы не могут существовать в течение неограниченного периода времени и постоянно распадаются. Скорость распада ядер этих изотопов измеряется их периодом полураспада – временем, за которое первоначальное количество частиц уменьшается вдвое. У большинства нестабильных изотопов этот период составляет не более нескольких секунд, хотя известны изотопы с периодом полураспада в миллионы лет. Во время распада ядра таких атомов испускают радиоактивное излучение. Таким образом, можно сказать, что все неустойчивые изотопы обладают радиоактивностью (рис. 116).
Химические свойства элементов, т. е. их способность вступать в химические реакции, не зависят от числа нейтронов в ядре атома, а связаны со строением его электронной оболочки. Поэтому в химическом отношении все изотопы одного элемента являются абсолютно одинаковыми. Эту особенность используют во многих областях науки, техники и медицины. Таким образом можно, например, судить о превращениях какого-либо химического вещества в организме и о местах его включения в клетки и ткани. Можно синтезировать биологически активное вещество, включив в него неустойчивый радиоактивный изотоп какого-либо атома, например углерода или азота. В химическом и биологическом отношении это вещество ничем не будет отличаться от такого же вещества, не содержащего радиоактивного изотопа. В какие бы другие соединения это вещество ни превращалось, как бы ни изменялось строение его молекулы, радиоактивное излучение нестабильного атома всегда будет сохраняться. Если затем ввести это вещество в кровь, то, измеряя испускаемое этим изотопом слабое, безопасное для организма, радиоактивное излучение в различных участках человеческого тела, можно судить о том, где и в каких количествах накапливается в организме это вещество или продукты его обмена. Постепенно эти продукты или само вещество будут выводиться из организма, и по уменьшению радиоактивности можно определить скорость их выведения. Такой метод получил название исследования с применением «меченых атомов».
Рис. 116. Радиоактивный металл кюрий светится в темноте, испуская большое количество ядер гелия
| <<< Назад Строение ядра. |
Вперед >>> Сильное и слабое взаимодействие. |
- Межклеточное вещество
- 04. На что влияет нагрев планет звездами, звезд Ядрами Галактик, Ядер Галактик Ядрами Сверхгалактик
- Список литературы
- Разные человечества
- Красные тучи, закрывающие солнце
- Московская белая
- Муравей, семья, колония
- Примерные рационы для котят от месяца до пяти и старше
- Голосеменные растения завоевывают мир
- Пароль скрещенных антенн
- Позор страны
- Что такое водопад?
