Книга: Самая главная молекула. От структуры ДНК к биомедицине XXI века
Рентгеноструктурный анализ
| <<< Назад Эрвин Шрёдингер |
Вперед >>> Уотсон и Крик |
Рентгеноструктурный анализ
Среди тех мест, где был услышан призыв Шрёдингера, особенно большую роль суждено было сыграть двум английским научным центрам – прославленной Кавендишской лаборатории в Кембридже, главой которой некогда был Резерфорд, и Королевскому колледжу в Лондоне. Здесь разыгрались завершающие сцены драмы, развязкой которой стало выяснение физической природы гена.
Место действия не было случайным. Именно в Великобритании сформировалась к тому времени (начало 1950-х годов) самая сильная в мире научная школа рентгеноструктурного анализа. И именно этот метод оказался тем инструментом, который помог физикам проникнуть в тайну жизни.
Квантовая механика явилась теоретическим фундаментом для понимания внутреннего строения окружающих нас веществ – атомов, молекул и всевозможных состоящих из них материалов, будь то кусок железа или кристалл обыкновенной поваренной соли. Но многообразие структур, которые могут получаться из атомов, необозримо. Как узнать, какова структура того или иного конкретного материала? Тут теория обычно мало помогает. Можно, конечно, выдвинуть те или иные предположения, но нельзя утверждать наверняка – слишком много мыслимых вариантов. Необходим экспериментальный метод, который позволял бы напрямую выяснить атомное строение вещества. Именно таким методом и является рентгеноструктурный анализ.
Рентгеновские лучи знакомы всем – ими просвечивают, если вы сломали ногу или заболели воспалением легких. Физическая природа этих лучей та же, что и у видимого света или у радиоволн. Это все разные варианты электромагнитного излучения, различающиеся только длиной волны. Для рентгеновских лучей характерна длина волны порядка 10–10 м. Расстояние между атомами в молекулах и кристаллах имеет тот же масштаб. Это обстоятельство навело немецкого физика Макса фон Лауэ на мысль, что при прохождении рентгеновских лучей через кристалл, в котором атомы расположены строго регулярно, должна возникать дифракционная картина, подобная той, которая наблюдается при прохождении видимого света сквозь дифракционную решетку.
Опыты, проведенные в 1912 году, полностью подтвердили эту догадку. Когда пучок рентгеновских лучей направили на кристалл, за которым поместили фотопластинку, то после проявления фотопластинки на ней обнаружили причудливую, но весьма регулярную систему пятен (рис. 1). Вскоре стало ясно, что по распределению пятен на рентгенограмме и по их яркости можно судить о взаимном расположении атомов или молекул, образующих кристалл, и в случае молекул – даже об их внутреннем строении. Так возник метод рентгеноструктурного анализа. Наибольший вклад в его развитие внесли британские ученые Генри (отец) и Лоуренс (сын) Брэгги. Рентгеноструктурный анализ позволил точно определить структуру всех минералов, а также бесчисленного множества молекул.
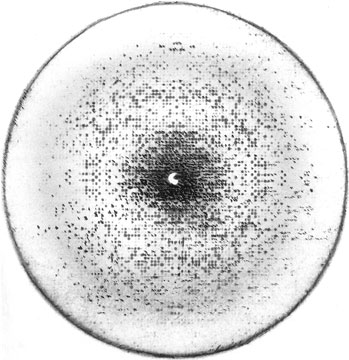
Рис. 1. Так выглядит рентгенограмма кристалла белка
Мало-помалу «рентгеноструктурщики» переходили к все более сложным объектам исследования и наконец в 1930-е годы обратили свои взоры к биологическим молекулам. Однако после первых же попыток стало ясно, что решение задачи им пока еще не по плечу. Прежде всего из биологических молекул очень трудно получить кристаллы. Но даже если это удавалось, десятки тысяч атомов, входящих в каждую молекулу, создавали на рентгенограмме такой причудливый узор, что восстановить по нему координаты всей этой массы атомов было просто невозможно. Потребовались многие годы, пока ученые научились решать столь сложные задачи.
Преодолением этих трудностей занимались в Кавендишской лаборатории в довоенные и послевоенные годы. Усилия лаборатории, руководимой Лоуренсом Брэггом, были сосредоточены на определении пространственного строения белков. Это и понятно. В те годы все были убеждены, что главная молекула живой природы – молекула белка. В самом деле, ферменты, т. е. молекулы, проводящие в клетке всевозможные химические превращения, – это всегда белки. Белок представляет собой главный строительный материал клетки. Неудивительно, что всеобщим было убеждение, что и гены устроены из белка. Казалось несомненным, что путь к разгадке всех тайн жизни лежит через изучение строения белков.
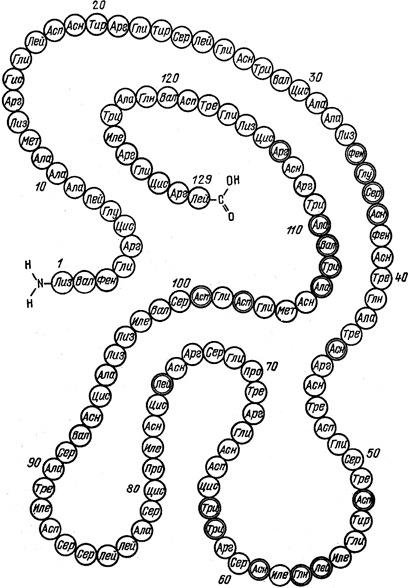
Рис. 2. Аминокислотная последовательность одного из белков (лизоцима.
Белок представляет собой полимерную молекулу, мономерными звеньями, «кирпичиками» которой служат аминокислотные остатки (рис. 2). Аминокислотные остатки располагаются всегда строго линейно, плечом к плечу, подобно солдатам, стоящим по стойке смирно. Но так устроен и биологически активный белок, и белок, нагретый, скажем, до 60 °C, когда он уже полностью теряет свою биологическую активность. Значит, одного химического строения белка, т. е. последовательности аминокислотных остатков, недостаточно для того, чтобы белок был биологически активен. Необходима еще совершенно определенная укладка в пространстве групп, закодированных на рис. 2 в виде сокращенных названий аминокислот, которые на самом деле вовсе не кружочки и не шарики, а имеют каждая свою весьма причудливую форму. Вот за то, чтобы определять пространственную структуру всей молекулы белка по рентгенограммам типа приведенной на рис. 1, и велась затяжная борьба в стенах Кавендишской лаборатории. Лишь в середине 1950-х годов Джону Кендрю и Максу Перуцу удалось добиться успеха – они научились определять трехмерную структуру белков. Это случилось уже после того, как была решена проблема устройства гена, – к чему, как оказалось, белки отношения вовсе не имеют.
| <<< Назад Эрвин Шрёдингер |
Вперед >>> Уотсон и Крик |
