Книга: Медицинская микробиология, иммунология и вирусология
Микробиология чумы
| <<< Назад Глава 60 Возбудители особо опасных инфекций |
Вперед >>> Иерсинии – возбудители псевдотуберкулеза (Y. pseudotuberculosis) и кишечного иерсиниоза (Y. enterocolitica) |
Микробиология чумы
Чума (pestis) – острое инфекционное заболевание, протекающее по типу геморрагической септицемии. В прошлом чума была грозным бичом для человечества. Известны три пандемии чумы, которые унесли миллионы человеческих жизней.
Первая пандемия была в VI в. н. э. От нее погибло с 531 по 580 г. около 100 млн человек – половина населения Восточной Римской империи («юстинианова» чума). Вторая пандемия разразилась в XIV веке. Она началась в Китае и поразила многие страны Азии и Европы. В Азии от нее погибло 40 млн человек, а в Европе из 100 млн человек погибло 25 млн. Вот как описывает эту пандемию Н. М. Карамзин в «Истории государства Российского»: «Болезнь обнаруживалась железами в мягких впадинах тела, человек харкал кровью и на второй или третий день умирал. Нельзя, говорят летописцы, вообразить зрелища более ужасного… От Пекина до берегов Евфрата и Ладоги недра земли наполнились миллионами трупов, и государства опустели… В Глухове и Белозерске не осталось ни одного жителя… Сия жестокая язва несколько раз приходила и возвращалась. В Смоленске она свирепствовала 3 раза, наконец, в 1387 г. осталось в нем только 5 человек, которые, по словам летописи, вышли и затворили город, наполненный трупами». Третья пандемия чумы началась в 1894 г. и закончилась в 1938 г., унеся 13 – 15 млн человеческих жизней.
Возбудитель чумы был открыт в 1894 г. французским ученым А. Иерсеном, в честь которого и получил название Yersinia pestis. Род Yersiniа относится к семейству Enterobacteriaceae и включает 11 видов, из них патогенными для человека являются три: Y. pestis, Y. pseudotuberculosis и Y. enterocolitica; патогенность остальных пока еще не ясна.
Y. pestis имеет длину 1 – 2 мкм и толщину 0,3 – 0,7 мкм. В мазках из организма больного и из трупов погибших от чумы людей и грызунов выглядит как короткая овоидная (яйцевидная) палочка с биполярной окраской. В мазках из бульонной культуры палочка располагается цепочкой, в мазках из агаровых культур – беспорядочно (см. цв. вкл., рис. 95). Биполярная окраска в том и другом случае сохраняется, но в мазках из агаровых культур несколько слабее. Возбудитель чумы по Граму окрашивается отрицательно, лучше красится щелочными и карболовыми красителями (синькой Леффлера), спор не образует, жгутиков не имеет. Содержание Г + Ц в ДНК – 45,8 – 46,0 мол % (для всего рода). При температуре 37 °C образует нежную капсулу белковой природы, которая выявляется на влажных и слегка кислых питательных средах. Y. pestis – аэроб, дает хороший рост на обычных питательных средах. Оптимальная для роста температура 27 – 28 °C (диапазон – от 0 до 45 °C), рН = 6,9 – 7,1. Палочка чумы дает характерный рост на жидких и плотных питательных средах: на бульоне он проявляется образованием рыхлой пленки, от которой спускаются нити в виде сосулек, напоминающих сталактиты, на дне – рыхлый осадок, бульон остается прозрачным. Развитие колоний на плотных средах проходит через три стадии: через 10 – 12 ч под микроскопом рост в виде бесцветных пластинок (стадия «битого стекла»); через 18 – 24 ч – стадия «кружевных платочков», при микроскопировании заметна светлая кружевная зона, расположенная вокруг выступающей центральной части, желтоватой или слегка буроватой окраски. Через 40 – 48 ч наступает стадия «взрослой колонии» – буровато-очерченный центр с выраженной периферической зоной (см. цв. вкл., рис. 95.3). Y. pseudotuberculosis и Y. enterocolitica стадии «битого стекла» не имеют. На средах с кровью колонии Y. pestis зернистые со слабо выраженной периферической зоной. С целью быстрейшего получения характерного для Y. pestis роста на средах к ним рекомендуется добавлять стимуляторы роста: сульфит натрия, кровь (или ее препараты) или лизат культуры сарцины. Палочке чумы свойствен выраженный полиморфизм, особенно на средах с повышенной концентрацией NaCl, в старых культурах, в органах разложившихся чумных трупов (см. цв. вкл., рис. 95.2). Чумная палочка не имеет оксидазы, не образует индола и H2S, обладает каталазной активностью и ферментирует глюкозу, мальтозу, галактозу, маннит с образованием кислоты без газа.
Резистентность. В мокроте палочка чумы может сохраняться до 10 дней; на белье и одежде, испачканных выделениями больного, сохраняется неделями (белок и слизь охраняют ее от губительного действия высыхания). В трупах людей и животных, погибших от чумы, выживает с начала осени до зимы; низкая температура, замораживание и оттаивание не убивают ее. Солнце, высыхание, высокая температура губительны для Y. pestis. Нагревание до 60 °C убивает через 1 ч, при температуре 100 °C погибает через несколько минут; 70° спирт, 5 % раствор фенола, 5 % раствор лизола и некоторые другие химические дезинфектанты убивают за 5 – 10 – 20 мин.
Антигенный состав. У Y. pestis, Y. pseudotuberculosis и Y. enterocolitica обнаружено до 18 сходных соматических антигенов. Для Y. pestis характерно наличие капсульного антигена (фракция I), антигенов T, V – W, белков плазмокоагулазы, фибринолизина, белков наружной мембраны и pH6-антигена. Однако в отличие от Y. pseudotuberculosis и Y. enterocolitica, Y. pestis в антигенном отношении более однородна;
серологической классификации этого вида нет.
Факторы патогенности. Y. pestis является самой патогенной и агрессивной среди бактерий, поэтому и вызывает наиболее тяжелое заболевание. У всех чувствительных к нему животных и у человека возбудитель чумы подавляет защитную функцию фагоцитарной системы. Он проникает в фагоциты, подавляет в них «окислительный взрыв» и беспрепятственно размножается. Неспособность фагоцитов осуществить свою киллерную функцию в отношении Y. pestis – основная причина восприимчивости к чуме. Высокая инвазивность, агрессивность, токсигенность, токсичность, аллергенность и способность подавлять фагоцитоз обусловлены наличием у Y. pestis целого арсенала факторов патогенности, которые перечислены ниже.
1. Способность клеток сорбировать экзогенные красители и гемин. Она связана с функцией системы транспорта железа и обеспечивает Y. pestis возможность размножаться в тканях организма.
2. Зависимость роста при температуре 37 °C от наличия в среде ионов Ca2+.
3. Синтез V – W-антигенов. Антиген W расположен в наружной мембране, а V – в цитоплазме. Эти антигены обеспечивают размножение Y. pestis внутри макрофагов. 4. Синтез «мышиного» токсина. Токсин блокирует процесс переноса электронов в митохондриях сердца и печени чувствительных животных, поражает тромбоциты и сосуды (тромбоцитопения) и нарушает их функции.
5. Синтез капсулы (фракции I – FraI). Капсула угнетает активность макрофагов.
6. Синтез пестицина – видовой признак Y. pestis.
7. Синтез фибринолизина.
8. Синтез плазмокоагулазы. Оба эти белка локализованы в наружной мембране и обеспечивают высокие инвазивные свойства Y. pestis.
9. Синтез эндогенных пуринов.
10. Синтез термоиндуцибельных белков наружной мембраны – Yop-белков (англ. Yersinia outer proteins). Белки YopA, YopD, YopE, YopH, YopK, YopM, YopN подавляют активность фагоцитов.
11. Синтез нейраминидазы. Она способствует адгезии (высвобождает рецепторы для Y. pestis).
12. Синтез аденилатциклазы. Предполагается, что она подавляет «окислительный взрыв», т. е. блокирует киллерное действие макрофагов.
13. Синтез пилей адгезии. Они угнетают фагоцитоз и обеспечивают внедрение Y. pestis, как внутриклеточного паразита, в макрофаги.
14. Синтез аминопептидаз широкого спектра действия.
15. Эндотоксин (ЛПС) и другие компоненты клеточной стенки, обладающие токсическим и аллергенным действием.
16. pH6-антиген. Он синтезируется при температуре 37 °C и низкой рН, подавляет фагоцитоз и обладает цитотоксическим действием на макрофаги.
Значительная часть факторов патогенности Y. pestis контролируется генами, носителями которых являются следующие 3 класса плазмид, обнаруживаемых обычно вместе у всех патогенных штаммов:
1) рYP (9,5 т. п. н.) – плазмида патогенности. Несет 3 гена:
pst – кодирует синтез пестицина;
pim – определяет иммунитет к пестицину;
pla – определяет фибринолитическую (активатор плазминогена) и плазмокоагулазную активность.
2) рYТ (65 МД) – плазмида токсигенности. Несет гены, определяющие синтез «мышиного» токсина (сложный белок, состоящий из двух фрагментов А и В, с м. м. 240 и 120 кД соответственно), и гены, контролирующие белковый и липопротеиновый компоненты капсулы. Третий ее компонент контролирует гены хромосомы. Ранее плазмида имела название pFra.
3) pYV (110 т. п. н.) – плазмида вирулентности. Она определяет зависимость роста Y. pestis при 37 °C от присутствия в среде ионов Ca2+, поэтому имеет другое название – Lcr-плазмида (англ. low calcium response). Гены этой, особенно важной, плазмиды кодируют также синтез антигенов V и W и термоиндуцируемых белков Yop. Их синтез осуществляется под сложным генетическим контролем при температуре 37 °C и в отсутствие в среде Ca2+. Все типы Yop-белков, кроме YopM и YopN, гидролизуются за счет активности активатора плазминогена (ген pla плазмиды pYP). Белки Yop во многом определяют вирулентность Y. pestis. YopE-белок обладает антифагоцитарным и цитотоксическим действием. YopD обеспечивает проникновение YopE в клетку-мишень; YopH обладает антифагоцитарной и протеин-тирозин-фосфатазной активностью; белок YopN – свойствами кальциевого сенсора; YopM связывается с ?-тромбином крови человека.
Эпидемиология. Круг теплокровных носителей чумного микроба чрезвычайно обширен и включает более 200 видов 8 отрядов млекопитающих. Основным же источником чумы в природе являются грызуны и зайцеобразные. Естественная зараженность установлена у более чем 180 их видов, свыше 40 из них входят в состав фауны России и сопредельных территорий (в пределах бывшего СССР). Из 60 видов блох, для которых в экспериментальных условиях установлена возможность переноса возбудителя чумы, на этой территории обитают 36.
Чумной микроб размножается в просвете пищеварительной трубки блох. В ее переднем отделе образуется пробка («чумной блок»), содержащая большое количество микробов. При укусе млекопитающих c обратным током крови в ранку с пробки смывается часть микробов, что и ведет к заражению. Кроме того, выделяемые блохой при питании экскременты при попадании в ранку также могут вызывать заражение.
Основные (главные) носители Y. pestis на территории России и Средней Азии – суслики, песчанки и сурки, в некоторых очагах также пищухи и полевки. С ними связано существование следующих очагов чумы:
1) 5 очагов, в которых основным носителем чумного микроба выступает малый суслик (Северо-Западный Прикаспий; Терско-Сунженское междуречье; Приэльбрусский очаг; Волго-Уральский и Зауральский полупустынные очаги).
2) 5 очагов, в которых носители – суслики и сурки (на Алтае – пищухи): Забайкальский, Горно-Алтайский, Тувинский и высокогорные Тянь-Шанский и ПамироАлайский очаги.
3) Волго-Уральский, Закавказский и Среднеазиатский пустынные очаги, где основные носители – песчанки.
4) Высокогорные Закавказский и Гиссарский очаги с основными носителями – полевками.
Разные классификации Y. pestis основываются на разных группах признаков – биохимических особенностях (глицерин-позитивные и глицерин-негативные варианты), области распространения (океанические и континентальные варианты), видах основных носителей (крысиный и сусликовый варианты). По одной из наиболее распространенных классификаций, предложенной в 1951 г. французским исследователем чумы Р. Девинья (R. Devignat), в зависимости от географического распространения возбудителя и его биохимических свойств различают три внутривидовые формы (биовара) Y. pestis (табл. 28).
По классификации отечественных ученых (Саратов, 1985), вид Y. pestis разделен на 5 подвидов: Y. pestis subsp. pestis (основной подвид; он включает все три биовара классификации Р. Девинья), Y. pestis subsp. altaica (алтайский подвид), Y. pestis subsp. caucasica (кавказский подвид), Y. pestis subsp. hissarica (гиссарский подвид) и Y. pestis subsp. ulegеica (улэгейский подвид).
Заражение человека происходит через укус блох, при прямом контакте с заразным материалом, воздушно-капельным, редко алиментарным путем (например, при употреблении мяса верблюдов, больных чумой). В 1998 – 1999 гг. чумой в мире переболело 30 534 человека, из них 2 234 умерли.
Дифференциальные признаки биоваров Y. pestis
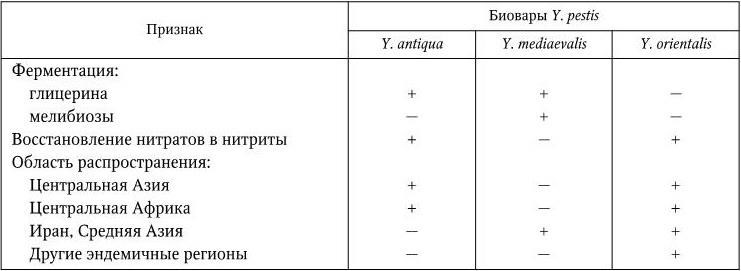
Таблица 28
Примечание. (+) – признак положительный; ( – ) – признак отсутствует.
Патогенез и клиника. В зависимости от способа заражения различают бубонную, легочную, кишечную форму чумы; редко септическую и кожную (гнойные пузырьки на месте укуса блохи). Инкубационный период при чуме варьирует от нескольких часов до 9 сут. (у лиц, подвергнутых серопрофилактике, до 12 сут.). Возбудитель проникает через мельчайшие повреждения кожи (укус блохи), иногда через слизистую оболочку или воздушно-капельным путем, достигает регионарных лимфатических узлов, в которых начинает бурно размножаться. Болезнь начинается внезапно: сильная головная боль, высокая температура с ознобом, лицо гиперемировано, затем оно темнеет, под глазами темные круги («черная смерть»). Бубон (увеличенный воспаленный лимфатический узел) появляется на второй день. Иногда болезнь развивается столь стремительно, что больной погибает раньше, чем появится бубон. Особенно тяжело протекает легочная чума. Она может возникнуть и как результат осложнения бубонной чумы, и при заражении воздушно-капельным путем. Болезнь развивается также очень бурно: озноб, высокая температура и уже в первые часы присоединяются боли в боку, кашель, вначале сухой, а потом с мокротой кровянистого характера; появляется бред, цианоз, коллапс, и наступает смерть. Больной легочной чумой представляет исключительную опасность для окружающих, так как выделяет с мокротой огромное количество возбудителя. В развитии болезни основную роль играет подавление активности фагоцитов: нейтрофильных лейкоцитов и макрофагов. Ничем не сдерживаемое размножение и распространение возбудителя через кровь по всему организму полностью подавляет иммунную систему и приводит (при отсутствии эффективного лечения) к гибели больного.
Постинфекционный иммунитет прочный, пожизненный. Повторные заболевания наблюдаются крайне редко. Природа иммунитета клеточная. Хотя антитела появляются и играют определенную роль в приобретенном иммунитете, он опосредуется главным образом Т-лимфоцитами и макрофагами. У лиц, переболевших чумой или вакцинированных, фагоцитоз имеет завершенный характер. Он и обусловливает приобретенный иммунитет.
Лабораторная диагностика. Используются бактериоскопический, бактериологический, серологический и биологический методы, а также аллергическая проба с пестином (для ретроспективной диагностики). Материалом для исследования служат: пунктат из бубона (или его отделяемое), мокрота, кровь, при кишечной форме – испражнения. Y. pestis идентифицируют на основании морфологии, культуральных, биохимических признаков, пробы с чумным фагом и с помощью биологической пробы. Простым и надежным методом определения антигенов чумной палочки в исследуемом материале является применение РПГА, особенно с использованием эритроцитарного диагностикума, сенсибилизированного моноклональными антителами к капсульному антигену, и ИФМ. Эти же реакции могут быть использованы для обнаружения антител в сыворотке больных.
Биологический метод диагностики заключается в заражении исследуемым материалом (когда он очень загрязнен сопутствующей микрофлорой) морской свинки накожно, подкожно или, реже, внутрибрюшинно.
При работе с материалом, содержащим возбудителя чумы, требуется соблюдение строгого режима, поэтому все исследования проводятся только хорошо обученным персоналом в специальных противочумных учреждениях.
Профилактика. Постоянный контроль за природными очагами чумы и организация мероприятий по предупреждению заболеваний людей в стране осуществляется специальной противочумной службой. Она включает в себя пять противочумных институтов и десятки противочумных станций и отделений.
Несмотря на наличие природных очагов, с 1930 г. на территории России в них не было ни одного случая заболевания людей чумой. Для специфической профилактики чумы используется живая ослабленная вакцина из штамма EV. Она вводится накожно, внутрикожно или подкожно. Кроме того, предложена сухая таблетированная вакцина для перорального применения. Поствакцинальный иммунитет формируется к 5 – 6-му дню после прививки и сохраняется в течение 11 – 12 мес. Для его оценки и ретроспективной диагностики чумы предложена внутрикожная аллергическая проба с пестином. Реакция считается положительной, если на месте введения пестина через 24 – 48 ч образуется уплотнение не менее 10 мм в диаметре и появляется краснота. Аллергическая проба положительна и у лиц, имеющих постинфекционный иммунитет.
Большой вклад в изучение чумы и организацию борьбы с ней внесли русские ученые: Д. С. Самойлович (первый не только в России, но и в Европе «охотник» за микробом чумы еще в XVIII в., он же первым предложил делать прививки против чумы), Д. К. Заболотный, Н. П. Клодницкий, И. А. Деминский (изучение природных очагов чумы, носителей возбудителя ее в очагах и т. п.) и др.
| <<< Назад Глава 60 Возбудители особо опасных инфекций |
Вперед >>> Иерсинии – возбудители псевдотуберкулеза (Y. pseudotuberculosis) и кишечного иерсиниоза (Y. enterocolitica) |
