Книга: Оптический флюорит
Природа оптических свойств флюорита
| <<< Назад Введение |
Вперед >>> Флюорит в природе |
Природа оптических свойств флюорита
Трудно найти минерал более универсального применения, чем флюорит — природное соединение кальция и фтора, фтористый кальций. Он является главным источником фтора и фтористых соединений для химической промышленности, которые используются буквально везде: от фреона в холодильниках и высокооктанового топлива до производства алюминия и даже космической техники [Петров, 1976]. Без флюорита как лучшего флюса невозможен современный металлургический процесс. Он широко применяется в цементной промышленности, в стекольном и эмалевом производстве, используется в электродуговой сварке для электродных покрытий и приготовления флюсов. Кроме того, он является одним из важнейших оптических материалов, о чем будет идти речь ниже.
Флюорит (fluore, нем. — течь) получил свое наименование из-за своего важного свойства снижать температуру плавления металлов в смесях с ним и придавать текучесть шихте. Пожалуй, впервые под близким к современному названию «флюорес» флюорит описан в знаменитом «Диалоге о металлах» Г. Бауэра (Агриколы). У этого научного названия минерала много синонимов, по-разному звучащих на разных языках, но смысл их один и тот же, и лучше всего он выражен в русском бытовом названии «плавиковый шпат». Оно отражает сразу оба главных качества флюорита: и способность быть металлургическим флюсом-плавиком, и оптическое совершенство («шпат», а шпаты от немецкого «spalten» — раскалывать — неметаллические минералы с совершенной спайностью).
Исключительно важное значение флюорита в современной технике, особенно в оптическом приборостроении, определяется совокупностью его свойств, которые детально охарактеризованы в специальной литературе [Степанов, Феофилов, 1957; Воронкова и др., 1965; Справочник..., 1980]. Здесь мы остановимся лишь на оптических свойствах.
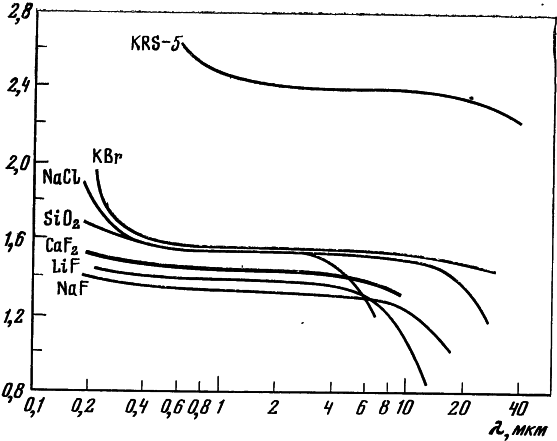
Рис. 1. Зависимость показателя преломления (n) от длины волны (?) для флюорита и ряда других кристаллических материалов
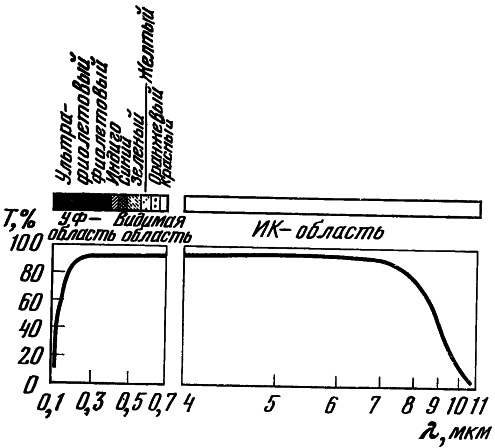
Рис. 2. Спектральное пропускание (T) флюорита в ультрафиолетовой, видимой и инфракрасной областях спектра
Флюорит оптически изотропен, т. е. все его оптические свойства не зависят от направления в кристалле. Он характеризуется относительно низким показателем преломления (n), который имеет (при 19° С) следующие значения для различных длин волн (?):
| n | ?, мкм | n | ?, мкм |
|---|---|---|---|
| 1,6421 | 1,1311 | 1,47635 | 0,2288 |
| 1,5152 | 0,1819 | 1,30756 | 9,724 |
Показатель преломления мало зависит от длины волны (рис. 1), для него характерен типичный для щелочно-галоидных кристаллов ход частной дисперсии. Температурный коэффициент показателя преломления (dn/dt) варьирует от —6,2?10-6/°С для ? = 0,2288 мкм до —5,6?10-6/°С для ? = 9,724 мкм; минимальное значение установлено для ? = 0,852 мкм и равно —10,6?10-6/°С.

Рис. 3. Границы спектрального пропускания различных оптических материалов
Особенно важным свойством флюорита является его высокая прозрачность в широком спектральном диапазоне: от 0,125 мкм в вакуумной ультрафиолетовой (УФ) (шумановской) до 11 мкм в инфракрасной (ИК) областях спектра (рис. 2). На рис. 3 приведены сравнительные данные о диапазонах пропускания. Среди различных оптических материалов нет ни одного, для которого так удачно, как для флюорита, сочетались бы оптические характеристики. Только немногие искусственные кристаллы имеют более коротковолновую границу пропускания — это кристаллы фтористого лития LiF, фтористого магния MgF2, дигидрофосфата аммония NH4H2PO4(ADP). Но они либо имеют двойное лучепреломление, либо характеризуются низкой твердостью, либо водо- и кислотонеустойчивы (табл. 1), что ограничивает их применение в оптическом приборостроении. Ряд материалов, имеющих в ИК-области более длинноволновую границу пропускания, чем у фтористого кальция, уступают ему по пропусканию в УФ-диапазоне и могут использоваться исключительно в спектральных приборах для ИК-области. Это бромистый калий KBr, бромистый цезий CsBr, йодистый калий KI, KRS-5 (состава TlBr — TlI).
Таблица 1. Оптические характеристики некоторых кристаллов
| Кристалл | Показатель преломления nD | Твердость, кг/мм2 | Растворимость в воде, г/100 г | Коэффициент линейного расширения ??106 |
|---|---|---|---|---|
| CaF2 | 1,4338 | 120 | 1,31?10-3 | 19,5 |
| NaF | 1,336 | 60 | 4,2 | — |
| NaCl | 1,54432 | 18 | 26,0 | 42 |
| LiF | 1,3915 | 99 | 0,27 | 41 |
| MgF2 | n0 = 1,3777 | 415 | 7,6?10-3 | 11 |
| ne = 1,3895 |
Все оптические характеристики флюорита высокостабильны. Эти особые свойства определяют незаменимость оптического флюорита при создании высококорректированных оптических систем (апохроматов, планапохроматов), обеспечивающих высокое качество изображения и ограничение хроматических аберраций. Вместе с тем прозрачность и достаточно большая дисперсия флюорита в УФ-области спектра обусловливают его использование в объективах современных ультрафиолетовых микроскопов и при изготовлении призменной оптики в вакуумных приборах (спектрографах, монохроматорах и др.).
Благоприятные механические, технические и эксплуатационные характеристики кристаллов флюорита в сочетании с прозрачностью в широком спектральном диапазоне, высокой оптической однородностью, отсутствием двойного лучепреломления, люминесценции, высокой радиационной устойчивостью и лучевой прочностью определяют и ряд новых его практических применений в тепловидении и фурье-спектроскопии, астрономии, космической технике, в квантовой и силовой оптике и т. д.
Области практического применения оптического флюорита непрерывно расширяются, в связи с чем энергично возрастают и потребности в этом уникальном оптическом материале.
Свойства флюорита, в том числе и оптические, определяются его конституцией, т. е. химическим составом и кристаллической структурой.
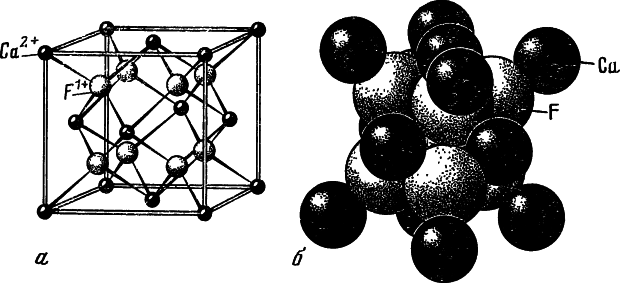
Рис. 4. Различные модели кристаллической структуры флюорита
Объяснение в тексте
Флюорит (по химической номенклатуре — фтористый кальций CaF2) состоит из атомов кальция (51,33%) и фтора (48,67%), закономерно упакованных по принципу гранецентрированной кубической кристаллической решетки. Это значит, что если мы соединим мысленно все взаимодействующие друг с другом атомы по кратчайшим расстояниям между ними прямыми линиями, то получим регулярную пространственную решетку, которая состоит из бесконечного множества совершенно одинаковых элементарных ячеек, как бы размножающихся в пространстве. Кристаллохимики называют такие ячейки параллелепипедами повторяемости.
Элементарная ячейка флюорита представляет собой куб, разделенный на восемь маленьких кубиков — октантов. Ионы кальция (Ca2+) располагаются по вершинам большого куба и по центрам каждой из его граней, а ионы фтора (F-) — в центрах каждого октанта. Каждый ион фтора оказывается, таким образом, окруженным четырьмя ионами кальция (FCa4), располагающимися по вершинам тетраэдра, который называется координационным, а каждый ион кальция находится внутри координационности куба, образованного восемью ионами фтора (CaF8).
Если изобразить ионы кальция и фтора разноцветными шариками, то элементарная ячейка флюорита будет выглядеть так, как показано на рис. 4, а. На первый взгляд кажется, что в ней слишком много ионов кальция. Но нужно учесть, что каждый ион кальция в вершинах ячейки принадлежит восьми ячейкам, а располагающийся на грани — двум ячейкам. Так что «собственных» ионов кальция здесь всего (1 : 8?8+1 : 2?6), ионов фтора — восемь, а число формульных единиц CaF2 в ячейке z — четыре. Если шарики, изображающие ионы, «раздуть» до их истинных размеров, характеризуемых эффективными радиусами (Са2+ = 1,04 ?, F- = l,33 ?), то получим более близкую к реальной, хотя и менее наглядную модель структуры флюорита (см. рис. 4, б). Структуру флюорита можно изобразить также в виде анионных полиэдров — Ca-кубов или катионных F-тетраэдров. Размер ребра элементарной ячейки ?0 = 5,46295±0,00010 ?.
Рассмотренная схема кристаллической структуры флюорита является идеальной. Реальная структура несколько сложнее, и это связано прежде всего с тем, что во флюорит, кроме кальция и фтора, в тех или иных количествах входят атомы некоторых других элементов. Ионы F- могут частично замещаться кислородом О2-, но основные вариации химического состава связаны с изоморфными замещениями Са2+ на Ag+, Cd2+, Ge2+, Cu+, Hg2+, In3+, Mn2+, Sn2+, Sr2+, Sb3+, Tl3+, Pb4+, Th4+, U4+ и особенно на двух- и трехвалентные ионы редкоземельных элементов — TR2+(Sm2+, Eu2+, Yb2+ и др.) и TR3+(Y3+, Се3+, La3+, Lu3+ и др). Элементы-примеси присутствуют во флюорите обычно в незначительных количествах, однако содержание редких земель иногда может достигать десятков процентов. Максимально возможное содержание TRF3 во флюорите, не разрушающее его структуру, 50%. Механизм замещения двухвалентного кальция трехвалентным иттрием или другими редкими землями довольно своеобразный. Ионные радиусы этих элементов близки друг другу (Y3+ = 0,97 ?, Са2+ = 1,04 ?), и при вхождении YF3 в структуру CaF2 иттрий занимает места ионов кальция. При этом две трети ионов фтора заполняют все тетраэдрические позиции, которые им и положено занимать, а одна треть их входит в октаэдрические пустоты между катионами кальция, бывшие в CaF2 незаполненными. В результате такого изоморфизма «с заполнением пространства» плотность и показатель преломления иттрофлюорита по сравнению с флюоритом повышаются, увеличивается параметр элементарной ячейки до ?0 = 5,50 ?. При замещении кальция трехвалентными ионами редкоземельных элементов происходит компенсация избыточного заряда эквивалентными количествами ионов О2-, Na+ и других элементов по схемам
Ca2+ + F- ? TR3+ + O2-,
2Ca2+ ? TR3+ + Na+ и т. п.
Вхождение изоморфных примесей во флюорит изменяет многие его структурно-чувствительные физические свойства.
Большое влияние на свойства флюорита оказывают структурные дефекты. Структура кристаллов флюорита, как и вообще любых других кристаллов, всегда содержит множество локальных нарушений (точечных, линейных, плоскостных, объемных), возникающих в процессе кристаллизации в результате «ошибок» при встраивании в кристалл кристаллообразующих частиц, вхождении чужеродных примесных элементов, захвате включений и т. п.
Для кристаллов флюорита характерны все типы точечных дефектов. К простейшим точечным дефектам относятся вакансии, образующиеся в результате того, что в узлах решетки отсутствуют ионы кальция (такие дефекты называются дефектами Шоттки). Другой тип точечных дефектов (дефекты Френкеля) образуется, когда атом (ион) из узла решетки перемещается в междоузлие. Вызываемые ими нарушения в решетке строго локализованы — размеры их сравнимы с межатомными расстояниями. К точечным дефектам также относятся комплексы из небольшого числа простейших дефектов, если размеры нарушений не превышают нескольких межатомных расстояний. Такие комплексы иногда называют кластерами.
Точечные дефекты, располагаясь в целом хаотически, способны к упорядоченному расположению вдоль определенных кристаллографических направлений. Вследствие этого возникает анизотропия, особенно выраженная, если дефекты создаются примесями, например оптическая анизотропия в кубических кристаллах, в том числе в кристаллах флюорита.
Миграция дефектов по кристаллу, усиливающаяся с повышением температуры, приводит к их дальнейшему объединению и образованию более крупных, макроскопических, областей нарушений, влияющих на первичные свойства кристалла. Структурные дефекты могут быть причиной явлений, не характерных для идеального кристалла флюорита, — окраски, интенсивной люминесценции и др. В то же время, зная природу этих свойств, можно целенаправленно изменять их, вводя в структуру дефекты нужного «сорта». На этом основано, например, использование кристаллов фтористого кальция, легированных Sm2+, Dy2+, Nd3+, Er3+ в лазерной технике, а также в мазерах.
Основными линейными дефектами являются дислокации, образующиеся в результате сдвига атомных слоев друг относительно друга на одно межатомное расстояние. Дислокации могут быть краевыми, представляющими собой край «оборванной» в результате сдвига атомной плоскости, и винтовыми (фото 1, см. вкл.), в которых линия, последовательно соединяющая атомы один за другим, является винтовой. Вблизи дислокации кристалл сильно деформирован, причем если ширина деформированной зоны соответствует размерам точечного дефекта, то длина ее может достигать миллионов межатомных расстояний — дислокация как бы пронизывает кристалл насквозь. Плотность дислокаций, определяемая как число дислокационных линий, пересекающих площадку в 1 см2 в кристалле, может достигать в сильно деформированных кристаллах 1012. В хороших оптических кристаллах фтористого кальция она составляет 104 и менее на 1 см2. Плотностью дислокаций, их распределением и перемещением внутри кристалла определяются механические свойства флюорита.
Объемными дефектами являются блочность, мозаичность, широко проявляющиеся как на природных, так и на искусственных кристаллах флюорита (фото 2, см. вкл.), участки с внутренними напряжениями, скопления включений и т. п.
Дефектность структуры флюорита оказывает большое влияние на его оптические свойства. Примеси редкоземельных элементов, вакансии и другие точечные дефекты приводят к снижению пропускания в УФ-области спектра, появлению полос поглощения в видимом диапазоне и окрашенности кристаллов.
Природа разнообразной окраски и люминесценции флюорита детально рассмотрена в ряде работ [Пшибрам, 1959; Архангельская, 1970; Марфунин, 1974, 1975; Платонов, 1976; Таращан, 1978]. Простейшим центром окраски является F-центр (Farbe, нем. — цвет), представляющий собой вакансию отрицательно заряженного иона (аниона), захватившую электрон. Поглощение энергии F-центром соответствует переходу F-электрона с одного уровня на другой.
Величина поглощенной энергии ?Е = Е2—Е1 принимает не непрерывные значения, а «квантуется» — поглощение происходит дискретными порциями, квантами энергии hv: ?E = hv, где h — постоянная Планка, равная 6,626?10-34 Дж?с; v — частота, с-1. Вместо частоты используется волновое число, обратное длине волны: v' = 1/?, (см-1), которое связано с частотой отношением v' = v/c, где с — скорость света, м/с.
Таким образом, ?E = hcv' = hc1/?. Из этого уравнения видно, что чем больше величина поглощенного кванта, тем меньше длина волны, соответствующая поглощению света веществом. Таким образом, спектральное положение F-полосы определяет окраску кристалла.
Первые эксперименты по искусственному окрашиванию флюорита были выполнены Л. Вёлером в 1905 г. Он окрасил кристалл флюорита в синий цвет, нагревая его в парах кальция. Впоследствии эксперименты по аддитивному окрашиванию природного флюорита провели Г. Хаберландт и Е. Мольво. В спектрах поглощения таких кристаллов присутствуют две полосы поглощения — 375 (?-полоса) и 520 нм (?-полоса) — так называемый спектр Мольво, которые отождествляются с поглощением на F-центрах. Было установлено, что при аддитивном окрашивании в кристалле возникает избыточное, по сравнению со стехиометрическим составом, содержание атомов щелочного металла (обычно порядка 1016—1019 атомов на 1 см3). Это, в свою очередь, приводит к избытку свободных электронов, которые, перемещаясь по кристаллу, захватываются анионными вакансиями с образованием F-центров. Теоретические расчеты также дают количественное соответствие между величиной полного спектрального поглощения в F-полосе и тем избыточным количеством щелочного металла, которое устанавливается химическим анализом окрашенного кристалла. Кроме того, известно, что плотность аддитивно окрашенных кристаллов флюорита обычно меньше, чем у неокрашенных, за счет присутствия вакансий, однако твердость их выше.
Другим методом искусственного создания центров окраски является облучение кристаллов жестким излучением — рентгеновскими, ?-лучами, частицами высоких энергий. Активация центров окраски происходит и в природных условиях.
В кислородсодержащих кристаллах флюорита с высоким содержанием анионных вакансий после радиационного окрашивания П. П. Феофилов обнаружил две полосы поглощения — 370 и 560 нм, которые он отождествил с F2-центрами, представляющими собой парные анионные вакансии с двумя локализованными на них электронами. Такие же центры были обнаружены и в кристаллах SrF2.
В природных кристаллах флюорита обычно наблюдаются сложные центры окраски, представляющие собой агрегаты из двух, трех и четырех примыкающих друг к другу элементарных F-центров. Соответственно они обозначаются: F2-, F3- и F4-центры или М (F2-центр), R1 и R2 (F3-центр), N (F4-центр). В природных условиях образованию F-агрегатных центров способствует диффузия дефектов решетки с их последующей агрегацией в процессе роста и дальнейшего существования кристалла в изменяющихся температурных и радиационных полях. Такие сложные центры наиболее устойчивы к термическому обесцвечиванию. Они в противоположность простым F-центрам, как бы пройдя «естественный отбор», чаще наблюдаются в природных кристаллах.
Описанные центры окраски во флюорите являются по своей природе электронными. Кроме них, существуют дырочные центры окраски, которые отождествляются с ионами фтора, утратившими электрон, — F0. Эти центры устойчивы только при низких температурах.
Кроме электронно-дырочных центров, в объяснении окраски флюорита определенную роль играют примесные дефекты. Это прежде всего дефекты, связанные с внедрением ионов редкоземельных элементов в структуру флюорита. Причем роль двух- и трехвалентных ионов в окраске существенно различна в силу специфических особенностей их энергетического состояния. В спектрах CaF2 — TR3+ полосы поглощения, соответствующие (f—d)-переходам в пределах внутренней, защищенной от внешних влияний оболочки, попадают в далекую, за пределами видимой, УФ-область спектра. В видимой и прилегающей к ней части спектры TR3+-ионов, обусловленные (f—f)-переходами, имеют линейчатый характер, т. е. состоят из серии очень узких линий. Поэтому влияние ионов TR3+ на цвет флюорита практически исключается, тем более что концентрация редкоземельных элементов, а следовательно, и интенсивность полос поглощения незначительные.

Рис. 5. Спектр поглощения (1) и люминесценции (2) кристалла флюорита зеленой окраски
1 — при комнатной температуре; 2 — при —160° С
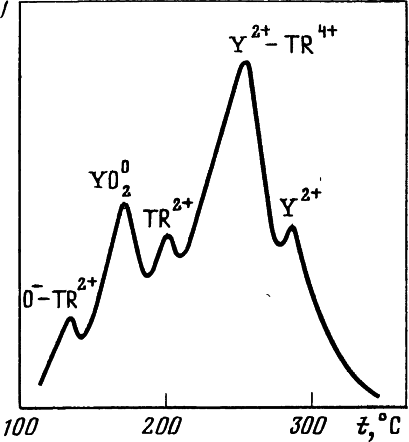
Рис. 6. Кривая термолюминесценции флюорита с полосами излучения на различных центрах
По-другому проявляют себя ионы TR2+. Они имеют широкие интенсивные полосы поглощения, соответствующие (f—d)-переходам и расположенные в видимой и ближней УФ-области спектра. Узкие слабые полосы (f—f)-переходов полностью перекрываются первыми, и поэтому окраска целиком определяется широкими полосами поглощения TR2+.
Наиболее значительное влияние на окраску флюорита оказывают Sm2+, Eu2+, Dy2+, Yb2+. Полосы поглощения других TR2+-ионов располагаются в ИК-области спектра.
П. П. Феофиловым [1956] было показано, что зеленая окраска кристаллов флюорита обусловлена двухвалентным самарием. В видимой области спектра у кристаллов CaF2—Sm2+ фиксируются две интенсивные полосы поглощения: ~425 и ~630 нм (рис. 5). В определенных условиях ионы могут переходить из одного валентного состояния в другое, вызывая тем самым изменение окраски кристалла. На этом основано окрашивание кристаллов с помощью ?-облучения и, наоборот, их обесцвечивание при нагревании.
Значительное влияние на оптические свойства флюорита оказывает присутствие кислорода в его структуре. Кислородсодержащие кристаллы имеют интенсивное поглощение начиная с 200—220 нм, поэтому непригодны для изготовления оптических деталей к приборам, предназначенным для вакуумной УФ-области. При этом O2-, внедряясь в структуру, размещается в ближайшем к TR3+ узле анионной подрешетки, представляя собой одиночный ион или образуя диполи с анионными вакансиями VF. С присутствием таких ассоциированных пар О2-—2VF связаны появление красно-фиолетовой окраски и пурпурно-красная люминесценция облученных кристаллов флюорита. 2VF-центры такого типа называются «красными» М-центрами. Во флюорите П. Л. Смолянским были установлены и «синие» М-центры, связанные с присутствием Na+.
Одним из широко известных свойств флюорита является люминесценция, природа которой также связана с дефектами его структуры. Явление люминесценции известно с древнейших времен. Еще Плиний Старший (23— 79 гг.) в легенде о светящихся в темноте камнях упоминает об «огненном хризолампсисе». Видимо, речь здесь шла именно о флюорите. Со второй половины XVII в. природа люминесценции флюорита уже рассматривалась в научной литературе. Еще до недавнего времени считалось, что люминесценция является чуть ли не неотъемлемым свойством флюорита, однако сейчас известно, что есть природные и искусственно созданные кристаллы флюорита, которые не имеют люминесценции. Это кристаллы высокой степени чистоты, практически свободные от дефектов. Люминесценция может возникать под воздействием различных причин: при фотовозбуждении (фотолюминесценция), при возбуждении катодными (катодолюминесценция) и рентгеновскими (рентгенолюминесценция) лучами, при нагревании (термолюминесценция), трении (триболюминесценция) и т. д.
Фотолюминесценция. Наиболее характерным видом свечения флюорита при фотовозбуждении является синефиолетовая люминесценция. Она возникает при облучении ультрафиолетовыми лучами с длиной волны ?=365 нм и объясняется присутствием во флюорите Eu2+. Спектр излучения Eu2+ состоит из четко выраженной полосы в фиолетовой области спектра (~430 нм). При температуре жидкого азота (77K) разгорается желто-зеленая люминесценция с максимумом в области 570 нм, обусловленная примесью Yb2+. Если возбуждение проводить длиной волны 400 нм, то обнаруживается красная люминесценция, вызванная присутствием Sm2+. Такое поведение связано с особенностями характеристических спектров поглощения этих ионов.
В спектрах фотолюминесценции были отмечены линии излучения и трехвалентных ионов — Sm3+, Dy3+, Tb3+, Er3+, наблюдаемые в видимой области спектра.
Рентгенолюминесценция. Очень интересным явлением, связанным с примесями редкоземельных элементов, является рентгенолюминесценция флюорита. Рентгеновские лучи обладают высокой проникающей способностью и значительно большей энергией кванта по сравнению со световыми лучами. Люминесценция возникает при переходах между электронными уровнями внутренних оболочек атомов в кристалле, тогда как фотолюминесценция — при переходах между уровнями внешних электронов. В связи с этим в спектрах рентгенолюминесценции появляются дополнительные линии по сравнению с оптическим возбуждением.
По спектрам рентгенолюминесценции удалось идентифицировать как центры на собственных дефектах решетки флюорита, так и примесные ионы, изоморфно входящие в структуру [Таращан, 1978; Красильщикова и др., 1981]. У кристаллов флюорита с невысоким содержанием редкоземельных элементов, порядка тысячных долей процента, в спектрах рентгенолюминесценции линии их излучения весьма слабы. Основные полосы излучения наблюдаются в УФ-области около 280 нм (дырочный VR-центр) и на границе видимой и ИК-области с максимумом 750 нм (дырочный F2--центр). В спектрах рентгенолюминесценции флюорита, обогащенного примесями редкоземельных элементов, в зависимости от количественного соотношения различных ионов, от формы их вхождения, способа локальной компенсации заряда, симметрии центра наблюдаются различные комбинации линий излучения этих центров. По спектрам рентгенолюминесценции были зафиксированы полосы излучения на Mn2+, а также центры на ионах TR с различной зарядовой компенсацией — кислородной (тригональные центры Dy3+—O2-; Sm3+—O2-; Er3+—O2-), натриевой (ромбические для Er3+), фторовой (тетрагональные для Er3+). Расшифровка спектров рентгенолюминесценции флюорита весьма сложна, особенно для природных образцов, характеризующихся различными наборами примесей, сложными физико-химическими и температурными условиями образования.
Термолюминесценция. Такой же сложный характер имеют кривые термовысвечивания флюорита, для которого зафиксировано множество центров захвата и высвечивания на различных дефектах. Термовысвечивание кристаллов CaF2 происходит в широком спектральном диапазоне от 300 до 800 нм и состоит из серии полос и линий различной интенсивности, принадлежащих к различным активаторам. В процессе нагревания образца излучение происходит вначале в видимой области спектра, а при дальнейшем повышении температуры, когда высвобождаются электроны из более глубоких энергетических ловушек, преобладающим становится ультрафиолетовое излучение. Каждому активатору соответствуют свои линии и полосы излучения, проявляющиеся при тех или иных температурах. В результате на кривой термовысвечивания в определенных температурных интервалах наблюдаются максимумы свечения, природа которых иногда имеет сложный многоцентровой характер.
Природа центров захвата электронов и центров свечения по кривым и максимумам термолюминесценции не может быть установлена. Эти данные получают с помощью методов спектроскопии, в частности электронного парамагнитного резонанса (ЭПР).
Термолюминесценция в системе CaF2, содержащей примеси TR, представляет собой рекомбинационный процесс, так как центры свечения (TR3+) и центры захвата (дефекты термического и примесного происхождения) пространственно разделены. Во флюорите установлены следующие основные центры захвата и свечения.
Центр O- — TR2+. Это дипольный центр, возникающий в результате изоморфных замещений иона Ca2+ ионами TR3+ с компенсацией избыточной валентности ионом кислорода. При возбуждении происходит переход электрона с O2- на TR3+; обратный же переход сопровождается излучением иона TR в интервале температур 130-150° С (рис. 6).
Центр YO02. Он образуется при изоморфном замещении Y3+ ? Ca2+ и локализации двух ионов O2- в соседних вакансиях F. Образующийся комплекс Y3+ — O4-2 в результате облучения захватывает дырку и может рассматриваться как молекула YO02. Запасенная этими центрами световая энергия в природных образцах высвечивается обычно через ионы-активаторы — Mn2+ или TR3+ в области 200-220° С.
Центр TRO02 Дырочный центр, аналогичный YO02. Чаще всего встречается в кристаллах флюорита, образовавшихся в сильно окислительных условиях. С ним связан максимум термовысвечивания при 330° С.
Центр TR2+. Устойчивые центры на двухвалентных ионах редкоземельных элементов образуются в условиях, когда часть свободных дырок локализована на глубоких уровнях захвата, что сдерживает их миграцию по кристаллу и соответственно препятствует переводу иона TR2+ в трехвалентное состояние. Наиболее устойчивыми двухвалентными ионами во флюорите являются Eu2+, Yb2+, Sm2+, Dy2+. В связи с тем, что энергия их термической ионизации достаточно большая, максимумы термовысвечивания располагаются в области высоких температур (~400°С). В природных кристаллах в области 200—250° С наблюдались пики высвечивания на ионах Nd2+, Er2+, Ho2+.
Взаимосвязи конституционных особенностей и физических свойств флюорита, главные из которых мы рассмотрели в этой главе, позволяют прогнозировать свойства кристаллов и, наоборот, по оптическим показателям судить о кристаллохимии исследованных кристаллов флюорита.
| <<< Назад Введение |
Вперед >>> Флюорит в природе |
- Введение
- Природа оптических свойств флюорита
- Флюорит в природе
- Поиски путей замены природного флюорита. Искусственные кристаллы
- Индустрия искусственных кристаллов флюорита
- Кристаллы с заданными свойствами
- Флюорит в оптической технике
- Заключение
- Литература
- Сноски из книги
- Содержание книги
- Популярные страницы
- О будущем оптических телескопов
- Индустрия искусственных кристаллов флюорита
- Месторождения оптических кристаллов
- Очистка природного флюорита и подготовка шихты
- Таблица 7.1. Координаты и компоненты скорости Апофиса в эпоху JD 2454200,5 (10.04.2007) и их средние ошибки, полученные ...
- Добыча и обработка оптических кристаллов. Изготовление деталей
- Обработка кристаллов и изготовление оптических деталей
- Проникновение в субмикрокосмос
- Таблица 7.2. Минимальные расстояния между Землей и Апофисом 13 апреля 2029 г.
- 126. Почему астрономы соединяют телескопы вместе?
- Основы химической структуры жизни
- Измерители излучений
