Книга: Общая химия
66. Термодинамические величины. Внутренняя энергия и энтальпия.
| <<< Назад 65. Факторы, определяющие направление протекания химических реакций. |
Вперед >>> 67. Термодинамические величины. Энтропия и энергия Гиббса. |
66. Термодинамические величины. Внутренняя энергия и энтальпия.
Внутренняя энергия У вещества (или системы) — это полная энергия частиц, составляющих данное вещество (см. также § 54). Она слагается из кинетической и потенциальной энергий частиц. Кинетическая энергия — это энергия поступательного, колебательного и вращательного движения частиц; потенциальная энергия обусловлена силами притяжения и отталкивания, действующими между частицами.
Внутренняя энергия зависит от состояния вещества. Изменение внутренней энергии системы ?U при том или ином процессе можно определять. Пусть в результате какого-нибудь процесса система переходит из начального состояния 1 в конечное состояние 2, совершая при этом работу А и поглощая из внешней среды теплоту Q*.
* В термохимическоих уравнениях (см. 55) положительной принято считать теплоту, выделенную системой. В уравнениях термодинамики принято обратное условие: положительной считается теплота, поглощенная системой.
- 188 -
Ясно, что внутренняя энергия системы уменьшится на величину А, возрастет на величину Q и в конечном состоянии будет равна
U2 = U1 + Q - A
где U1 и U2 — внутренняя энергия системы в начальном (1) и в конечном (2) состояниях. Если обозначить разность U2 - U1 через ?U, то уравнение можно представить в виде:
?U = Q - A
Это уравнение выражает закон сохранения энергии, согласно которому изменение внутренней энергии не зависит от способа проведения процесса, а определяется только начальным и конечным состояниями системы. Однако какая часть энергии пойдет на совершение работы, а какая превратится в теплоту — зависит от способа проведения процесса: соотношение между работой и теплотой может быть различным. В частности, если в ходе процесса не производится никакой работы, в том числе работы расширения против внешнего давления, т. е., если объем системы не изменяется, то
?U = Qv
где Qv — теплота, поглощенная системой в условиях постоянного объема.
Последнее уравнение дает возможность определять изменение внутренней энергии при различных процессах. Например, в случае нагревания вещества при постоянном объеме изменение внутренней энергии определяется по теплоемкости этого вещества:
?U = Qv = nCv?T
Здесь Cv — молярная теплоемкость вещества при постоянном объеме; n — количество вещества; ?T -разность между конечной и начальной температурами.
В случае химической реакции, протекающей без изменения объема системы, изменение внутренней энергии равно взятому с обратным знаком тепловому эффекту этой реакции.
Энтальпия. Однако чаще в химии приходится иметь дело с процессами, протекающими при постоянном давлении. При этом удобно пользоваться величиной энтальпии Н, определяемой соотношением:
H = U + PV
При постоянном давлении и при условии, что в ходе процесса совершается только работа расширения ( A = P?V )*
?H = ?U + P?V
или
?U = ?H + P?V
* Работа (А) против силы внешнего давления равна величине этой силы (F), умноженной на путь (?l), т.е. A = F?l. Но сила равна давлению (Р), умноженному на ту площадь (S), на которую оно действует: F = PS, откуда A = PS?l или A = ?V.
- 189 -
Сравнивая последнее уравнение с уравнением внутренней энергии
?U = Q - A
видим, что при указанных условиях
?H = Qp
где Qp — теплота, поглощенная системой при постоянном давлении.
Последнее уравнение дает возможность определять изменение эптальпии при различных процессах. Такие определения аналогичны определениям внутренней энергии, с той разницей, что все измерения должны проводиться в условиях постоянного давления. Так, при нагревании вещества изменение его энтальпии определяется по теплоемкости этого вещества при постоянном давлении
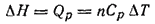
где n — количество вещества; Ср — молярная теплоемкость вещества при постоянном давлении.
При изменениях агрегатного состояния вещества и при аллотропных переходах изменение энтальпии равно по величине, но обратно по знаку теплоте соответствующего превращения (плавление, кипение, превращение из одной модификации в другую). Наконец, в случае химической реакции изменение энтальпии равно взятому с обратным знаком тепловому эффекту реакции, проведенной при постоянной температуре и постоянном давлении.
Энтальпия, как и внутренняя энергия, характеризует энергетическое состояние вещества, но включает энергию, затрачиваемую на преодоление внешнего давления, т. е. на работу расширения. Подобно внутренней энергии, энтальпия определяется состоянием системы и не зависит от того, каким путем это состояние достигнуто. В случае газов различие между ?U и ?H в ходе того или иного процесса может быть значительным. В случае систем, не содержащих газов, изменения внутренней энергии и энтальпии, сопровождающие процесс, близки друг к другу. Это объясняется тем, что изменения объема (?V) при процессах, претерпеваемых веществами в конденсированных (т. е. в твердом или в жидком) состояниях, обычно очень невелики, и величина P?V мала в сравнении с ?H .
| <<< Назад 65. Факторы, определяющие направление протекания химических реакций. |
Вперед >>> 67. Термодинамические величины. Энтропия и энергия Гиббса. |
- 54. Превращения энергии при химических реакциях.
- 55. Термохимия.
- 56. Термохимические расчеты.
- 57. Скорость химической реакции.
- 58. Зависимость скорости реакции от концентраций реагирующих веществ.
- 59. Зависимость скорости реакции от температуры и от природы реагирующих веществ.
- 60. Катализ.
- 61. Скорость реакции в гетерогенных системах.
- 62. Цепные реакции.
- 63. Необратимые и обратимые реакции. Химическое равновесие.
- 64. Смещение химического равновесия. Принцип Ле Шателье.
- 65. Факторы, определяющие направление протекания химических реакций.
- 66. Термодинамические величины. Внутренняя энергия и энтальпия.
- 67. Термодинамические величины. Энтропия и энергия Гиббса.
- 68. Стандартные термодинамические величины. Химико-термодинамические расчеты.
- 67. Термодинамические величины. Энтропия и энергия Гиббса.
- Определение величины стресса
- Жизненная энергия
- Углерод и энергия жизни
- Энергия повсюду
- 5.3.1. Внутренняя среда организма. Состав и функции крови. Группы крови. Переливание крови. Иммунитет
- § 34 Кинетическая энергия
- Эукариотическая клетка, ее внутренняя архитектура и пропасть между прокариотической и эукариотической клеточной организа...
- 5.3. Внутренняя среда организма человека. Группы крови. Переливание крови. Иммунитет. Обмен веществ и превращение энерги...
- § 33 Потенциальная энергия
- Скорость и энергия химических реакций
- § 51 Скорость и энергия химических реакций
