Книга: Общая химия
40. Неполярная и полярная ковалентная связь.
| <<< Назад 39. Ковалентная связь. Метод валентных связей. |
Вперед >>> 41. Способы образования ковалентной связи. |
40. Неполярная и полярная ковалентная связь.
Если двухатомная молекула состоит из атомов одного элемента, как, например, молекулы H2, N2, Cl2 и т.п., то каждое электронное облако, образованное общей парой электронов и осуществляющее ковалентную связь, распределяется в пространстве симметрично относительно ядер обоих атомов. В подобном случае ковалентная связь называется неполярной или гомеополярной. Если же двухатомная молекула состоит из атомов различных элементов, то общее электронное облако смещено в сторону одного из атомов, так что возникает асимметрия в распределении заряда. В таких случаях ковалентная связь называется полярной или гетерополярной.
Для оценки способности атома данного элемента оттягивать к себе общую электронную пару пользуются величиной относительной электроотрицательности. Чем больше электроотрицательность атома, тем сильнее притягивает он общую электронную пару. Иначе говоря, при образовании ковалентной связи между двумя атомами разных элементов общее электронное облако смещается к более электроотрицательному атому, и в тем большей степени, чем больше различаются электроотрицательности взаимодействующих атомов. Значения электроотрицательности атомов некоторых элементов по отношению к электроотрицательности фтора, которая принята равной 4, приведены в табл. 6*.
Таблица 6. Относительная электроотрицательность атомов
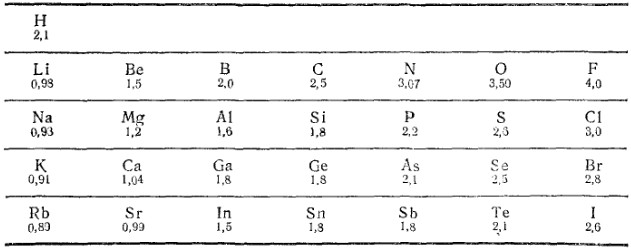
* Относительная электроотрицательность атома не является строго постоянной величиной; она зависит как от валентности, проявляемой атомом в соответствующем соединении, так и от того, с атомами каких других элементов соединен данный атом. Поэтому числа, приведенные в табл. 6, могут служить лишь для оценки направления смещения электронов при образовании молекул.
- 119 -

Рис. 29. Электрическое поле диполя.
Стрелками показаны направления силовых линий.
Как показывает табл. 6, электроотрицательность закономерно изменяется в зависимости от положения элемента в периодической системе. В начале каждого периода находятся элементы с наиболее низкой электроотрицательностью — типичные металлы, в конце периода (перед благородными газами) — элементы с наивысшей электроотрицательностью, т.е. типичные неметаллы. У элементов одной и той же подгруппы электроотрицательность с ростом заряда ядра проявляет тенденцию к уменьшению. Таким образом, чем более типичным металлом является элемент, тем ниже его электроотрицательность; чем более типичным неметаллом является элемент, тем выше его электроотрицательность.
Смещение общего электронного облака при образовании полярной ковалентной связи приводи к тому, что средняя плотность отрицательного электрического заряда оказывается выше вблизи более электроотрицательного атома и ниже — вблизи менее электроотрицательного. В результате первый атом приобретает избыточный отрицательный, а второй — избыточный положительный заряд; эти заряды принято называть эффективными зарядом атомов в молекуле.
Так, в молекуле хлороводорода общая электронная пара смещена в сторону более электроотрицательного атома хлора, что приводит к появлению у атома хлора эффективного отрицательного заряда, равного 0,17 заряда электрона, а у атома водорода такого же по абсолютной величине эффективного положительного заряда. Следовательно, молекула HCl является полярной молекулой. Ее можно рассматривать как систему из двух равных по абсолютной величине, но противоположных по знаку зарядов, расположенных на определенном расстоянии друг от друга. Такие системы называются электрическими диполями. Хотя суммарный заряд диполя равен нулю, в окружающем его пространстве образуется электрическое поле, изображенное на рис. 29. Напряженность этого поля пропорциональна дипольному моменту молекулы ?, представляющему собой произведение абсолютного значения заряда электрона q на расстояние l между центрами положительного и отрицательного зарядов в молекуле:
? = ql
Дипольный момент молекулы служит количественной мерой ее полярности. Дипольные моменты молекул обычно измеряют в дебаях (D)*: 1D = 3,33 · 10-30 Кл · м.
* Эта единица названа в честь голландского физика П. Дебая, известного своими работами в области физики твердого тела, рентгеноструктурного анализа и теории полярный жидкостей.
- 120 -
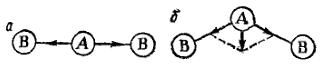
Рис. 30. Дипольные моменты отдельных связей в молекулах типа АВ2 различного строения:
а — линейное строение; б — угловое строение; жирной средней стрелкой показан вектор суммарного дипольного момента молекулы.
Молекула тем более полярна, чем больше смещена общая электронная пара к одном из атомов, т.е. чем выше эффективные заряды атомов и чем больше длина диполя l. Поэтому в ряду сходно построенных молекул дипольный момент возрастает по мере увеличения разности электроотрицательностей атомов, образующих молекулу. Например, дипольный моменты HCl, HBr и HI равны соответственно 1,04; 0,79 и 1,38 D, что связано с уменьшением разности электроотрицательностей атомов при переходе от HCl к HBr и HI (см. табл. 6).
Многоатомные молекулы также могут быть неполярными — при симметричном распределении зарядов или полярными — при асимметричном распределении зарядов. В последнем случае дипольный момент молекулы будет отличаться от нуля. Каждой связи в многоатомной молекуле можно приписать определенный дипольный момент, характеризующий ее полярность; при этом следует принимать во внимание не только величину дипольного момента, но и его направление, т.е. рассматривать дипольный момент каждой связи как вектор. Тогда суммарный дипольный момент молекулы в целом можно считать равным векторной сумме дипольных моментов отдельных связей. Дипольный момент обычно принято считать направленным от положительного конца диполя к отрицательному.
Дипольные моменты молекул можно экспериментально определять путем измерения некоторых макроскопических свойств соответствующего вещества, например, его диэлектрической проницаемости*. Найденные таким образом значения дипольных моментов содержат важную информацию о геометрической структуре молекул.
Так, на рис. 30 изображены схемы возможного строения молекулы типа АВ2; векторы дипольных моментов отдельных связей А-В показаны стрелками, направленными от А к В. При линейном строении (рис. 30, а) равные по величине дипольные моменты двух связей А — В противоположны по направлению. Следовательно, дипольный момент такой молекулы будет равен нулю.
* Диэлектрической проницаемостью (или диэлектрической постоянной) вещества называется число, показывающее, во сколько раз взаимодействие между зарядами в среде данного вещества слабее, чем в вакууме.
В случае углового строения (рис. 30, б) векторная сумма дипольных моментов двух связей А — В отличается от нуля; такая молекула обладает дипольным моментом и является полярной.
- 121 -
Поэтому наличие или отсутствие дипольного момента у молекулы типа АВ2 позволяет сделать вывод о нее геометрическом строении. Например, то, что молекула CO2 неполярна, а молекула SO2 обладает дипольным моментом (? = 1,61 D), свидетельствует о линейном строении первой молекулы и об угловом строении второй.
На рис. 31 изображены схемы возможно строения молекулы типа АВ3. Если молекула построена в форме плоского треугольника (рис. 31, а), то векторная сумма дипольных моментов отдельных связей равна нулю — молекула неполярна. Если молекула имеет пирамидальное строение (рис. 31, б), то ее суммарный дипольный момент отличается от нуля — молекула полярна. Таким образом, можно сделать вывода, что молекула BF3, дипольный момент которой равен нулю, имеет плоское строение, а полярная молекула NH3 (? = 1,46 D) построена в форме пирамиды*.
* Следует иметь в виду, что на величину дипольного момента молекулы влияет не только полярность отдельных связей и геометрическая структура молекулы, но и наличие неподеленных электронных пар на гибридных орбитах (см. стр. 132-133).
Полярность молекул оказывает заметное влияние на свойства образуемых ими веществ. Полярные молекулы стремятся ориентироваться по отношению друг к другу разноименно заряженными концами. Следствием такого диполь-дипольного взаимодействия является взаимное притяжение полярных молекул и упрочнение связи между ними. Поэтому вещества, образованные полярными молекулами, обладают, как правило, более высокими температурами плавления и кипения, чем вещества, молекулы которых неполярны.
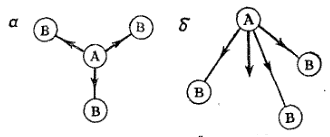
Рис. 31. Дипольные моменты отдельных связей в молекулах типа АВ3:
а — плоский треугольник; б — пирамида; жирной стрелкой показан вектор суммарного дипольного момента молекулы.
При растворении вещества, состоящего из полярных молекул или имеющих ионное строение, в жидкости, также составленной из полярных молекул, между молекулярными диполями растворителя и молекулами или кристаллами растворяемого вещества возникают электростатические силы диполь-дипольного или ион-дипольного взаимодействия, способствующие распаду растворяемого вещества на ионы (см. § 83). Поэтому жидкости, состоящие из полярных молекул, проявляют свойства ионизирующих растворителей, т.е. способствуют электролитической диссоциации растворенных в них веществ.
- 122 -
Так, хлороводород растворяется и в воде, и в бензоле, но его растворы в воде хорошо проводят электрический ток, что свидетельствует о практически полной диссоциации молекул HCl на ионы, тогда как растворы HCl в бензоле не обладают заметной электрической проводимостью.
| <<< Назад 39. Ковалентная связь. Метод валентных связей. |
Вперед >>> 41. Способы образования ковалентной связи. |
- 38. Теория химического строения.
- 39. Ковалентная связь. Метод валентных связей.
- 40. Неполярная и полярная ковалентная связь.
- 41. Способы образования ковалентной связи.
- 42. Направленность ковалентной связи.
- 43. Гибридизация атомных электронных орбиталей.
- 44. Многоцентровые связи.
- 45. Метод молекулярных орбиталей.
- 46. Ионная связь.
- 47. Водородная связь.
