Книга: Общая химия
204. Основные типы и номенклатура комплексных соединений.
| <<< Назад 203. Основные положения координационной теории. |
Вперед >>> 205. Пространственное строение и изомерия комплексных соединений. |
204. Основные типы и номенклатура комплексных соединений.
К основным типам комплексных соединений относятся следующие.
Аммиакаты — комплексы, в которых лигандами служат молекулы аммиака, например: [Cu(NH3)4]SO4, [Co(NH3)6]Cl3, [Pt(NH3)6]Cl4. Известны комплексы, аналогичные аммиакатам, в которых роль лиганда выполняют молекулы аминов: CH3NH2(метиламин), C2H5NH2(этиламин), NH2CH2CH2NH2(этилендиамин, условно обозначаемый Еп) и др. Такие комплексы называют аминатами.
Аквакомплексы — в которых лигандом выступает вода: [Co(H2O)6]Cl2 [Al(H2O)6]Cl3 [Cr(H2O)6]Cl3 и др. Находящиеся в водном растворе гидратированные катионы содержат в качестве центрального звена аквакомплекс. В кристаллическом состоянии некоторые из аквакомплексов удерживают и кристаллизационную воду, например: [Cu(H2O)4]SO4·H2O, [Fe(H2O)6]SO4·H2O. Кристаллизационная вода не входит в состав внутренней сферы, она связана менее прочно, чем координированная, и легче отщепляется при нагревании.
Ацидокомплексы. В этих комплексах лигандами являются анионы. К ним относятся комплексы типа двойных солей, например K2[PtCl4], K4[Fe(CN)6] (их можно представить как продукт сочетания двух солей — PtCl4·2KCl Fe(CN)2·4KCN и т. п.), комплексные кислоты — H2[SiF6], H2[CoCl4], гидроксокомплексы — Na2[Sn(OH)4], Na2[Sn(OH)6] и др.
Между этими классами существуют переходные ряды, которые включают комплексы с различными лигандами. О таких комплексах мы уже упоминали. Приведем переходный ряд между аммиакатами и ацидокомплексами платины(II) [Pt(NH3)4]Cl2, [Pt(NH3)3Cl]Cl, [Pt(NH3)2Cl2], K[Pt(NH3)Cl3], K[PtCl4].
Циклические, или хелатные (клешневидные), комплексные соединения. Они содержат би- или полидентатный лиганд, который как бы захватывает центральный атом подобно клешням рака:

В этих комплексах символом М обозначен атом металла, а стрелкой — донорно-акцепторная связь. Примерами таких комплексов служат оксалатный комплекс железа(III) [Fe(C2O4)3]3- и этилендиаминовый комплекс платины(IV) -[PtEn3]4+ . К группе хелатов относятся и внутрикомплексные соединения, в которых центральный атом входит в состав цикла, образуя ковалентные связи с лигандами разными способами: донорно-акцепторным и за счет неспаренных атомных электронов. Комплексы такого рода весьма характерны для аминокарбоновых кислот.
- 569 -
Простейший их представитель — амииоуксусная кислота (глицин) NH2CH2COOH — образует хелаты с ионами Cu2+, Pt2+, Rh3+, например:
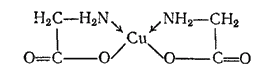
Известны также комплексы с более сложными амннокарбоновыми кислотами и их аналогами. Такие лиганды называются комплексонами. Двухзарядный анион этилендиамиптетрауксусной кислоты, называемый в виде двунатриевой соли комплексоном III, или трилоном Б, дает с двухвалетным металлом комплекс типа:
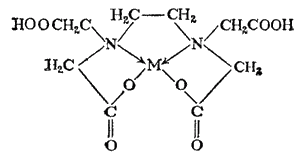
Хелатные соединения отличаются особой прочностью, так как центральный атом в них как бы «блокирован» циклическим лигандом. Наибольшей устойчивостью обладают хелаты с пяти- и шестичленными циклами. Комплексоны настолько прочно связывают катионы металлов, что при их добавлении растворяются такие плохо растворимые вещества, как сульфаты кальция и бария, оксалаты и карбонаты кальция. Поэтому их применяют для умягчения воды, для маскировки «лишних» ионов металла при крашении и изготовлении цветной пленки. Большое применение они находят и в аналитической химии.
Многие органические лиганды хелатного типа являются весьма чувствительными и специфическими реагентами на катионы переходных металлов. К ним относится, например, диметилглиоксим, предложенный Л. А. Чугаевым как реактив на ионы Ni2+, и Pd2+,.

Лев Александрович Чугаев (1873—1922)
Лев Александрович Чугаев принадлежит к числу наиболее выдающихся советских химиков. Родился в Москве, в 1895 г. окончил Московский университет. В 1904-1908 — профессор Московского высшего технического училища, в 1908—1922 г. — профессор неорганической химии Петербургского университета и одновременно (с 1909 г.) - профессор органической химии Петербургского технологического института.
- 570 -
Занимался изучением химии комплексных соединений переходных металлов, в особенности металлов платиновой группы. Открыл много новых комплексных соединений, важных в теоретическом и практическом отношениях. Чугаев впервые обратил внимание на особую устойчивость 5- и 6-членных циклов во внутренней сфере комплексных соединений и охарактеризовал кислотно-основные свойства аммиакатов платины (IV). Он был одним из основоположников применения органических реагентов в аналитической химии. Много внимания уделял организации и развитию промышленности по добыче и переработке платины и платиновых металлов в СССР. Создал большую отечественную школу химиков-неоргаников, работающих в области изучения химии комплексных соединений.
Большую роль играют хелатные соединения и в природе. Так, гемоглобин состоит из комплекса — гема, связанного с белком — глобином. В геме центральным ионом является ион Fe2+, вокруг которого координированы четыре атома азота, принадлежащие к сложному лиганду с циклическими группировками. Гемоглобин обратимо присоединяет кислород и доставляет его из легких по кровеносной системе ко всем тканям. Хлорофилл, участвующий в процессах фотосинтеза в растениях, построен аналогично, но в качестве центрального иона содержит Mg2+.
Все перечисленные классы комплексных соединений содержат один центральный атом, т. е. являются одноядерными. Встречаются комплексы и более сложной структуры, содержащие два или несколько центральных атомов одного и того же или разных элементов. Эти комплексы называются поли(много)ядерными.
Существуют различные типы полиядерных комплексов.
Комплексы с мостиковыми атомами или группами атомов, например с мостиковыми атомами хлора
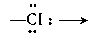
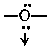
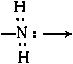
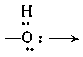
Комплексы кластерного типа, в которых атомы металла непосредственно связаны друг с другом. Это наблюдается, например, в димерах (CO)5Mn-Mn(CO)5, [Re2H2Cl8]2-. В последнем соединении между атомами рения имеется тронная связь:
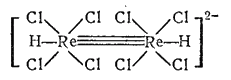
К многоядерным соединениям относятся также изополикислоты.
Изополикислоты образуются при соединении двух или нескольких кислотных остатков одной и той же кислородной кислоты за счет кислородных мостиков. В их число входят двухромовая H2CrO7, пирофосфорная H4P2O7, тетраборная H2B4O7 кислоты, а также поликремниевые кислоты, составляющие основу силикатов.
- 571 -
Гетерополикислоты содержат не менее двух различных кислот или оксидов (производных неметалла и металла) и большое количество воды (до 30 молекул). Наиболее важное значение в аналитической химии имеют следующие гетерополикпслоты:
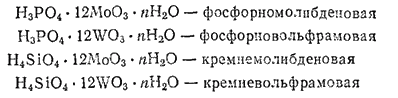
Известно немного комплексов, в которых центром координации является акнон, — это полигалогениды, содержащие анионы [I·xI2]-(где x меняется от 1 до 4) или [Br·xBr2]-(где x 1 или 2); существуют и смешанные полигалогенидные анионы — [I·xBr2]-, [I·xCl2]-. Большую роль при их образовании играет поляризация: чем больше интенсивность поляризационного взаимодействия между анионом Э- и молекулой Э2, тем устойчивее комплекс. Именно поэтому наиболее устойчивыми из них оказываются полииодиды (молекулы 12 легко поляризуются), а полифториды не получены. Вследствие наличия в растворе равновесия
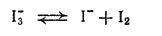
раствор полииодида обнаруживает свойства свободного иода.
Существует много способов образования названий комплексных соединений, в том числе и традиция называть их по фамилиям исследователей, их открывших. Такой способ, хотя и отдает дань уважения ученым, сложен для запоминания. Мы приведем номенклатуру главнейших типов комплексных соединений, основанную на рекомендациях Международного союза теоретической и прикладной химии.
Название комплексного аниона начинают с указания состава внутренней сферы.
Во внутренней сфере, прежде всего называют анионы, прибавляя к их латинскому названию окончание "o". Например: Cl- - хлоро, CN- — циано, SO32- — сульфито, OH- — гидрэксо и т. д. Далее называют нейтральные лиганды. При этом пользуются терминами: для координированного аммиака — аммин, для воды — аква. Число лигандов указывают греческими числительными: 1 — моно (часто не приводится), 2 — ди, 3 — три, 4 — тетра, 5 — пента, 6 — гекса. Затем называют комплексообразователь, используя корень его латинского названия и окончание ат, после чего римскими цифрами указывают (в скобках) степень окисленности комплексообразователя. После обозначения состава внутренней сферы называют внешнесферные катионы. В случае неэлектролитов степень окисленности центрального атома не приводят, так как она однозначно определяется, исходя из электронейтральности комплекса.
- 572 -
Если центральный атом входит в состав катиона, то используют русское название элемента и в скобках указывают его степень окисленности. Приведем примеры:

| <<< Назад 203. Основные положения координационной теории. |
Вперед >>> 205. Пространственное строение и изомерия комплексных соединений. |
- 203. Основные положения координационной теории.
- 204. Основные типы и номенклатура комплексных соединений.
- 205. Пространственное строение и изомерия комплексных соединений.
- 206. Природа химической связи в комплексных соединениях.
- 207. Диссоциация комплексных соединений в растворах.
- 208. Влияние координации на свойства лигандов и центрального атома.
- 205. Пространственное строение и изомерия комплексных соединений.
- 32. Селекция: основные методы и достижения
- 2. Систематика и номенклатура микроорганизмов
- 4. Морфология бактерий, основные органы
- Глава 4. ОСНОВНЫЕ СРЕДЫ ЖИЗНИ И АДАПТАЦИИ К НИМ ОРГАНИЗМОВ
- 17. Основные осложнения химиотерапии
- Основные этапы формирования мирового хозяйства
- Основные типы стран современного мира
- 3.4. Основные пути приспособления живых организмов к условиям среды
- Основные виды природных ресурсов
- § 69. Основные свойства популяций
- ОСНОВНЫЕ ГРУППЫ ПРОКАРИОТ
