Книга: Общая химия
149. Мышьяк (Arsenicum).
| <<< Назад 148. Минеральные удобрения. |
Вперед >>> 150. Сурьма (Stibium). |
149. Мышьяк (Arsenicum).
Мышьяк встречается в природе большей частью в соединениях с металлами или серой и лишь изредка в свободном состоянии. Содержание мышьяка в земной коре составляет 0,0005% (масс.).
Обычно мышьяк получают из мышьяковистого колчедана FeAsS.
- 411 -
При его нагревании в атмосфере воздуха образуется оксид мышьяка (III) As2O3, который далее восстанавливают углем до свободного мышьяка.
Подобно фосфору, мышьяк существует в нескольких аллотропических модификациях. Наиболее устойчив при обычных условиях и при нагревании металлический, или серый, мышьяк. Он образует серостальную хрупкую кристаллическую массу с металлическим блеском на свежем изломе. Плотность серого мышьяка равна 5,72 г/см3. При нагревании под нормальным давлением он сублимируется. В отличие от других модификаций, серый мышьяк обладает металлической электрической проводимостью.
В воде мышьяк нерастворим. На воздухе при комнатной температуре он окисляется очень медленно, а при сильном нагревании сгорает, образуя белый оксид As2O3 и распространяя характерный чесночный запах. При высокой температуре мышьяк непосредственно взаимодействует со многими элементами. Сильные окислители переводят его в мышьяковую кислоту, например:
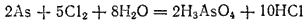
Как свободный мышьяк, так и все его соединения — сильные яды.
В соединениях мышьяк проявляет степень окисленности +5.
Гидрид мышьяка, или арсин, AsH3 представляет собой бесцветный, очень ядовитый газ с характерным чесночным запахом, мало растворимый в воде. Арсин образуется при восстановлении всех соединений мышьяка водородом в момент выделения. Например:

Арсин сравнительно нестоек и при нагревании легко разлагается на водород и свободный мышьяк. Это свойство арсин а используется для открытия мышьяка в различных веществах. На анализируемое вещество действуют восстановителем и, если в нем содержится какое-либо соединение мышьяка или мышьяк в свободном состоянии, то образуется AsH3. Далее продукты восстановления нагревают, арсин разлагается, а выделяющийся мышьяк образует на холодных частях прибора характерный черный блестящий налет, называемый «мышьяковым зеркалом».
С некоторыми металлами мышьяк образует соединения — арсениды, многие из которых можно рассматривать как продукты замещения водорода в арсине атомами металла — например, Cu3As, Ca3As2.
С кислородом мышьяк образует два оксида: As2O3 и As2O5.
Оксид мышьяка(III), или мышьяковистый ангидрид, As2O3 образуется при сгорании мышьяка на воздухе или при прокаливании мышьяковых руд. Это вещество белого цвета, которое называют белым мышьяком. Оксид мышьяка (III) довольно плохо растворяется вводе: насыщенный при 15°C раствор со держит всего 1,5% As2O3.
- 412 -
При растворении в воде оксид мышьяка (III) взаимодействует с нею, и образуется гидроксид мышьяка (III) или мышьяковистая кислота:
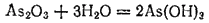
Гидроксид мышьяка (III) амфотерен, но у него преобладают кислотные свойства.
Ортомышьяковистая (или мышьяковистая) кислота H3AsO3 в свободном состоянии не получена и известна лишь в водном растворе, в котором устанавливается равновесие:

Это равновесие сильно смещено вправо, т. е. преобладающей формой является метамышьяковистая кислота HAsO2. Константа диссоциации этой кислоты K=6·10-10. При действии щелочей на As2O3 получаются соли мышьяковистой кислоты — арсениты, - например

Соединения мышьяка (III) проявляют восстановительные свойства; при их окислении получаются соединения мышьяка (V).
Мышьяковая кислота H3AsO4 при обычных условиях находится в твердом состоянии; она хорошо растворима в воде. По силе мышьяковая кислота почти равна фосфорной. Соли ее — арсенаты — очень похожи на соответствующие фосфаты. Известны также мета- и двумышьяковая кислоты. При прокаливании мышьяковой кислоты получается оксид мышьяка (V), или мышьяковый ангидрид, As2O5 в виде белой стеклообразной массы.
Кислотные свойства мышьяковой кислоты выражены значительно сильнее, чем у мышьяковистой. В этом проявляется рассмотренная на стр. 357 и 358 общая закономерность, согласно которой с повышением степени окисленности элемента кислотные свойства его гидроксидов усиливаются, а основные — ослабевают.
Будучи трехосновной, мышьяковая кислота образует средние (арсенаты) и кислые (гидро- и дигидроарсенаты) соли, например Na3AsO4, Na2HAsO4, NaH2AsO4.
В кислой среде мышьяковая кислота и арсенаты проявляют свойства окислителей.
В § 99 отмечалось, что электродные потенциалы процессов, протекающих с участием воды, ионов водорода или гидроксид-иопов, имеют тем большую величину, чем кислее раствор. Иначе говоря, если в электрохимическом процессе принимает участие вода и продукты ее диссоциации, то окислитель сильнее проявляет окислительные свойства в кислой среде, а восстановитель сильнее проявляет восстановительные свойства в щелочной среде. Эта общая закономерность хорошо видна на примере соединений мышьяка. Мышьяковая кислота и ее соли в кислой среде взаимодействуют с восстановителями, переходя в мышьяковистую кислоту или в арсениты. Например:
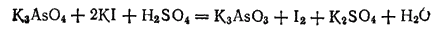
- 413 -
Здесь процесс восстановления описывается уравнением:
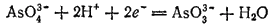
а процесс окисления — уравнением:
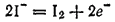
Видно, что восстановление протекает с участием воды и ионов H+, а окисление — без их участия. Следовательно, pH среды влияет только на потенциал процесса восстановления: чем меньше pH, тем выше этот потенциал и тем более сильным окислителем является AsO43-.
В то же время в щелочной среде мышьяковистая кислота и ее соли легко окисляются, переходя в арсенаты, например:
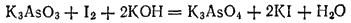
Здесь процесс восстановления описывается уравнением:
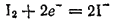
а процесс окисления — уравнением:
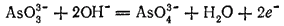
В этом случае вода и ионы ОН- принимают участие только в окислении. Следовательно, здесь pH среды влияет лишь на потенциал процесса окисления: чем больше pH, тем ниже этот потенциал и тем более сильным восстановителем служит AsO33-.
Таким образом, мы видим, что направление протекания окислительно-восстановительных реакций, идущих с участием воды и продуктов ее диссоциации, может изменяться при переходе от кислой среды к щелочной.
Сульфиды мышьяка. Если пропускать сероводород в подкисленный соляной кислотой раствор мышьяковистой кислоты, то образуется желтый осадок сульфида As2S3, нерастворимый в соляной кислоте. Происходящие реакции можно выразить уравнениями
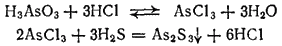
Аналогично можно получить желтый осадок сульфида мышьяка(V) As2S5, действуя сероводородом на раствор мышьяковой кислоты в присутствии соляной кислоты:
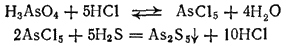
При взаимодействии сульфидов мышьяка с сульфидами щелочных металлов Na2S, K2S или с сульфидом аммония (NH4)2S образуются растворимые в воде соли тиомышьяковистой (H3AsS3) и тиомышьяковой (H3AsS4) кислот. Кислоты H3AsS3 и H3AsS4 можно рассматривать как соответствующие кислородсодержащие кислоты мышьяка, в которых весь кислород замещен серой:
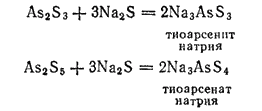
Применение свободного мышьяка ограничено.
- 414 -
Но соединения мышьяка применяют в медицине, а также в сельском хозяйстве, где они используются в качестве инсектицидов, т. е. средств для уничтожения вредных насекомых.
Оксид мышьяка (III) применяется как яд для уничтожения грызунов.
| <<< Назад 148. Минеральные удобрения. |
Вперед >>> 150. Сурьма (Stibium). |
- АЗОТ (NITROGENIUM)* 136. Азот в природе. Получение и свойства азота.
- 137. Аммиак. Соли аммония.
- 138. Фиксация атмосферного азота. Получение аммиака.
- 139. Гидразин. Гидроксиламин. Азидоводород.
- 140. Оксиды азота.
- 141. Азотистая кислота.
- 142. Азотная кислота.
- 143. Промышленное получение азотной кислоты.
- 144. Круговорот азота в природе.
- ФОСФОР (PHOSPHORUS) 145. Фосфор в природе. Получение и свойства фосфора.
- 146. Соединения фосфора с водородом и галогенами.
- 147. Оксиды и кислоты фосфора.
- 148. Минеральные удобрения.
- 149. Мышьяк (Arsenicum).
- 150. Сурьма (Stibium).
- 151. Висмут (Bismuthum).
